注重提煉“問題解決”的思維導圖在復習教學中實踐
史月英
【摘要】遇到新情景或陌生反應體系中的問題時,學生思維會陷入慌亂。為了幫助學生形成“問題解決”有套路意識,教師在總復習教學中有意識構建“化學反應的本質特征”思維導圖,通過可視化的圖像讓學生提煉“問題解決”的一般步驟,并通過實驗方案的分析、反思、感悟,幫助學生內化原知能力。
【關鍵詞】復習教學;問題解決;“化學反應的本質特征”思維導圖
在初中化學總復習教學過程中經常出現這樣的情況:盡管學生會認識化學概念、原理和事實“是什么”,但在解決化學問題時往往表現沒有思路或思路不清,遇到新情景或陌生反應體系中的問題就無從下手,不知怎么辦,思維陷入慌亂。
針對以上問題,筆者認為在總復習教學中應有意識地適時地幫助學生構建可視化的思維導圖。這種教學工具不僅能將學生的零散、細節知識轉化為整體知識,有意識、有目的、連貫性地對問題進行分析、反思、評價,而且能在不知不覺中克服學生依賴教師幫助解決問題的思想意識,使學生學會終身學習和解決問題的能力。因此,教師首先要意識到思維導圖的重要性,其次在教學過程中要設計適當的問題,利用問題鏈引導學生探索,在探究中獲取解決問題的思路,并領悟出解決此類問題的共同過程。
一、 構建“化學反應的本質特征”思維導圖,形成“問題解決”有套路的意識
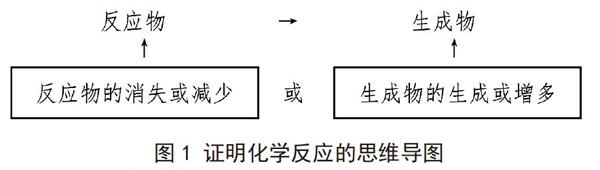
化學中無明顯現象不等于物質間沒有發生化學反應,要探究是否發生化學反應,就要引導學生從兩個角度分析:第一,反應物的消失或減少;第二,生成物的生成或增多。展示思維導圖1,通過直觀的圖像讓學生提煉“問題解決”的一般步驟,形成“問題解決”有套路的意識。
二、教學實踐
(一)案例一:探究二氧化碳與氫氧化鈉發生無明顯現象的化學反應
二氧化碳與氫氧化鈉反應是初中化學中很重要的反應,屬于常見堿的化學性質。由于二氧化碳與氫氧化鈣反應生成難溶于水的碳酸鈣,可以通過有白色沉淀的現象來驗證反應的發生,而二氧化碳與氫氧化鈉反應生成可溶于水的碳酸鈉,無法通過明顯現象驗證反應的發生。
在對沒有明顯現象的反應進行探究時,一些教師不是花時間幫助學生進行理清和整合,而是在課堂上反反復復講,然后讓學生一遍又一遍練習,當學生遇到新情景或復雜問題時,又會出現思維混亂、無從下手的局面。從復習的功能上看,過分強調物質性質的復習和記憶,沒有幫助學生建立解決化學問題的思維框架,不知不覺又陷入“冷飯重炒”的尷尬局面。這種總復習模式讓教師和學生都感到無趣和備受煎熬。
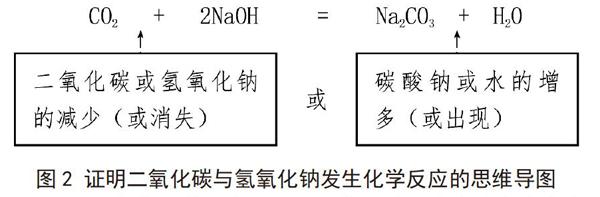
因此,在復習過程中,教師要引導學生依據“化學反應的思維導圖”,同時根據“書寫新情境下的化學方程式”思維導圖(即圖2)來自主探究,通過改變儀器或試劑,實現從“無”到“有”的轉化。
1.如果發生化學反應,那么二氧化碳就減少(或消失)。由于二氧化碳是氣體,氣體越多,氣壓越大;反之,氣體越少,氣壓越小。可以借助反應裝置或儀器證明二氧化碳減少。
2.如果發生化學反應,那么氫氧化鈉就減少(或消失)。氫氧化鈉水溶液呈堿性,通常用酸堿指示劑。但由于生成碳酸鈉在水溶液中也是呈堿性,所以借助酸堿指示劑證明氫氧化鈉消失不合理。
3.如果發生化學反應,那么就有碳酸鈉生成。可以借助合適的試劑證明碳酸鈉的生成,如取反應后的溶液,在試管中滴加鹽酸或氯化鋇溶液,根據有氣泡生成或有白色沉淀生成,證明有新物質生成。
4.如果發生化學反應,那么就有水生成。由于該反應是在水溶液中進行的,就使用固體氫氧化鈉,但固體氫氧化鈉很容易吸水變潮,所以不易用實驗證明有水生成。
以上方案的分析、反思,不僅幫助學生理清了解決問題最普遍的思維形式,而且提高了學生的原認知能力。第一,做到實驗的合理性。在利用物質性質探究過程中還要考慮其他方面的影響因素,如碳酸鈉也呈堿性,會干擾氫氧化鈉的檢驗,用指示劑檢驗氫氧化鈉消失不合理。第二,做到實驗的嚴謹性。二氧化碳與氫氧化鈉溶液反應,而溶液中有水,二氧化碳會溶解于水,氣體減少是否是由于二氧化碳溶于水造成的呢?所以需做對比實驗,利用控制變量(把氫氧化鈉溶液變成蒸餾水)進行實驗,觀察變化程度來證明二氧化碳不僅溶于水,而且與氫氧化鈉反應。通過這些問題的討論,拓展學生多角度分析問題,培養學生實驗的嚴謹性。
(二)案例二:探究氫氧化鈉溶液與鹽酸發生無明顯現象的中和反應
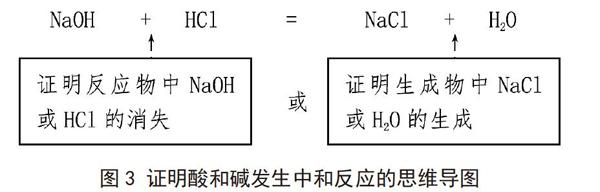
中和反應是屬于“酸和堿的性質與反應”的內容,一些學生對中和反應的定義會做文字表述,也記住了教材中的設計方案及現象,但是為什么必須借助無色酚酞試劑實現從“無”到“有”的轉化,學生往往說不清,對于用其他方法證明酸和堿發生中和反應,往往又難以下手。所以對中和反應的教學,不能只讓學生知道教材的設計方案,要讓學生知其然并知其所以然。教師要引導學生依據“化學反應的思維導圖”(即圖1),同時根據“書寫新情境下的化學方程式思維導圖”(即圖3),來找尋合理方案。
教師提出1:如何用實驗證明燒杯中氫氧化鈉在滴入鹽酸后,NaOH消失(或堿性減弱)?
學生設計方案1:在含有酚酞的氫氧化鈉溶液中慢慢滴入鹽酸,酚酞從紅色變無色,證明NaOH消失;或用pH試紙分別測定反應前后堿性的變化。
教師提出2:如何用實驗證明燒杯中鹽酸在滴入氫氧化鈉溶液后,HCl消失(或酸性減弱)?
學生設計方案2:在含有石蕊的鹽酸中慢慢滴入氫氧化鈉溶液,石蕊從紅色變紫色;或用pH試紙分別測定反應前后酸性的變化。
教師提出3:如何用實驗證明燒杯中氫氧化鈉溶液與鹽酸反應后有NaCl新物質生成?
學生設計方案3:在玻片上小心蒸發用足量鹽酸中和氫氧化鈉溶液樣品,在玻片上得到白色固體粉末,用實驗證明是NaCl(鹽酸蒸發,不會留下固態物質;得到白色固體物質溶于水,溶液不會使酚酞變紅則不是氫氧化鈉;根據反應前后組成的元素不變,水分蒸發,余下的固體是NaCl)。
教師提出4:如何用實驗證明燒杯中氫氧化鈉溶液與鹽酸反應后有新物質H2O生成?
學生設計方案4:由于該反應是在水溶液中進行的,難以用實驗證明是否有新物質H2O的生成(如果要證明酸和堿中和反應有H2O生成,必須把反應物的酸和堿換成無水的酸和干燥的堿進行實驗)。
教師提出5:通過以上幾個方案對比,選擇出哪種方案更好?
學生設計方案5:借助無色酚酞試劑證明鹽酸和氫氧化鈉發生反應這種方案最好。
通過以上的提問、感悟,學生不僅形成了“問題解決”有套路意識,而且理清了解決問題的一切細枝末節。第一,做到關注實驗的細節性。當借助酸堿指示劑驗證酸和堿中和反應時,多一滴少一滴都會造成酸堿度較大變化,如何證明酸和堿恰好反應,實驗時就要注意緩慢滴入酸或堿,最好選擇精密儀器滴入。第二,做到評價實驗的優劣性。借助紫色石蕊試液理論上是可行的,但顏色變化不明顯,不便觀察,而借助無色酚酞試液證明氫氧化鈉消失,現象明顯,為最佳方案。
三、總結“化學反應的本質特征”思維導圖在總復習教學中的作用
在化學教學總復習中引入思維導圖的作用主要體現在:思維導圖的運用不僅可以將零散的物質性質進行整合和關聯,而且能幫助學生搭建思考的橋梁,跨越思維障礙,可以輕松地得出正確的解決方法。教學實踐證明,學生在面對探究化學問題時,絕大部分往往會陷入迷茫中,究其原因,是學生解題時出現思維障礙。這時學生需要一個“引導者”才能跨越這個障礙。如何基于不同的化學知識問題,借助思維導圖,引導學生圍繞化學學科知識的實質性進行思維,值得進一步研究。
【參考文獻】
[1]郝建武.利用“列表法”教會學生思考——以初中化學“無明顯現象反應的探究”復習課教學為例[J].中學化學教與學,2017(02):43.
[2]張興濤.思維導圖在化學教學中的實踐探索[J].化學教學,2017(02):52.
[3]王云生.王云生的中學化學教學主張[M].北京:中國輕工業出版社,2014.
[4]薛青峰.基于問題導引圖示教學法的實踐與反思——以“從鋁土礦到鋁合金”教學為例[J].化學教學,2017(06):57.

