電針聯合硫辛酸治療肝胃郁熱型糖尿病周圍神經病變的臨床研究
葛俠 費愛華 方朝暉 張慶萍
〔摘要〕 目的 觀察電針聯合硫辛酸對糖尿病周圍神經病變(diabetic peripheral neuropathy, DPN)患者神經功能、神經傳導速度、脂代謝以及炎性指標的影響。方法 72例DPN患者按隨機數字表法分為治療組和對照組,各36例,兩組均采取常規基礎治療,治療組在此基礎上加用電針治療,每次30 min,1次/d,治療4周。對比兩組患者治療前后的臨床療效評分、神經傳導速度、C反應蛋白(high-sensitrity c-reactive protein, hs-CRP)、白細胞介素-6(interleukin-6, IL-6)、甘油三酯(triglyceride, TG)、總膽固醇(total cholesterol, TC)、低密度脂蛋白膽固醇(low density lipoproten-cholesterol, LDL-C)、體質量指數(body mass index, BMI)的變化。結果 (1)兩組治療后多倫多臨床評分系統(Toronto clinical scoring system, TCSS)均較治療前下降,且治療組低于對照組(P<0.05)。(2)兩組治療后神經傳導速度均較治療前提高,且治療組高于對照組(P<0.05)。(3)兩組治療后hs-CRP、IL-6均較治療前降低,且治療組低于對照組(P<0.05)。(4)兩組治療后TG、TC、LDL-C、BMI均較治療前降低,且治療組低于對照組(P<0.05)。結論 電針聯合硫辛酸可促進DPN患者的神經功能恢復,減輕炎性反應,改善脂代謝,提高神經傳導速度,值得臨床借鑒和推廣。
〔關鍵詞〕 糖尿病周圍神經病變;肝胃郁熱證;電針;神經功能;脂代謝;炎性指標;臨床療效
〔中圖分類號〕R245? ? ? ?〔文獻標志碼〕A? ? ? ? 〔文章編號〕doi:10.3969/j.issn.1674-070X.2023.06.023
〔Abstract〕 Objective To observe the effects of electroacupuncture combined with lipoic acid on nerve function, nerve conduction velocity (NCV), lipid metabolism, and inflammatoryindex in patients with diabetic peripheral neuropathy (DPN). Methods A total of 72 DPN patients were randomly divided into treatment group (n=36) and control group (n=36). Both groups received routine basic treatment, on this basis, the treatment group was treated with electroacupuncture for 30 min, once per day for 4 weeks. Then the changes of clinical efficacy score, NCV, high-sensitivity c-reactive protein (hs-CRP), interleukin-6 (IL-6), triglyceride (TG), total cholesterol (TC), low density lipoprotein-cholesterol (LDL-C), and body mass index (BMI) were compared between two groups before and after treatment. Results (1) After treatment, the Toronto clinical scoring system (TCSS) scores of both groups were lower than those before treatment, and the scores in treatment group was lower than those in control group (P<0.05). (2) The NCV of the two groups after treatment was higher than that before treatment, and the velocity in treatment group was higher than that in control group (P<0.05). (3) After treatment, the levels of hs-CRP and IL-6 in both groups were lower than those before treatment, and the above levels in treatment group was lower than those in control group (P<0.05). (4) The levels of TG, TC, LDL-C, and BMI in both groups after treatment were lower than those before treatment, and the above levels in treatment group were lower than those in control group (P<0.05). Conclusion Electroacupuncture combined with lipoic acid can promote the recovery of nerve function, reduce inflammatory response, improve lipid metabolism, and increase nerve conduction velocity in DPN patients, which is worthy of clinical application and promotion.
〔Keywords〕 diabetic peripheral neuropathy; liver-stomach heat pattern; electroacupuncture; nerve function; lipid metabolism; inflammatory index; clinical efficacy
糖尿病周圍神經病變(diabetic peripheral neur?
opathy, DPN)的發病率非常高,大約1/2的糖尿病患者以及1/3的糖尿病前期患者會發生DPN[1-2]。DPN主要臨床表現是下肢遠端的嚴重燒灼感和刺痛感,除疼痛外,DPN還可能與失眠、情緒障礙、燒燙傷、跌倒和社交恐懼癥有關。目前,臨床上治療該病多以給予營養神經、改善微循環為主,短期可使患者癥狀好轉,但無法改善患者的長期預后。臨床發現,體型較胖的DPN患者除雙下肢麻木、疼痛、感覺異常等外,多伴隨脘腹痞滿、口膩不渴、心煩口苦、舌紅、苔黃、脈弦數等,辨證分型多為肝胃郁熱型。安徽中醫藥大學第二附屬醫院內分泌科采取常規基礎治療合并電針治療該類型患者,發現此治療方案可明顯改善患者臨床癥狀、減輕炎性反應、改善脂質代謝、提高神經傳導速度,現報道如下。
1 資料與方法
1.1? 一般資料
選取2021年8月至2022年10月收治的72例肝胃郁熱型DPN住院患者,按隨機數字表法分為治療組(36例)和對照組(36例)。治療組男性21例,女性15例,年齡32~76(57.19±9.52)歲,糖尿病病程(8.83±3.72)年,空腹血糖(7.88±1.21) mmol/L,體質量指數(body mass index, BMI)(26.20±1.51) kg/m2;對照組男性20例,女性16例,年齡34~75(56.28±8.31)歲,糖尿病病程(9.14±3.89)年,空腹血糖(7.89±1.17) mmol/L,BMI(26.09±1.57) kg/m2。兩組患者一般資料比較,差異均無統計學意義(P>0.05),具有可比性。
1.2? 病例選擇標準
1.2.1? 中醫診斷標準? 參照《糖尿病周圍神經病變中醫臨床診療指南》[3]中診斷標準:患者有明確病史,主癥見下肢麻木、疼痛、感覺異常等,兼癥見肢體麻木不仁、脘腹痞滿、口黏膩不欲飲、煩躁口苦、舌紅、苔黃、脈弦數等。
1.2.2? 西醫診斷標準? 參考中華醫學會糖尿病學分會制定的《中國2型糖尿病防治指南(2020年版)》[4]中的診斷標準:病史明確;診斷糖尿病時或之后出現的神經病變;患者臨床癥狀(疼痛、麻木不適、感覺異常等)和體征(踝反射、振動覺、壓力覺等)與該病相符;排除其他致病因素導致的該病;有明確的肌電圖檢查異常結果。
1.2.3? 納入標準? 符合上述診斷標準;年齡在18~80歲;中醫辨證分型為肝胃郁熱證;患者為初次治療該病并簽署研究知情同意書。
1.2.4? 排除標準? 合并較重的基礎病,例如嚴重心力衰竭、肝腎功能不全;針刺部位皮膚病變;因其他因素(如頸腰椎疾病、吉蘭-巴雷綜合征)出現周圍神經病變;處于妊娠期或哺乳期的女性。
1.3? 治療方法
1.3.1? 對照組? 患者均給予常規中西醫結合治療及糖尿病健康宣教;調控血糖處理;均給予抗氧化、營養神經治療:注射用硫辛酸600 mg(四川美大康華康藥業,批號:H20183110)配伍0.9%氯化鈉注射液250 mL靜脈滴注,1次/d,靜脈滴注1個療程,2周。
1.3.2? 治療組? 常規基礎治療聯合清熱通絡電針處理,常規基礎治療同對照組。取穴:曲池、合谷、行間、大椎、胰俞、肺俞、脾俞、腎俞、陽陵泉、血海、足三里、三陰交。操作方法:除大椎穴外,余穴均雙側取穴,華佗牌毫針(0.30 mm×40 mm)直刺,深度為20~35 mm,得氣之后,大椎、曲池、行間三穴毫針刺入得氣后行提插、捻轉瀉法30 s,其余穴位平補平瀉手法行針30 s,必要時輔助手法助得氣。陽陵泉和足三里作為一對、血海和三陰交作為一對分別接電針儀(KWD-808I型,英迪電子醫療器械有限公司),選用疏密波,緩慢調節電流強度(由小到大),在患者耐受范圍,最好可見穴位局部肌肉有顫動或麻刺感,持續時間為30 min,1次/d,治療4周。
1.4? 觀察指標
1.4.1? 臨床功能評估? 采用多倫多臨床評分系統(Toronto clinical scoring system, TCSS)進行評定[5],評定內容具體包括:下肢麻木、疼痛、乏力等神經癥狀評分,踝反射、膝反射等神經反射評分,溫度覺、觸壓覺、振動覺、位置覺等感覺功能評分。評分區間為0~19分,分值與病情嚴重程度成正相關。
1.4.2? 神經傳導速度評定? 采用肌電圖誘發電位儀(型號:NDI-099,蘇州海神聯合醫療器械有限公司)分別測定兩組患者治療前、后脛神經與腓總神經的運動神經傳導速度(motor nerve conduction velocity, MNCV)和感覺神經傳導速度(sensory nerve conduction velocity, SNCV)。
1.4.3? 炎性指標測定? 早上6點空腹取血,采用酶聯免疫吸附法測定兩組患者治療前后炎癥因子[C反應蛋白(high-sensitrity c-reactive protein, hs-CRP)、白細胞介素-6(interleukin-6, IL-6)]水平。
1.4.4? 脂代謝指標測定? 早上6點空腹取血,測定兩組患者治療前后脂代謝指標[甘油三酯(triglyceride, TG)、總膽固醇(total cholesterol, TC)、低密度脂蛋白膽固醇(low density lipoproten-cholesterol, LDL-C)]。
1.4.5? BMI測定? 早上6點空腹測定兩組患者治療前后BMI。
1.4.6? 臨床療效判定標準? 參照《中藥新藥臨床研究指導原則(試行)》[6]進行療效評定。顯效:癥狀明顯好轉,接近正常,脛神經和腓總神經傳導速度接近正常;有效:癥狀好轉,脛神經和腓總神經傳導速度好轉,仍不正常;無效:癥狀未改善甚至加重,脛神經和腓總神經傳導速度不變甚至降低。總有效率=(顯效例數+有效例數)/總病例數×100%。
1.5? 統計學方法
采用SPSS 22.0 軟件分析。計量資料以“x±s”表示,組內治療前后比較采用配對設計的t檢驗;組間比較采用方差分析,非正態分布或方差不齊時采用秩和檢驗。以P<0.05為差異有統計學意義。
2 結果
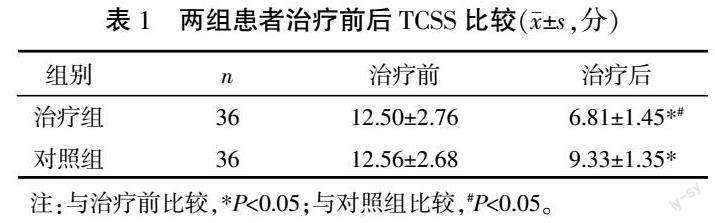
2.1? 兩組患者治療前后TCSS比較
治療前,兩組患者TCSS差異無統計學意義(P>0.05)。治療后,兩組患者TCSS較治療前下降(P<0.05),且治療組TCSS低于對照組(P<0.05)。詳見表1。
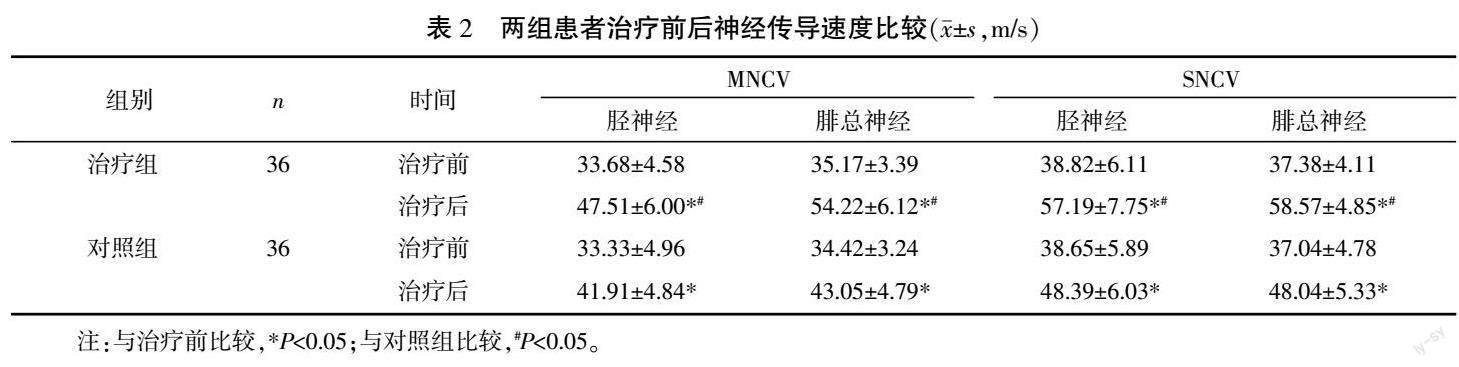
2.2? 兩組患者治療前后神經傳導速度比較
治療前,兩組患者脛神經與腓總神經的MNCV、SNCV差異無統計學意義(P>0.05)。治療后,兩組患者上述神經傳導速度均較治療前明顯提高(P<0.05),且治療組高于對照組(P<0.05)。詳見表2。
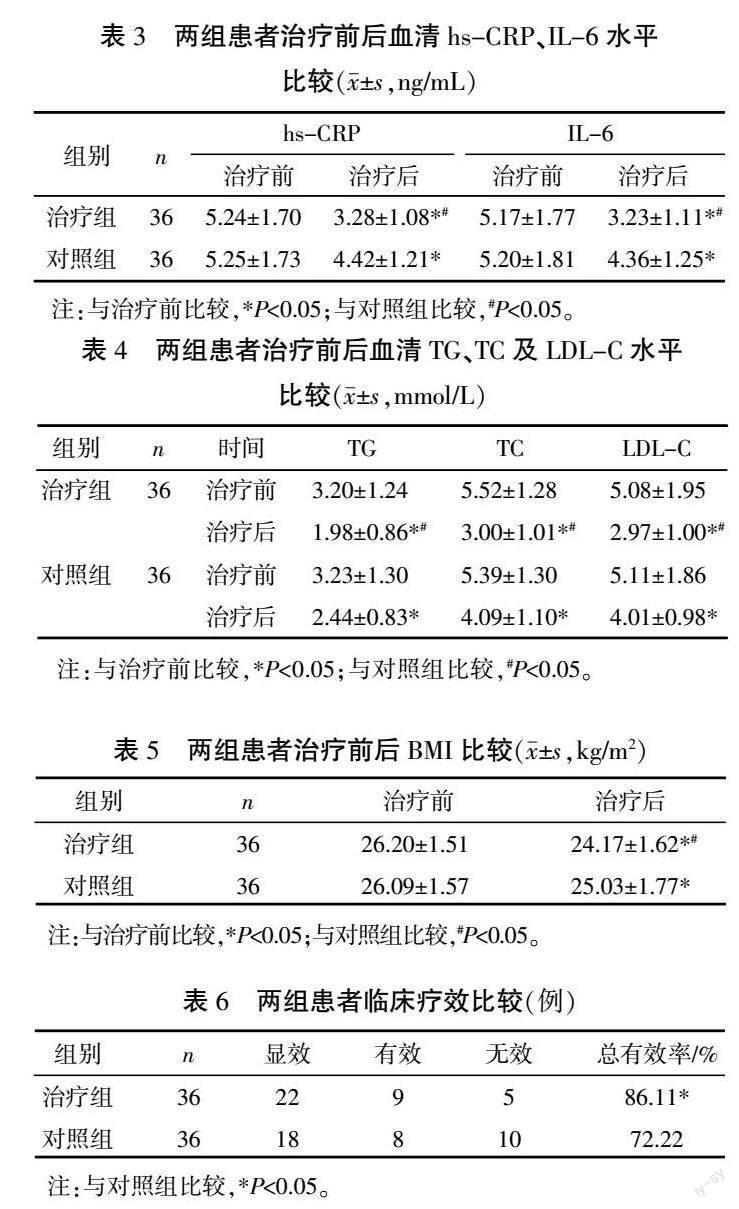
2.3? 兩組患者治療前后炎性因子hs-CRP、IL-6比較
治療前,兩組患者hs-CRP、IL-6差異無統計學意義(P>0.05);治療后,兩組患者hs-CRP、IL-6均較治療前降低(P<0.05),且治療組低于對照組(P<0.05)。詳見表3。
2.4? 兩組患者治療前后脂代謝指標TG、TC及LDL-C比較
治療前,兩組患者TG、TC及LDL-C差異無統計學意義(P>0.05)。治療后,血清TG、TC及LDL-C均較治療前降低(P<0.05),且治療組低于對照組(P<0.05)。詳見表4。
2.5? 兩組患者治療前后BMI比較
治療前,兩組患者BMI差異無統計學意義(P>0.05)。治療后,兩組患者BMI較治療前降低(P<0.05),且治療組低于對照組(P<0.05)。詳見表5。
2.6? 兩組患者臨床療效比較
治療組總有效率為86.11%(31/36),優于對照組的72.22%(26/36),差異有統計學意義(P<0.05)。詳見表6。
2.7? 不良反應
研究方案實施過程中兩組患者均未出現皮疹、瘙癢、疼痛等不良反應,且依從性較好,研究過程中均未出現脫落病例。
3 討論
據國際糖尿病聯合會估計,2021年全球約有5.37億成年人(20~79歲)患有糖尿病;預計到2045年,患者人數將上升至近8億人[7]。隨著糖尿病發病率逐年增加,DPN的發病率也在逐年增加[8-9]。DPN是糖尿病最常見的并發癥[10]。DPN的發病機制尚不確切,考慮可能與高糖高脂狀態以及微血管病變導致的神經元炎性改變、氧化應激、線粒體功能障礙以及細胞凋亡有關[11]。目前,西醫多在降糖基礎上對癥治療,以改善臨床癥狀為主,主要包括營養神經、抗氧化、改善微循環等,如本研究中兩組基礎治療用硫辛酸注射液。隨著中醫治療的臨床普及,中西醫結合治療該病越來越受到醫者和患者的關注,綜合使用針刺、艾灸、穴位貼敷、中藥湯劑等方法治療該病,臨床療效顯著。
DPN屬中醫學“消渴”“痿病”“痹病”范疇。《素問·痿論》曰:“肉痿者,得之濕地也。有所遠行勞倦,逢大熱而渴,渴則陽氣內伐,內伐則熱舍于腎,腎者水藏也,今水不勝火,則骨枯而髓虛,故足不任身,發為骨痿。故痿者,生于大熱也。”《素問·痹論》有云:“其熱者,陽氣多,陰氣少,病氣勝,陽遭陰,故為痹熱,所謂陽遭陰者,腑臟經絡,先有蓄熱,而復遇風寒濕氣客之,熱為寒郁,氣不得通,久之寒亦化熱,則痹然而悶也。”體型較胖的DPN患者,更符合痿證肉痿的范疇,辨證分型多屬肝胃郁熱證,治療上予以清熱通絡針灸處方,療效顯著。
既往研究發現,電針可明顯改善患者下肢疼痛、感覺異常等臨床癥狀[12-13]。王宇等[14]發現,在下肢沿神經走行方向取穴予以電針治療DPN可以促進腓總神經功能重建,從而減輕臨床癥狀。本研究采用清熱通絡電針聯合硫辛酸治療DPN患者,結果顯示治療組TCSS評分、神經傳導速度、總有效率均大于對照組(P<0.05)。該結果說明清熱通絡電針聯合硫辛酸能夠提高患者脛神經和腓總神經的傳導速度,改善疼痛、麻木等癥狀,可能是由于電針可以修復局部損傷神經,同時促進局部變性、壞死產物吸收。研究發現,電針治療時選用疏密波可抑制或延緩患者運動神經和感覺神經的即刻反應,起到鎮痛作用,同時,這種抑制或延緩作用持續時間長,可明顯改善患者臨床療效[15]。疏密波可以促進代謝產物從局部運出,改善局部微循環,消除炎性水腫,起到修復神經的作用[16],因此,本研究中選用疏密波。
大椎穴是督脈和手足三陽經交會穴,故大椎穴能通調全身陽氣,用瀉法針刺大椎穴可清瀉亢盛的陽氣,行清熱瀉火之功。胰俞又稱胃脘下俞,為治療糖尿病要穴。脾俞具有生化氣血、溫補脾陽的功效。陽陵泉為筋會,針刺其可活絡舒筋。血海具有運行氣血、化血為氣的作用,針刺該穴可舒筋活血。足三里是胃經合穴,針刺其可和胃通絡。三陰交具有健脾、理血、平肝陽的作用,針刺其有活血通絡之功。合谷具有疏風解表清熱之效。曲池為大腸經合穴,針刺可瀉脾土之熱,燥大腸之濕熱。行間是足厥陰肝經滎穴,乃肝經子穴,根據“實者瀉其子”及“榮主身熱”的法則,瀉之有清泄肝火之功。故諸穴合用,具有清肝和胃、清熱通絡之功。
IL-6對于炎癥具有雙向調節作用,可以誘發炎癥加重,也有抗炎的作用[17]。當IL-6的血清濃度長期高于2 pg/mL時,IL-6表現為炎癥效應,可能促進糖尿病神經病變的進展[18]。hs-CRP是急性時相反應蛋白,在炎癥反應過度表達時血清濃度升高,且不受外界因素干擾,研究發現,血清hs-CRP水平變化可反映周圍神經損傷嚴重程度,其血清濃度越高,提示病情越重[19-20]。本研究中,治療組患者的炎性指標IL-6、hs-CRP治療后較治療前明顯降低,且低于對照組,表明清熱通絡電針聯合硫辛酸可顯著改善DPN患者的細胞因子水平,減輕炎癥損傷,促進神經修復。另一項研究表明,對于DPN患者,降低其TG、TC、LDL-C時,會顯著減緩其疾病進程,明顯改善患者的臨床癥狀[21]。萬芳等[22]研究發現,DPN患者血脂水平普遍較高,TG、TC、LDL-C與DPN發病關系密切,是誘發神經微血管病變的重要因素。本研究發現清熱通絡電針聯合硫辛酸干預后,治療組患者TG、TC、LDL-C、BMI明顯低于對照組。此結果表明清熱通絡電針聯合硫辛酸不僅可以改善DPN患者的臨床癥狀,而且從根本上降低了誘發DPN的炎性指標,從而降低了該病的發病率。
綜上所述,清熱通絡電針聯合硫辛酸能明顯提高DPN患者的神經傳導速度和降低脂代謝相關指標,改善炎性反應和患者預后,其臨床療效高于單獨西藥治療,值得臨床借鑒。
參考文獻
[1] POP-BUSUI R, BOULTON A J M, FELDMAN E L, et al. Diabetic neuropathy: A position statement by the American diabetes association[J]. Diabetes Care, 2017, 40(1): 136-154.
[2] RUMORA A E, KIM B, FELDMAN E L. A role for fatty acids in peripheral neuropathy associated with type 2 diabetes and prediabetes[J]. Antioxidants & Redox Signaling, 2022, 37(7/8/9): 560-577.
[3] 方朝暉, 吳以嶺, 趙進東. 糖尿病周圍神經病變中醫臨床診療指南(2016年版)[J]. 中醫雜志, 2017, 58(7): 625-630.
[4] 中華醫學會糖尿病學分會. 中國2型糖尿病防治指南(2020年版)[J]. 國際內分泌代謝雜志, 2021, 41(5): 482-548.
[5] 陳明月, 蔡慧敏, 陳江云, 等. 密歇根糖尿病神經病變評分和多倫多臨床評分系統在糖尿病周圍神經病變中的診斷價值研究[J]. 中國全科醫學, 2017, 20(4): 427-431.
[6] 鄭筱萸. 中藥新藥臨床研究指導原則: 試行[M]. 北京: 中國醫藥科技出版社, 2002: 85-87.
[7] SUN H, SAEEDI P, KARURANGA S, et al. IDF Diabetes Atlas: Global, regional and country-level diabetes prevalence estimates for 2021 and projections for 2045[J]. Diabetes Research and Clinical Practice, 2022, 183: 109119.
[8] YANG H, SLOAN G, YE Y C, et al. New perspective in diabetic neuropathy: From the periphery to the brain, a call for early detection, and precision medicine[J]. Frontiers in Endocrinology, 2019, 10: 929.
[9] LING E, LEPOW B, ZHOU H, et al. The impact of diabetic foot ulcers and unilateral offloading footwear on gait in people with diabetes[J]. Clinical Biomechanics, 2020, 73: 157-161.
[10] YANG K, WANG Y, LI Y W, et al. Progress in the treatment of diabetic peripheral neuropathy[J]. Biomedecine & Pharmacotherapie, 2022, 148: 112717.
[11] SLOAN G, SELVARAJAH D, TESFAYE S. Pathogenesis, diagnosis and clinical management of diabetic sensorimotor peripheral neuropathy[J]. Nature Reviews Endocrinology, 2021, 17(7): 400-420.
[12] 姜麗芳, 顧一煌.電針背腧穴并膝局部穴位治療膝骨性關節炎臨床觀察[J]. 陜西中醫, 2016, 37(2): 236-238.
[13] 崔? 燕, 蔣永取, 鄒? 滎. 固本通絡電針法聯合八脈交會穴針刺治療氣虛血瘀型糖尿病周圍神經病變的療效及對SOD、MDA和hs-CRP水平影響[J]. 針灸臨床雜志, 2021, 37(1): 22-25.
[14] 王? 宇, 葉? 田, 宋聰琳. 沿神經走行電針取穴治療腓總神經損傷臨床觀察[J]. 新中醫, 2016, 48(5): 132-134.
[15] 羅芳芳, 林木南, 黃冬娥, 等. 電針疏密波、電針斷續波、電針連續波在瘀血阻滯型膝骨關節炎中的應用對比[J]. 中國醫藥導報, 2022, 19(15): 136-139.
[16] 王連芳, 席? 強. 臨床電針治療膝骨關節炎參數選擇現狀及分析[J]. 中醫藥導報, 2019, 25(8): 108-113.
[17] ROTHAUG M, BECKER-PAULY C, ROSE-JOHN S. The role of interleukin-6 signaling in nervous tissue[J]. Biochimica et Biophysica Acta, 2016, 1863(6 Pt A): 1218-1227.
[18] TZENG H P, LAN K C, YANG T H, et al. Benzo[a]pyrene activates interleukin-6 induction and suppresses nitric oxide-induced apoptosis in rat vascular smooth muscle cells[J]. PLoS One, 2017, 12(5): e0178063.
[19] 周? 玉, 肖麗紅, 陳國蘭, 等. 血清胱抑素C、C反應蛋白與糖尿病周圍神經病變的相關性研究[J]. 贛南醫學院學報, 2019, 39(5): 500-502, 506.
[20] 徐祥坤, 孫玉玲. 血清C反應蛋白和同型半胱氨酸及尿酸水平與2型糖尿病周圍神經病變的相關性研究[J]. 中國預防醫學雜志, 2019, 20(10): 980-983.
[21] ZILLIOX L A, RUSSELL J W. Physical activity and dietary interventions in diabetic neuropathy: A systematic review[J].Clinical Autonomic Research, 2019, 29(4): 443-455.
[22] 萬? 芳, 曹玲玲, 孫? 斐. TG、HDL-C、TC與糖尿病周圍神經病變的相關性研究[J]. 中國現代醫生, 2018, 56(35): 37-39.

