糖皮質激素在腫瘤內科臨床應用的評價
戎佩佩
(武漢大學人民醫院藥學部,湖北 武漢 430060)
?
糖皮質激素在腫瘤內科臨床應用的評價
戎佩佩
(武漢大學人民醫院藥學部,湖北 武漢430060)
摘要:目的對武漢大學人民醫院糖皮質激素類藥品在腫瘤內科的的臨床應用情況進行回顧性調查并分析。方法抽取近期200份使用糖皮質激素類藥品的病歷,評價其用藥合理性。結果我院腫瘤內科糖皮質激素的使用基本合理。結論糖皮質激素在我院腫瘤內科的總體應用較合理。
關鍵詞:糖皮質激素;臨床應用;評價分析
糖皮質激素是臨床應用最廣泛的藥物之一,為了規范該類藥物的臨床應用,我國衛生主管部門曾于2011年發布了《糖皮質激素類藥物臨床應用指導原則》。然而該原則僅涉及了糖皮質激素類藥物在少數血液系統腫瘤中的應用規范,對于該類藥物在實體瘤中的應用鮮有闡述。近年來,多項基礎研究證實,糖皮質激素可誘導實體瘤對多種化療藥物和靶向治療藥物的耐藥[1-4],從而降低化療藥物和靶向治療藥物的療效。因此,實體瘤病人合理應用糖皮質激素類藥物顯得尤為重要。為了更全面地了解糖皮質激素在腫瘤內科的臨床使用情況,筆者進行了調查分析,報道如下。
1 資料與方法
1.1資料來源與評價標準采用回顧性調查方法,利用醫院病案質控管理系統隨機抽查我院腫瘤內科共4個病區近期使用過糖皮質激素的病歷資料共200份。涉及的病種主要有乳腺癌、宮頸癌、卵巢癌、前列腺癌、膀胱癌、淋巴瘤、肺癌、膠質瘤、頭頸部腫瘤、鼻咽癌、胃癌、肝癌、結直腸癌、食管癌、胰腺癌等。用藥指征及合理例數見表1。
糖皮質激素在腫瘤內科的應用十分廣泛,而目前尚無針對糖皮質激素在腫瘤內科應用的指南或專家共識發布。本文對糖皮質激素在腫瘤內科應用合理性的評價指標主要參考藥品說明書和美國綜合癌癥網(NationalComprehensiveCancerNetwork,NCCN)發布的指南中對糖皮質激素類藥物的描述,另有部分應用目前尚無指南對之進行描述,其標準給藥方式有待驗證。本文對用藥合理性評價的標準見表2。
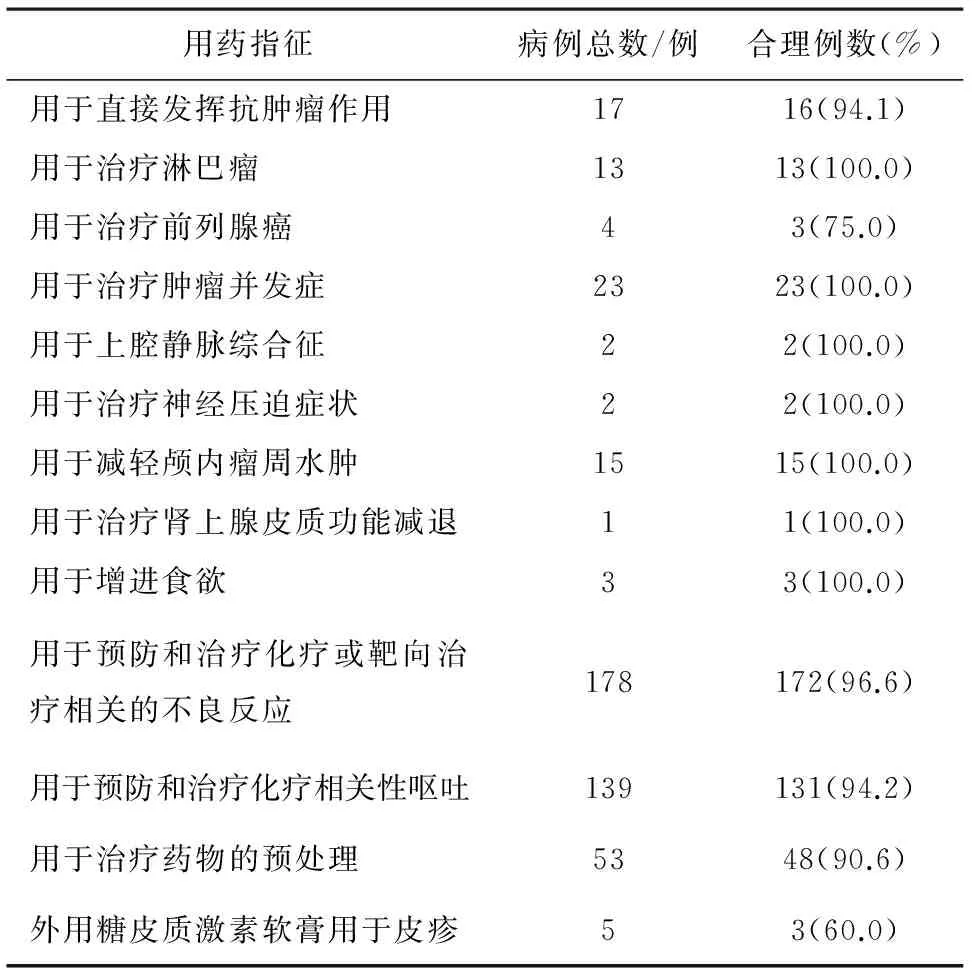
表1 用藥指征及合理例數

表2 用藥合理性評價標準
2 結果與用藥合理性分析
2.1用于治療淋巴瘤糖皮質激素能誘導淋巴細胞凋亡,是淋巴系統惡性腫瘤治療中最重要的藥物之一,常與化療藥物合用,治療急性淋巴細胞白血病、淋巴瘤和多發性骨髓瘤等疾病。本次抽取的200份病歷中,有13例為淋巴瘤患者,包括9例B細胞淋巴瘤(8例彌漫大B細胞淋巴瘤和1例套細胞淋巴瘤)和4例T細胞淋巴瘤(均為外周T細胞淋巴瘤)患者,11例患者的用法均為醋酸潑尼松100mg,口服,d1~5,用法用量均與臨床研究中所設計的方案一致[5]。1例患者將標準治療方案中的潑尼松100mg,口服,d1~5,替換成地塞米松15mg,口服,d1~5。目前已經證實,5mg潑尼松或潑尼松龍與0.75mg地塞米松不僅在抗炎效果上等效,在誘導淋巴細胞凋亡的作用方面也幾乎等效[6],因此該替換可視為合理。另有1例患者既往有胃潰瘍病史,將口服給予潑尼松替換為靜脈給予100mg氫化潑尼松,以期減少消化道不良反應的發生,也視為合理。此外,盡管淋巴瘤聯合化療方案中糖皮質激素的使用均不超過2周,可按規定時間用完即停,無需逐漸減量至停藥,但因淋巴瘤需多個療程化療,仍應注意糖皮質激素長期應用的副作用,最好將給藥時間調整為每日清晨6~8時一次給予全天劑量,使之與正常節律同步而減少其不良反應。
2.2用于治療前列腺癌人體腎上腺分泌約10%循環雄激素,某些去勢抵抗性前列腺癌患者的腫瘤細胞仍然保留雄激素敏感性,糖皮質激素通過抑制腎上腺促皮質激素(ACTH)的分泌,可抑制雄激素、雄甾烯二酮,脫氫異雄甾酮和去氫異雄酮的產生從而誘導臨床反應[7]。此外,糖皮質激素與化療合用時,可減輕化療引起的不良反應[8]。本次抽取的200份病歷中,有4例為前列腺癌患者,均符合去勢抵抗性前列腺癌(castration-resistantprostatecancer,CRPC)診斷標準,并接受以多西他賽為基礎的化療方案。其中3例加用潑尼松5mg,每日2次,口服,持續整個治療周期,并于多西他賽治療前12h,3h及1h時,口服地塞米松8mg。另有1例將潑尼松替換為地塞米松,用法為0.75mg,每日2次,口服。目前已有臨床研究證實,地塞米松用去勢抵抗性前列腺癌療效優于潑尼松,劑量為0.5mg,每日1次[9]。因此,該例患者此處激素用量較大,依據欠充分。
2.3用于上腔靜脈綜合征本次抽取的200份病歷中,有1例廣泛期小細胞肺癌患者和1例肺鱗癌患者因腫塊壓迫上腔靜脈而引起上腔靜脈綜合征(superiorvenacavasyndrome,SVCS),2例患者均在給予放療或化療的同時應用了大劑量地塞米松,用法為靜脈給藥,每日15mg,治療5d后改為口服,每日7.5mg,3d后停藥。糖皮質激素減輕上腔靜脈壓迫癥狀的機制尚不明確,可能與其降低腫瘤組織內毛細血管的通透性,減少腫瘤組織內毛細血管的滲漏,從而減輕水腫有關。該兩例患者激素的用法用量均視為合理。
2.4用于治療神經壓迫癥狀美國綜合癌癥網(NationalComprehensiveCancerNetwork,NCCN)發布的成人癌痛指南中,將糖皮質激素列為晚期癌痛用藥,但臨床實際應用較少,且目前尚無公認的推薦劑量。糖皮質激素的鎮痛機制可能包括:(1)穩定神經元細胞膜,阻斷神經肽合成減少異常放電。(2)減輕受損神經根的炎癥水腫。(3)抑制前列腺素的合成等。本次抽取的200份病歷中,有1例肺鱗癌骨轉移患者試用糖皮質激素緩解背部疼痛癥狀,用法為口服地塞米松7.5mg,每4d減量50%,直至停藥。另有1例肺腺癌骨轉移患者雙下肢肌力、感覺逐漸下降,試用糖皮質激素緩解脊髓壓迫癥狀,用法為靜脈給予地塞米松10mg,連用3d后逐漸減量至停藥,該兩例用法均視為合理。
2.5用于減輕顱內瘤周水腫本次抽取的200份病歷中,有11例腦轉移瘤患者和4例復發性膠質瘤患者接受糖皮質激素治療,用于減輕顱內腫瘤周圍水腫。糖皮質激素通過降低毛細血管通透性、改善血腦屏障功能、穩定腦細胞膜離子通道、抑制腦脊液分泌等減輕間質性腦水腫的發生[10],推薦劑量為:地塞米松15~25mg·d-1或甲潑尼龍80~160mg·d-1,靜脈給藥,每3~4天減量50%,2~3周內停藥。15例患者均依據推薦劑量和療程給藥,視為合理。
2.6用于治療腎上腺皮質功能減退1例小細胞肺癌腎上腺轉移患者化療后出現腎上腺皮質功能減退癥狀,表現為心率加快,血壓降低,靜脈給予氫化可的松100mg經驗性治療后血壓上升,病情穩定后,逐漸減量,使用小劑量激素替代治療,每日5mg,上午8點頓服,該用法視為合理。
2.7用于增進食欲3例患者單用孕激素類藥物改善食欲不佳的效果欠理想,加用小劑量地塞米松后訴食欲較前改善,用法為口服0.75mg,每日一次。糖皮質激素可促進胃酸分泌,因而試用于改善惡病質狀態病人的厭食癥狀。由于該類研究普遍存在樣本量小、缺乏統一標準、缺少對照、觀察指標具有主觀性等問題,因此標準給藥方式有待驗證。該3例患者用法用量視為合理。
2.8用于預防和治療化療相關性嘔吐地塞米松是預防急性嘔吐和預防延遲性嘔吐的基本用藥,其機制目前尚不明確,可能與中樞性抑制前列腺素轉換和減少中樞神經系統5-羥色胺轉換有關,亦或與地塞米松能改變血腦屏障的通透性,降低血液中5-羥色胺作用于腦干后區和孤束核的濃度有關。地塞米松用于預防高、中、低度致吐風險化療方案所致惡心嘔吐的給藥劑量存在差異,見表3。
共139例患者使用地塞米松用于預防和治療化療相關性嘔吐,其中131例患者根據化療方案的致吐風險應用地塞米松。有3例患者未根據風險分層使用地塞米松預防化療相關惡心嘔吐。有5例患者重復使用地塞米松,其中4例患者的治療藥物預處理方案中已包含地塞米松,另有1例患者的化療方案中已包含地塞米松,該5例患者均未調整止吐劑量,用法欠合理。
2.9用于治療藥物的預處理地塞米松是預防化療藥物相關不良反應的基本用藥,其用于不同化療藥物的預處理時,有著不同的用途和給藥劑量,具體見表4。
共53例患者使用地塞米松進行預處理以預防不良反應的發生。其中4例患者同時使用地塞米松用于預防和治療化療相關性嘔吐,出現劑量疊加,應視為不合理。此外,目前我院腫瘤內科使用的單抗類藥物主要有曲妥珠單抗、西妥昔單抗、尼妥珠單抗、利妥昔單抗、貝伐珠單抗等。目前尚無證據支持使用上述藥物前需應用地塞米松等糖皮質激素類藥物進行預處理。1例使用曲妥珠單抗的乳腺癌患者于給藥前應用5mg地塞米松,應視為不合理。
2.10外用糖皮質激素軟膏用于皮疹5例患者接受外用糖皮質激素軟膏用于治療化療或靶向治療引起的皮疹,其中3例用于培美曲塞和吉西他濱引起的皮疹,另有2例分別用于厄洛替尼和西妥昔單抗治療相關性皮疹,該2例應用均視為不合理。該2例患者均系表皮生長因子酪氨酸激酶抑制劑和抗表皮生長因子受體單克隆抗體類藥物引起的痤瘡樣皮疹,且均在用藥后第2周出現,主要發生在顏面部、前胸、后背。由于該類藥物引起的皮疹與藥物影響了表皮細胞生長分化,同時一些炎性因子、凋亡因子和黏附因子上調使毛囊阻塞和損傷而增加細菌過度生長有關[11]。因此,單用糖皮質激素類藥物并不適用于該類伴有膿皰的皮疹的治療,應聯合使用紅霉素軟膏等外用抗菌藥物。

表3 地塞米松用于預防高、中、低度致吐風險化療方案所致惡心嘔吐的劑量及給藥方案

表4 地塞米松用于預處理的劑量及給藥方案
3 小結
糖皮質激素在腫瘤內科的應用非常廣泛,其用藥的合理性值得重視。從本次抽樣的200份病歷來看,糖皮質激素在我院腫瘤內科的應用基本合理,但也暴露出少量問題。臨床藥師應對糖皮質激素的專科應用進行定期分析評價,對其中暴露出的問題進行總結分析,通過開展專題講座等方式對其中欠妥當之處進行點評和分析,防范錯誤的再次發生,以期更好地促進合理用藥。
參考文獻
[1]ChenYX,WangY,FuCC.Dexamethasoneenhancescellresistancetochemotherapybyincreasingadhesiontoextracellularmatrixinhumanovariancancercells[J].EndocrRelatCancer,2010,17(1):39-50.
[2]SumikawaT,ShigeokaY,IgishiT.Dexamethasoneinterfereswithtrastuzumab-inducedcellgrowthinhibitionthroughrestorationofAKTactivityinBT-474breastcancercells[J].IntJOncol,2008,32(3):683-688.
[3]GasslerN,ZhangC,WengerT.Dexamethasone-inducedcisplatinandgemcitabineresistanceinlungcarcinomasamplestreatedexvivo[J].BrJCancer.2005Mar28;92(6):1084-1088.
[4]QianYH,XiaoQ,ChenH.Dexamethasoneinhibitscamptothecin-inducedapoptosisinC6-gliomaviaactivationofStat5/Bcl-xLpathway[J].BiochimBiophysActa,2009,1793(5):764-771.
[5]FisherRI,GaynorER,DahlbergS.Comparisonofastandardregimen(CHOP)withthreeintensivechemotherapyregimensforadvancednon-Hodgkin'slymphoma[J].NEnglJMed,1993,328(14):1002-1006.
[6]InabaH,PuiCH.Glucocorticoiduseinacutelymphoblasticleukaemia[J].LancetOncol,2010,11(11):1096-1106.
[7]那彥群.中國泌尿外科疾病診斷治療指南[M].北京:人民衛生出版社,2014:81.
[8]TannockIF,deWitR,BerryWR.Docetaxelplusprednisoneormitoxantroneplusprednisoneforadvancedprostatecancer[J].NEnglJMed.2004Oct7;351(15):1502-1512.
[9]HolderSL,DrabickJ,ZhuJ.Dexamethasonemaybethemostefficaciouscorticosteroidforuseasmonotherapyincastration-resistantprostatecancer[J].CancerBiolTher.2015,16(2):207-209.
[10] 中華醫學會神經外科學分會.顱內腫瘤周圍水腫藥物治療專家共識 [J].中華醫學雜志,2010,90(1):5-9.
[11]Perez-SolerR,VanCutsemE.ClinicalresearchofEGFRinhibitorsandrelateddermatologictoxicities[J].Oncology(WillistonPark),2007,21(11Suppl5):10-16.
(收稿日期:2016-03-12,修回日期:2016-04-23)
valuationandanalysisofglucocorticoiddrugsatDepartmentofOncology
RONGPeipei
(Department of Pharmacy,Renmin Hospital of Wuhan University,Wuhan430060,China)
Abstract:ObjectiveToevaluate and analyze the clinical application of glucocorticoid drugs at the Department of Oncology in Renmin Hospital of Wuhan University.MethodsWe evaluated the rationality of medication with a random sample of 200 recent cases.ResultsThe usage of glucocorticoid in the Department of Oncology is rational.ConclusionThe application is reasonable on the whole.
Key words:glucocorticoid drug;clinical application;evaluation and analysis

