基于核心素養的“提質減負”課堂案例研究
摘 要:課堂是“提質減負”的主戰場,筆者從實際課堂教學出發,基于學科核心素養,創設真實問題情境,增補課堂實驗,調整教學內容結構等方面激發學生興趣,培養學生的創新精神和實踐能力,提升學生化學學科核心素養,真正實現“提質減負”。
關鍵詞:學科核心素養;提質減負;課堂教學
“減負”,并不是簡單地讓學生減少學習時間、降低學習難度,而是“提質減負”。課堂作為“提質減負”的主戰場,就應該基于學科核心素養,創設真實問題情境,增補課堂實驗,調整教學內容結構,激發學生學習化學的興趣,培養學生的創新精神和實踐能力,提升學生化學學科核心素養,真正減輕學生學業負擔,提升學校教育教學質量。
一、 領悟學科核心素養內涵,倡導真實問題情境創設
新版新課標中有這樣的描述:基于學科本質凝練學科核心素養,明確學生學習該學科課程后應達成的正確價值觀念、必備品格和關鍵能力,對知識與技能、過程與方法、情感態度與價值觀三維目標進行了整合,形成了化學學科核心素養。新課標把創設真實情境、激發興趣、改變學生的學習方式作為重點,提供了“情境素材建議”,鼓勵廣大教師基于真實情境組織教學。
學生的課堂參與度是情境化學習的外在表現。學生在教師的組織下,通過對情境素材的分析,提出問題,展開有序研究,或實驗設計和操作、或學生交互討論、或教師釋疑解惑,共同總結,形成模型認知。這一系列的學習過程無不融入了學生的參與意識,這種情境化的化學教學是提高學生課堂參與度的有效途徑,對促進學生形成正確的價值觀念、必備品格和關鍵能力具有重要意義。
案例1:食鹽加碘劑成分探究的情境創設。
【情境1】(課前布置)日常生活中每天都會攝入一定量的加碘鹽,同學們知道食鹽加碘劑的成分嗎?
化學離不開生活,利用生活中常見食鹽加碘成分的了解,對于學生來說是容易完成的任務。這種生活真實情境再現的創設讓學生感到學科內容的親切而且富有興趣。
【情境2】已知:KI作為加碘劑的食鹽在保存過程中,由于空氣中氧氣的作用,容易引起碘的損失。請用化學方程式解釋。
學生很快寫出反應:O2+4KI+2H2O2I2+4KOH,并解釋KI易被氧氣氧化,I2易升華,容易引起碘的損失。但也有學生提出:碘在堿性條件下易發生歧化反應,上述反應產物I2和KOH不能共存。我當即對該學生的質疑進行了肯定,并且適時給出了鹵素單質發生歧化反應的溶液pH,I2需要在pH>8時歧化生成IO-3和I-。這一情境的創設,看是增加了學生的負擔,實則是更有效地促使學生認知化學:物質世界是運動和變化的(尤其是學生的質疑),化學反應需要一定的條件,并遵循一定的規律;化學反應是有限度的,可以調控;能全方位多角度、變化著分析化學反應,運用化學反應原理解決實際問題。培養了學生的變化觀念與平衡思想,是課堂增效的具體表現。
【情境3】為了提高加碘鹽(添加KI)的穩定性,可加穩定劑減少碘的損失。
下列物質中有可能作為穩定劑的是()。
A. Na2S2O3 B. AlCl3 C. Na2CO3 D. NaNO2
KI被空氣氧化成單質碘,易升華造成流失,硫代硫酸鈉具有還原性,可將I2還原為I-,A項可選;B項中的鋁鹽對人體有害;D項的亞硝酸鈉屬于強致癌物;根據前面分析,預防碘元素流失,應在堿性條件下,將其轉化為碘化鉀和碘酸鉀,所以選擇AC。
通過本情境的分析,促使學生具備嚴謹求實的科學態度,具備探索未知、崇尚真理的意識,能對與化學有關的社會熱點問題做出正確的價值判斷,滲透了學科人文知識教育、愛心責任教育,體現了科學精神與社會責任,增加了學生學習的內驅力,從心理層面減輕了學生的學業負擔。
【情境4】市面上大部分包裝帶著碘字的鹽都屬于加碘鹽。請寫出檢驗加碘鹽是否含有碘的反應的化學方程式(實驗物品為KIO3和家中常見物品)。
要想檢驗加碘鹽中的碘元素,可用KIO3等氧化劑先將KI氧化成I2,然后用土豆等富含淀粉的物質來檢驗。書寫此反應的化學方程式必備知識:碘酸鉀中碘元素的化合價為+5價,KI中碘元素的化合價為-1價,+5價的碘發生還原反應,從+5價降低到0價,-1價的碘必發生氧化反應,從-1價升高到0價,故有:I5++5e-→I,I--e-→I。乘適當系數使電子得失相等后,兩式相加得:I5++5I-→3I2,
將各物質寫成主要存在形態,得:IO-3+5I-3I2+3O2-。反應物轉化為生成物后將會游離出3O2—(非氧化還原組分,不能單獨在水溶液中存在)應結合成3H2O,尚需添加6H+,故有:IO-3+5I-+6CH3COOH3I2+6CH3COO-。檢查兩邊的電荷可見方程式已經配平,若需改寫成化學方程式,先添加反應物的搭配離子,然后使它們在生成物中搭配起來,即得:KIO3+5KI+6CH3COOH3I2+6CH3COOK。故該檢驗過程還需要用到食醋(家庭常備),提供氫離子。
該情境的創設,旨在強化未知型方程式的書寫,通過用半反應式配平書寫氧化還原反應方程式熟悉半反應,將相關知識進行整合,使學生在學習過程中,構建良好的知識體系,為后續的電化學學習奠定基礎。學生能從元素和原子、分子水平認識物質的組成和變化,能從宏觀和微觀相結合的視角分析解決實際問題,能通過分析推理建立模型,并能運用模型熟練書寫陌生方程式,提高學習效率,減輕學業負擔。
二、 利用學科特點落實核心素養目標
實驗教學是化學學科的特點,高中化學課程標準的編寫非常重視實驗探究,特別是通過化學實驗對學生創新能力的培養。為此,對于實驗教學內容,教師應該給學生留下足夠的思考空間,并通過教學設計讓化學實驗在全面提高學生的科學素養方面起到積極作用。在化學教學中,尤其是化學復習中,大膽引入探究性實驗,在學生學習與實驗過程中進行科學探究與創新精神的培養。
案例2:自發性氧化還原反應設計成原電池(以KMnO4和H2O2的反應為例)
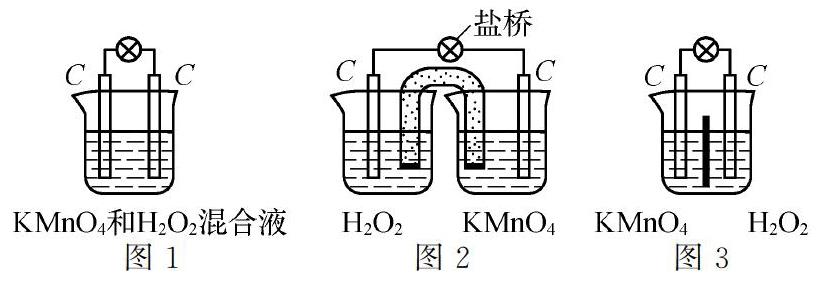
高三一輪氧化還原專題復習練習講評中,涉及KMnO4和H2O2反應的電子轉移問題,我要求學生將該反應的化學方程式拆分成氧化反應和還原反應兩個半反應,并提問“雙氧水中O2-2失電子給Mn7+,如何利用好轉移的電子”,學生能夠馬上聯想到原電池原理,回答“可以設計成化學電源”。我借此機會要求學生以小組為單位設計一款有關KMnO4和H2O2反應的電池裝置。學生饒有興趣的討論并設計了如圖1裝置。
將圖1裝置投影,我鼓勵設計這套裝置的小組利用事先準備的器材和藥品,現場實驗,發現靈敏電流計指針沒有發生偏轉,溶液中產生大量氣泡,溶液顏色變淺。說明KMnO4和H2O2已經發生反應,但為什么沒有電流產生呢?怎樣才能產生電流呢?帶著問題,我引導學生在此套裝置的基礎上進行改進。很快有小組提出了一種想法:KMnO4和H2O2的反應是離子和分子之間的反應,將這兩種溶液混合,離子間接觸非常充分,反應速率極快,電子基本上在H2O2和MnO-4之間傳遞,所以電流表指針不發生偏轉。如果能將兩種溶液分隔開來,就可以形成原電池裝置,聯想到丹尼爾電池,設計了如圖2裝置。另有小組則給出了如圖3裝置,為了鼓勵他們,我讓提出這兩種創意的小組派代表上來演示(因為沒有交換膜,圖3裝置無法實驗),經過幾位學生的合作,大家發現電流計指針發生明顯偏轉,此時掌聲一片,這幾位學生也興奮地歡呼“真的可以的”。
學生在實驗中觀察到的原始材料、實驗數據、實驗事實等都是高中化學課堂教學中體現核心素養的“證據推理與模型認知”。同時在一定程度上為學生提供更多的“發現問題”的機會,可以促進學生創造性思維的發展。學生會主動考慮實驗的各種相關因素如環境的影響、藥品的用量,交換膜的使用,會從宏觀和微觀相結合的視角分析解決實際問題,體現學科知識與培養學生科學態度和社會責任等核心素養的內在關系。
高三復習往往以考代練,以練代講,容易忽視教學內容的結構化設計,我們的課堂應該倡導真實情境的創設,開展以實驗為主的多種探究活動,尤其是在練習講評課中適當增添實驗探究活動,以激發學生學習化學的興趣,促進學生學習方式的轉變,培養他們的創新精神和實踐能力,基于核心素養為本的課堂教學才能真正實現“提質減負”之功效。
總之,提質減負是時代賦予每一個教育工作者的一份厚重的責任。路雖遠,行則必至;事雖難,做則能成。
參考文獻:
[1]中華人民共和國教育部.普通高中化學課程標準(2017年版)[S].北京:人民教育出版社,2018.
[2]北師大等.無機化學第四版(上冊)[M].北京:高等教育出版社,2002:353.
作者簡介:
金立新,浙江省金華市,浙江省金華市外國語學校。

