西羅莫司預防移植物抗宿主病療效的Meta分析
郭璐 沈瑋蕓 周恒

[摘要] 目的 系統性的評價含有西羅莫司預防方案對于移植物抗宿主病的臨床療效。 方法 計算機檢索Pubmed、Embase、Cochrane圖書館、萬方、知網數據庫,納入以西羅莫司作為移植物抗宿主病治療手段隨機對照試驗(RCT),按納入與排除標準選擇試驗,提取資料和質量評價后,運用RvMan5.3軟件對納入的分類變量資料以相對危險度(risk ratio,RR)為統計量,無論異質性的大小都采用隨機效應模型。 結果 納入五項研究,共395例患者。含有西羅莫司的治療方案能有效減少患者Ⅱ~Ⅳ急性移植物抗宿主病(acute graft-versus-host disease,aGVHD)的發生率(RR=0.58,95%CI:0.43~0.77,P=0.0002)。慢性移植物抗宿主病(chronic graft versus host disease,cGVHD)、疾病復發(disease relapse)、非復發死亡(no relapse of mortality,NRM)、總體生存率(overall survival,OS)等研究結局上并未有差異。但西羅莫司使用可能會增加血栓性微血管病(thrombotic microangiopathy,TMA)(RR=2.87,95%CI:1.52~5.40,P=0.001)和靜脈阻塞性疾病(veno occlusive disease,VOD)(RR=2.43,95%CI:1.31~4.49,P=0.005)藥物毒性事件的發生。 結論 西羅莫司可作為移植物抗宿主病的預防用藥,能有效的減少Ⅱ~Ⅳ aGVHD的發生,但應密切觀察聯合用藥后增加的藥物毒性事件,對引起毒性的藥物及時停藥。
[關鍵詞] 西羅莫司;移植物抗宿主病;Meta分析;隨機對照試驗
[中圖分類號] R614.2 ? ? ? ? ?[文獻標識碼] B ? ? ? ? ?[文章編號] 1673-9701(2019)24-0097-06
[Abstract] Objective To systematically evaluate the clinical efficacy of sirolimus on prevention regimen for graft versus host disease. Methods The Pubmed, Embase, Cochrane Library, Wanfang, and HowNet databases were searched by computer, and a randomized controlled trial of sirolimus as a treatment for graft versus host disease. The trials were selected according to inclusion and exclusion criteria. After extracting data and the quality evaluation, the RvMan5.3 software was used to measure the categorical variable data by the relative risk(risk ratio RR), and the random effect model was used regardless of the heterogeneity. Results Five studies were included with a total of 395 patients. Treatment with sirolimus was effective in reducing the incidence of acute graft-versus-host disease (GVHD) in patients with Ⅱ-Ⅳ (RR=0.58, 95% CI: 0.43-0.77, P=0.0002). There were no differences in the outcomes of studies such as chronic graft versus host disease cGVHD, disease relapse, no relapse of mortality (NRM), and overall survival OS. However, sirolimus use may increase the occurrence of thrombotic microangiopathy(TMA) (RR=2.87, 95% CI: 1.52-5.40, P=0.001) and Veno occlusive disease VOD (RR=2.43), 95% CI:1.31-4.49, P=0.005) and drug toxicity events. Conclusion Sirolimus can be used as a preventive drug for graft-versus-host disease, which can effectively reduce the occurrence of Ⅱ-ⅣaGVHD. However, the drug toxicity events increased after combined use should be closely observed, and the drugs causing toxicity should be stopped in time.
[Key words] Sirolimus; Graft versus host disease; Meta-analysis; Randomized
同種異體造血干細胞移植(allogeneic hematopoietic stem cell transplantation,allo-HSCT)作為治療造血系統惡性腫瘤的有效手段在臨床上廣泛開展,但是移植后出現的移植物抗宿主病(graft-versus-host disease,GVHD)卻增加了非復發的死亡(NRM)[1],降低GVHD的發生對于提高移植的成功率具有很重要的意義。通常我們將移植后100 d以內發生GVHD的稱為aGVHD,超過100 d以后發生的稱為cGVHD[2-3]。
目前預防GVHD發生的基本藥物主要有三類:鈣調磷酸酶抑制劑(他克莫司tacrolinus TAC或環孢素cyclosporine,CsA)、細胞毒藥物(甲氨蝶呤methotrexate,MTX)和抗代謝藥物(嗎替麥考酚酯mycophenolate mofetil,MMF)。但即使以它們中的一種或幾種作為預防用藥,GVHD的發生率也在40%~60%左右[1],所以新的治療藥物也在不斷進行臨床評估,西羅莫司(sirolimus,SIR)就是其中之一,其最初是作為一種大環內酯類的抗生素用于治療真菌感染[4],但是研究發現其可以抑制T細胞增殖通路上的靶蛋白(mTOR),阻斷白介素2(IL-2)介導的信號轉錄[5],抑制原始CD4 T細胞分化為Th17細胞,促進調節性T細胞(Treg)的增殖[6]。基礎研究也證實其預防GVHD,降低GVHD相關的死亡率方面具有一定的療效[7],臨床多中心的RCT研究也在廣泛開展,針對這些RCT研究,我們進行系統評價來了解SIR對allo-HSCT患者移植后短期和長期預后的有效性及藥物的安全性。
1 材料與方法
1.1 文獻檢索策略
計算機檢索Pubmed、Embase、Cochrane圖書館、萬方、知網數據庫。檢索時間為建庫到2019年3月。中文檢索詞:“西羅莫司/雷帕霉素”,“移植物抗宿主病”。英文檢索詞:“sirolimus/rapamycin/rapamune”,“graft versus host/graft vs host”,“randomized controlled trials”。文獻語種無限定。手工檢索部分會議文件,并在臨床試驗報告論文或綜述的參考文獻中追蹤查閱相關文獻。
1.2 納排標準
納入標準:①RCT研究必須包含西羅莫司組和非西羅莫司組;②研究對象需為惡性血液系統腫瘤患者并且接受了allo-HSCT;③不考慮患者的年齡、性別、移植前放化療的水平、供體的來源。排除標準:非RCT研究、回顧性分析、自身對照研究、會議文獻、重復發表的研究。
1.3 數據提取
2名研究者獨立篩選、提取資料。提取信息:①一般資料,如作者信息、發表的時間、試驗開展的國家、招募時間、分組信息、樣本量、患者平均年齡、平均隨訪時間、SIR給藥劑量、SIR給藥時間;②結局指標,Ⅱ~Ⅳ急性移植物抗宿主病(acute graft-versus-host disease,aGVHD)、慢性移植物抗宿主病(chronic graft versus host disease,cGVHD)、疾病復發(disease relapse)、非復發死亡(no relapse of mortality,NRM)、總體生存率(overall survival,OS)、血栓性微血管病(thrombotic microangiopathy,TMA)、靜脈阻塞性疾病(veno occlusive disease,VOD)。
1.4 質量評價
運用RvMan5.3軟件中Cochrane風險評估工具,以選擇偏倚(隨機序列產生、分配隱藏)、實施偏倚、隨訪偏倚、測量偏倚、報告偏倚、其他偏倚,按照高、低、未知風險,來評價納入5項研究質量高低[8]。
1.5 統計學方法
納入的研究提取的都為二分類變量數據,采用相對危險度(RR)和95%可信區間(CI)作為療效分析的統計量。首先分析納入研究的臨床異質性,然后采用χ2檢驗分析其統計學異質性。以P=0.05為檢驗水準,同時根據I2判斷異質性的大小。若P<0.05,I2≥50% 為高度異質性,說明各試驗結果間存在異質性,采用隨機效應模型,反之,則說明各試驗結果具有同質性,采用固定效應模型[9]。在RvMan5.3軟件中,在不存在異質性的前提下,固定效應模型和隨機效應模型的結果是一致的,所以我們都應用隨機效應模型進行分析,若存在異質性,首先分析異質性的來源,如人種、設計方案、檢測方法等是否相同,可用亞組分析、敏感性分析等[10]。
2 結果
2.1 檢索結果
通過數據庫檢索,共檢索到中英文相關文獻162篇,通過Endnote軟件去重得到146篇,閱讀標題摘要排除138篇,剩余8篇通讀全文,排除1篇非隨機對照試驗,1篇回顧性研究,1篇同一RCT研究重復發表,最終剩下5篇[11-15](圖1)。其中有3篇[12-13,15]研究是以標準治療方案+SIR vs標準治療方案,2篇[11,14]研究則以SIR+TAC vs MTX+TAC。將納入的5篇研究的相關信息進行整理(表1、2)。
2.2 質量評價結果
Cochrane風險評估工具對納入的5篇RCT研究進行評價的結果(見圖2)。在選擇偏倚中,有Cutler[11]和Armand[15]中明確提到了運用計算機產生隨機序列。Pidala[14]則是按照年齡和供體類型來隨機分組,其他兩篇未提及分組方法。5篇研究均未提及分配隱藏的方式、實施偏倚方式。測量偏倚中Culter[11]提到了數據提取使用的盲法。其他幾方面的偏倚5篇研究都是低風險。
2.3 研究結局分析
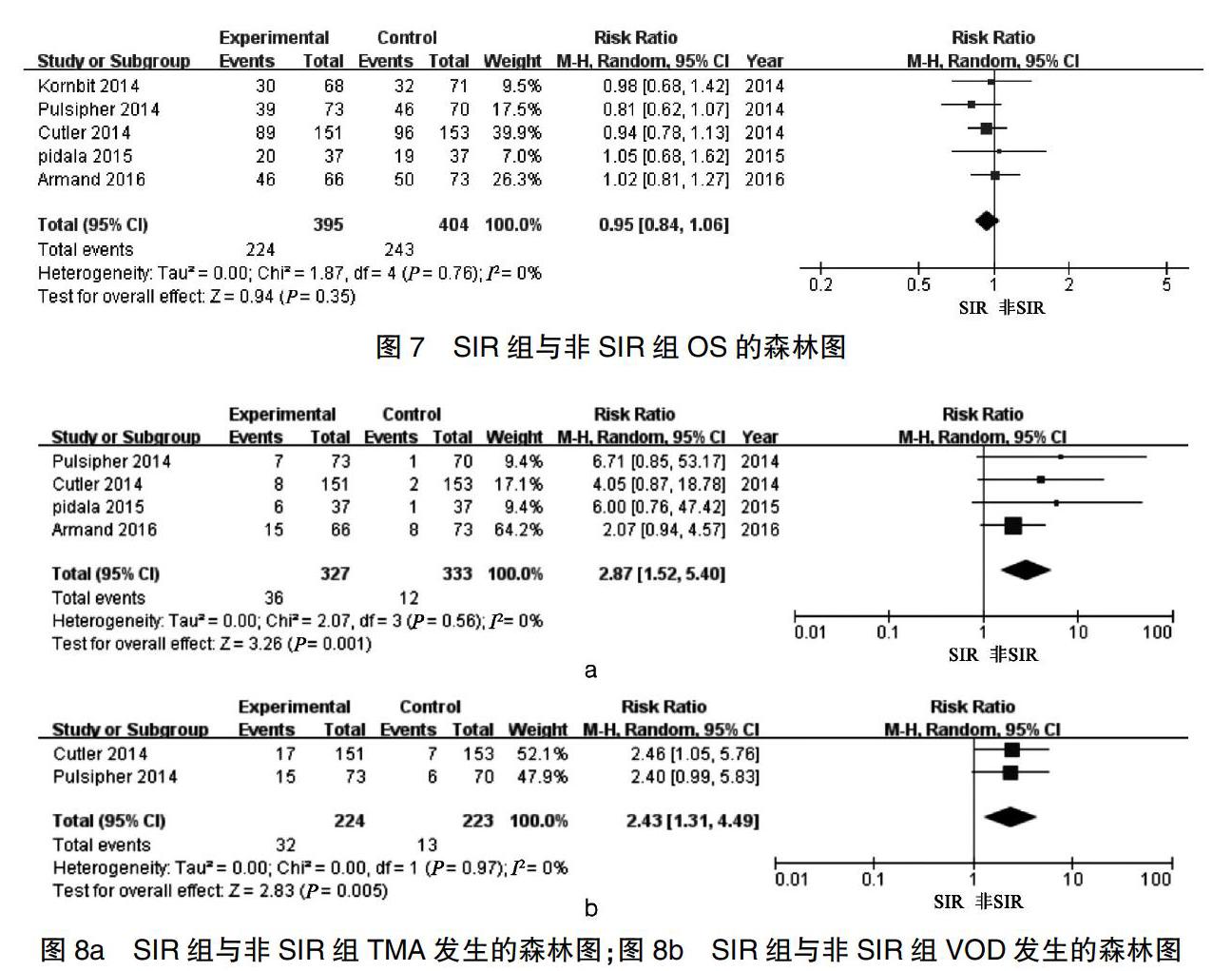
2.3.1 Ⅱ~ⅣaGVHD的發生率 ?5篇RCT都報道了Ⅱ~ⅣaGVHD累計發生情況,統計分析有顯著性異質性(P=0.04,I2=60%),所以我們選用隨機效應模型對數據進行分析,SIR組顯著降低了Ⅱ~ⅣaGVHD的發生率(RR=0.68,95%CI:0.56~0.83,P=0.0001)見圖3a。剔除Kornbit[12]后,異質性為(P=0.24,I2=28%),Ⅱ~Ⅳ aGVHD的發生率(RR=0.58,95%CI:0.43~0.77,P=0.0002)。見圖3b。
2.3.2 cGVHD發生率 ?5篇RCT都報道了cGVHD累計發生率,統計分析無顯著異質性(P=0.19,I2=34%),異質性不明顯時,固定效應模型和隨機效應模型結果一致,選用隨機效應模型,總體來說SIR的使用并未對cGVHD的發生有所改變(RR=1.00,95%CI:0.84~1.19,P=0.98)。見圖4。
2.3.3 Disease relapse ?骨髓移植的目的是為了重建患者的免疫系統來殺死惡性腫瘤細胞,但是移植后大量免疫抑制劑的使用必然會影響移植物抗腫瘤效應(graft versus leukemia,GVL),造成初始疾病的復發。5篇研究都報道了疾病復發的結果,統計分析無顯著性異質性(P=0.42,I2=0%),異質性不明顯,固定效應模型和隨機效應模型結果一致,選用隨機效應模型,兩組之間未見明顯的差異(RR=0.97,95%CI:0.79~1.20,P=0.80)。見圖5。
2.3.4 NRM ?5篇RCT都報道了NRM的結果,統計分析無顯著性異質性(P=0.33,I2=14%),異質性不明顯時,固定效應模型和隨機效應模型結果一致,選用隨機效應模型,SIR并未減少NRM的發生率(RR=1.26, 95%CI:0.89~1.78,P=0.19)。見圖6。
2.3.5 OS ?5篇RCT都報道了OS的結果,統計分析無顯著性異質性(P=0.76,I2=0%),異質性不明顯,固定效應模型和隨機效應模型結果一致,選用隨機效應模型,SIR并不能提高患者2年的總體生存率(RR=0.95, 95%CI:0.84~1.06,P=0.35)。見圖7。
2.3.6 藥物毒性TMA和VOD ?5篇[11-15]RCT報道了在移植后藥物預防GVHD的發生過程中,有藥物使用后引起的毒性反應,其中Cutler[11]和Pulsipher[13]同時報道了TMA和VOD的發生,對TMA的數據進行統計分析無顯著性異質性(P=0.56,I2=0%),異質性不明顯,固定效應模型和隨機效應模型結果一致,選用隨機效應模型,結果顯示含有SIR的治療方案會增加TMA的發生(RR=2.87,95%CI:1.52~5.40,P=0.001)。見圖8a。VOD分類變量數據無顯著的異質性(P=0.97,I2=0%),異質性不明顯,選用隨機效應模型,結果顯示含有SIR的治療方案會增加VOD的發生(RR=2.43, 95%CI:1.31~4.49,P=0.005)。見圖8b。
3 討論
GVHD的發生通常需要具備三個條件:供體和宿主之間的組織相容性抗原存在差異;宿主的免疫功能被有效抑制;供體中具有免疫活性的T淋巴細胞大量增殖攻擊宿主靶器官,造成宿主靶器官的損傷,致使移植的失敗[16]。所以增加配對之間的抗原相容性,親緣性移植,減少移植中T細胞的輸入都是我們解決GVHD發生的辦法,但最終還是要配合使用藥物來提高生存率。
這篇Meta分析系統性評價了SIR作為預防用藥對GVHD結局的影響。在標準治療方案+SIR vs標準治療方案與TAC+SIR vs TAC+MTX治療方案合并中,7個研究結局中,異質性分析發現,只有Ⅱ~Ⅳ aGVHD作為主要的研究結局存在中度異質性(P=0.04,I2=60%),通過重新閱讀5篇納入的文獻,我們分析認為Kornbit B等[12]開展的隨機對照試驗其標準治療方案為TAC+MMF,與其他四篇的標準治療方案(TAC+MTX)有所不同,并且其在aGVHD較易發生的100 d內就已停藥,其他四項研究給藥周期都≥100 d。所以在剔除Kornbit B等[12]研究之后,異質性明顯下降(P=0.24,I2=28%)。見圖3b,并且含有SIR治療方案仍然有效降低了Ⅱ~Ⅳ aGVHD的發生。
除了降低Ⅱ~Ⅳ aGVHD的發生率,在降低cGVHD的發生率上,SIR組與非SIR組之間沒有顯著的差異,這說明含有西羅莫司的治療方案并不能預防全部GVHD的發生,而cGVHD的發生與GVL效應、腫瘤復發低發生率密切相關[17]。一些研究認為,長期的免疫抑制劑的使用在GVHD的預防中發揮了很好的效果,但是過度的免疫抑制會使GVL作用下降,導致腫瘤的復發[18],在這篇Meta分析中我們發現SIR使用在減少Ⅱ~ⅣaGVHD發生的同時,并未增加疾病的復發,這可能是因為SIR激活具有抗淋巴細胞白血病的作用[15]。移植后不僅有腫瘤復發導致的治療失敗,包含GVHD在內的器官損傷,抵抗力下降后各種細菌、病毒、真菌的感染也是導致患者死亡的重要原因[19],對于NRM的分析,兩組之間沒有差異,這說明含有SIR的方案在降低了aGVHD的發生同時,可能會增加機會感染,如pidala J等[14]報道了呼吸道合胞病毒引起肺炎和敗血癥的發生,kornbit B等[12]則報道了巨細胞感染的增加。雖然在Disease relapse、Ⅱ~Ⅳ aGVHD這兩個研究結局方面含有SIR的治療方案與非SIR組相比都具有很好的優勢,但是在終點事件OS方面,meta分析結果并未提示含有SIR的方案提高患者的生存率。
TMA和VOD作為移植后相關的栓塞性疾病其發生率可從0.5%~63.6%不等,雖然目前它們的病理學發生機制不明,但相關研究指出這些栓塞疾病的發生與不同的預處理方案、aGVHD的發生、細菌或真菌感染、HLA不匹配、TAC或SIR的使用最終導致內皮的損傷,血栓形成和微循環纖維蛋白沉積密切相關[20-21]。雖然納入的5篇研究并未全部報道藥物的毒性事件的發生,但Meta分析結果提示,含有SIR的方案會增加栓塞疾病的發生風險,但值得注意的是TMA的發生并不一定是SIR引起的,pidala J等[14]的研究中TMA發生卻與TAC有關,這說明藥物毒性的產生也有可能是SIR和TAC共同作用的結果,所以在預防疾病過程中當有栓塞事件應區分引起毒性反應的藥物及時停藥處理。
綜上所述,納入西羅莫司的RCT研究還是太少,隨機對照試驗有些步驟并未完全按照盲法,所以對結果的發表會有一些人為因素的影響,所以還需要更多的RCT試驗來進一步驗證SIR的療效。
[參考文獻]
[1] Choi SW,Reddy P.Current and emerging strategies for the prevention of ?graft-versus-host disease[J].Nat Rev Clin Oncol,2014,11(9):536-547.
[2] Schaffer JV.The changing face of graft-versus-host disease[J].Semin Cutan Med Surg,2006,25(4):190-200.
[3] Reddy P.Pathophysiology of acute graft-versus-host disease[J].Hematol Oncol,2003,21(4):149-161 .
[4] Vezina C,Kudelski A,Sehgal SN.Rapamycin(AY-22,989),a new antifungal antibiotic. I. Taxonomy of the producing streptomycete and isolation of the active principle[J].J Antibiot,1975,28(10):721-726.
[5] Terada N,Lucas JJ,Szepesi A,et al.Rapamycin blocks cell cycle progression of activated T cells prior to events characteristic of the middle to late G1 phase of the cycle[J].J Cell Physiol,1993,154(1):7-15.
[6] Kopf H,dela Rosa GM,Howard OM,et al.Rapamycin inhibits differentiation of Th17 cells and promotes generation of FoxP3+ T regulatory cells[J].Int Immunopharmacol,2007,7(13):18-24.
[7] Blazar BR,Taylor PA,Panoskaltsis-Mortari A.In vivo inhibition of cytokine responsiveness and graft-versus-host disease mortality by rapamycin leads to a clinical-pathological syndrome discrete from that observed with cyclosporin A[J].Blood,1996,87(9):4001-4009.
[8] Higgins JP,Altman DG,Gotzsche PC,et al.The cochrane collaborations tool for assessing risk of bias in randomised trials[J].BMJ,2011,343:d5928.
[9] Higgins JP,Thompson SG.Quantifying heterogeneity in a meta-analysis[J].Stat Med,2002,21:1539-1558.
[10] 賈靜靜,趙勁東,董平栓,等.補充維生素D對心力衰竭患者臨床作用的Meta分析[J].臨床心血管病雜志,2018,34(2):136-141.
[11] Cutler C,Logan B,Nakamura R,et al.Tacrolimus/sirolimus vs tacrolimus/methotrexate as GVHD prophylaxis after matched,related donor allogeneic HCT[J].Blood,2014, 124(8):1372-1377.
[12] Kornblit B,Maloney DG,Storer BE,et al.A randomized phase II trial of tacrolimus,mycoph-enolate mofetil and sirolimus after non-myeloablative unrelated donor transplantation[J].Haemat-Ologica,2014,99(10):1624-1631.
[13] Pulsipher MA,Langholz B,Wall DA,et al.The addition of sirolimus to tacrolimus/metho-trexate GVHD prophylaxis in children with ALL:A phase 3 children's oncology group/pediatric blood and marrow transplant consortium trial[J].Blood,2014,123(13):2017-2025.
[14] Pidala J,Kim J,Alsina M,et al.Prolonged sirolimus administration after allogeneic hema-topoietic cell transplantation is associated with decreased risk for moderate-severe chronic graft-versus-host disease[J].Haematologica,2015,100(7):970-977.

