基于培養學生核心素養的單元整體架構的一輪復習
曹麗敏
摘要:分析了新高考試題及新課程標準在“水溶液中的離子平衡”這部分內容中對培養學生核心素養的要求,從發展學生核心素養的角度分析了在“水溶液中的離子平衡”進行單元整體架構的復習策略并進行了案例分析。
關鍵詞:單元整體架構;高三一輪復習;核心素養
文章編號:1008-0546(2020)06-0021-05 中圖分類號:G632.41 文獻標識碼:B
doi:10.3969/j.issn.1008-0546.2020.06.006
新版《普通高中化學課程標準》的頒布,拉開了基礎教育化學課程改革的序幕,發展學生的學科核心素養是這次改革的根本目標,如何將核心素養在課堂教學中“落地”是改革的重難點,如何開展以培養學生核心素養為目標的高三復習教學是廣大教師面臨的新課題。本文將以《化學反應原理》主題3“水溶液中的離子平衡”為例,探討如何在高三一輪復習中落實和發展學生的核心素養。
一、高考試題對核心素養的要求
“水溶液中的離子平衡”是中學化學的核心內容,一直是高中教學的重難點,也是高考命題中的熱點,主要考查學生能否運用基本理論和方法解決水溶液中發生的反應和生產生活中的實際問題。
分析近幾年的高考試題,高頻考點有:(1)電離平衡的影響因素;(2)平衡常數的簡單計算;(3)水解的程度及其影響因素;(4)利用平衡常數判斷條件改變對離子濃度的影響;(5)鹽類水解的應用等。試題著重考查學生對溶液系統的整體分析和對平衡體系的微觀過程的分析,考查學生對理論知識的應用能力,考查學生是否具備化學學科的基本觀念和核心素養,可以看出,高考試題的考查方向正在從外在現象逐漸進入內在本質。
二、新課程標準對核心素養的要求
新版《普通高中化學課程標準》在化學反應原理主題3水溶液中的離子反應和平衡中提出了指導性教學策略,這些策略都旨在“形成并發展學生的微粒觀、平衡觀和守恒觀”“引導學生形成認識水溶液中離子反應與平衡的基本思路”。策略提出的總體思路是“形成觀念、引導思路、發展素養、重視應用”,即以核心概念建立相關知識之間的內在邏輯關系,將知識進行理解性整合,使其成為一個有意義的整體,重點關注對整個溶液系統的整體分析和離子平衡的微觀分析。
三、從核心素養角度進行“水溶液中的離子平衡”單元整體架構復習的策略
1.從核心素養和學科觀念的角度建立本章復習框架
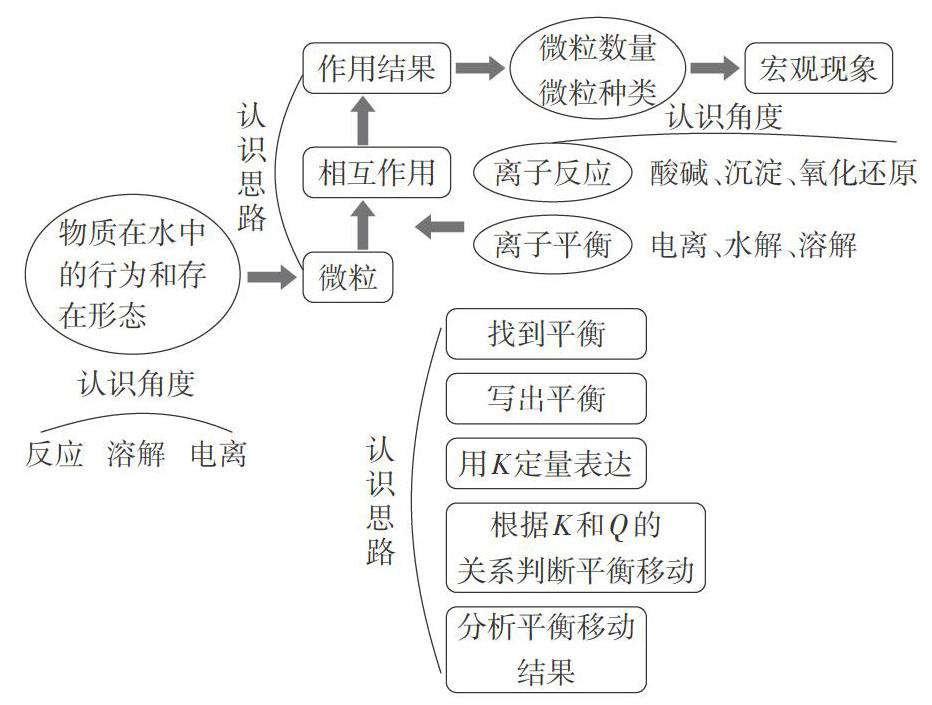
從圖1所示的本章內容框架不難看出:離子平衡是從微粒的角度認識物質在水溶液中的存在形態;從微粒間的溶解、反應、電離等行為理解微粒間的相互作用,從平衡的角度理解微粒間的變化關系,從而樹立學科基本觀念,繼而發展學生的學科核心素養。
基于以上分析,高三復習應做到兩個打通:(1)將全章內容打通,按知識的內在聯系重新整合,形成一個大的框架和體系,讓學生在面對水溶液問題時有整體的思路去分析微粒之間的相互作用;(2)將四大平衡打通,讓學生能將解決化學平衡的一般思路進行遷移,用來分析溶液中的問題。
因此,本章復習可以進行全章節的框架設計,將復習內容整合為以下四個板塊:
板塊一:溶液中離子的產生及離子反應
板塊二:水溶液中的各類平衡
板塊三:各類平衡的平衡常數及應用
板塊四:聯系實際的綜合應用
2.用微粒觀整合復習內容,發展學生“宏微結合”的核心素養
(1)從“微粒觀”的視角看電解質溶液的知識體系
從圖2所示的知識體系可以看出:水溶液中溶質(電解質)的行為與水分子有關,溶質微粒間、溶質微粒與水分子之間的相互作用表現為粒子間的“分離”和粒子間的“結合”。
①水分子間相互作用的結果就是純水的電離
②水分子對溶質微粒作用的結果是電解質的電離
由于水分子的作用,進入水中的電解質與水分子“結合”,導致了溶質內部的微粒克服微粒間的作用力而“分離”,即發生了電離。如果離子與水分子的“結合”不是很強,則“離”和“合”同時存在,是弱電解質。如果離子極易與水分子“結合”,則溶質只“離”不“合”,是強電解質。
③鹽離子對水分子反作用的結果是鹽類水解
④溶質微粒間相互作用的結果導致離子反應的發生
以上用粒子間的“分離”和“結合”看待電解質溶液中粒子的行為的觀點,可以幫助學生認清電解質溶液學習中的一些模糊問題,理解溶液中發生的各類反應的本質。
(2)教學案例分析
[任務1]小組討論以下問題。
①純水中存在哪些微粒?它們之間存在怎樣的相互作用?
②將氨水、HCl、HAc、H2CO3分別溶于水,溶液中存在哪些微粒?有哪些平衡?微粒間有怎樣的相互作用?在此基礎上分析溶液的酸堿性和微粒間的守恒關系。
將分析的結果填入表1。
③將醋酸鈉、氯化銨溶于水后,溶液中存在哪些微粒?存在哪些平衡?微粒間有怎樣的相互作用?在此基礎上分析溶液的酸堿性和微粒間的守恒關系。填人表2。
④將NaHCO3、NaHSO3溶于水后,分析溶液中的各項情況,填入表2。
⑤將氨水一氯化銨等物質的量溶于水后,分析溶液中的各項情況,填入表2。
活動設計意圖:本任務將水的電離平衡、弱電解質的電離平衡、鹽類水解平衡放在一起比較討論,以利于學生從整體上完整把握溶液中的各種平衡并進行綜合分析。任務設計線索由易到難,從單一平衡體系——純水出發→強電解質溶液→一元弱酸、弱堿溶液→多元弱酸溶液→鹽溶液一弱酸(堿)與其鹽的混合溶液,逐步增加任務討論的復雜程度,讓學生在“最近發展區”逐步提高對溶液復雜問題分析的能力。
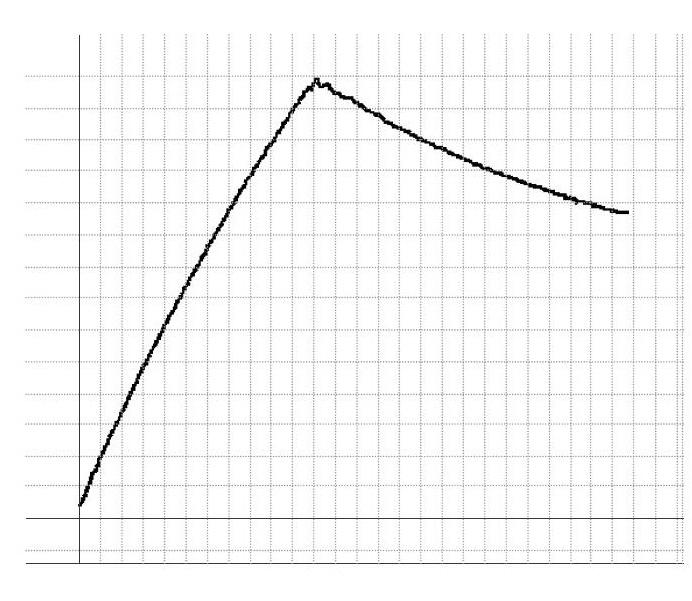
[任務2]常溫下,用0.1mol/L NaOH溶液滴定20.00mL,0.1moL/L CH3COOH溶液,滴定曲線如圖3所示。
結合滴定曲線,請小組討論分析以下問題:
①A、B、C、D四點分別對應溶質是什么?這四個點對應的溶液中存在哪些平衡?
②A點開始滴加NaOH,對CH3COOH的電離平衡有什么影響?如果D點之后繼續滴加NaOH,對CH3COO-的水解平衡有什么影響?
③分析整個滴定過程中水的電離程度有什么樣的變化趨勢?
④若已知A、B、C、D四點對應溶液的pH分別為3、5、7、9,計算這四點時由水電離出的H+或OH-的濃度分別是多大?并按水的電離程度由小到大排序。
⑤以B點溶液為例,寫出3個守恒關系。
⑥若已知A點溶液的pH為a,請計算A點時CH3COOH的電離平衡常數;
若已知D點的pH為9,請計算D點時CH3COO-的水解平衡常數。
活動設計意圖:滴定曲線是反映酸堿反應的動態過程的曲線。利用滴定曲線分析溶液中的反應,可以促進學生對電解質溶液的認識從宏觀、靜止、定性的層次向微觀、運動、變化、定量的水平層次轉化,提高學生對電解質中的微粒行為的理解層次。
3.用平衡常數串聯復習思路,發展學生的變化觀念與平衡思想。
(1)本章中的平衡體系
如圖4所示,化學平衡理論串起了整個平衡體系,而平衡常數是化學平衡理論的核心,是學生深入認識化學平衡的方法和工具。平衡常數能定量計算可逆過程的限度,將各種可逆過程建立聯系,從而實現平衡知識的結構化,同時平衡常數又承載著分析平衡問題的方法功能,這種分析問題的方法在分析各類平衡體系時具有普適性。
當四大平衡通過核心的認識工具——平衡常數建立聯系后,就形成了基于平衡常數的平衡觀及其知識結構,學生可以將平衡常數的方法功能遷移應用到每種平衡問題的分析中,建立關于化學平衡系統的系統性、整體性的認識。
但是教師在實際教學中發現:學生頭腦中并沒有將與平衡相關的知識真正建立聯系,他們的知識是孤立、零散的,他們對于平衡問題的解決往往多用勒夏特列原理,較少利用濃度商規則,缺乏從平衡常數的角度分析平衡問題的意識,定量表征意識比較薄弱。當問題一旦涉及復雜體系或多因素影響的平衡問題時,學生缺乏行之有效的解決問題的思路和方法。因此復習時有必要幫助學生建立對平衡系統的系統整體的認識。
(2)教學案例分析
[任務1]小組學習,并討論以下問題:
①寫出氨水、醋酸鈉、氯化銀的平衡體系及平衡常數表達式,填人表3。
②醋酸和次氯酸的平衡常數能告訴你什么?將平衡常數的意義填人表3。
[任務2]分析在表3的三個平衡體系中:
①加熱、加水如何使這些平衡體系移動?
②加電解質使這些平衡體系怎樣移動?結合每個具體的平衡舉一個電解質的例子分析說明。
③從K和Q如何理解平衡的移動?結合以上平衡移動定量計算加以說明。
[任務3-1]小組討論,利用表4提供的數據,嘗試利用平衡常數分析并解釋下列電解質溶液中發生的反府。
將足量的CO2通人到NaAlO2溶液中:
將少量的CO2通人到NaAlO2溶液中:
將少量的CO2通人到NaCIO溶液中:
將少量的CO2通人到苯酚鈉溶液中:
將NaHCO3溶液與NaAlO2溶液混合:
[任務3-2]小組討論,利用表4提供的數據,嘗試利用平衡常數分析并解釋下列電解質溶液中的離子濃度。
①同濃度的CH3COONa、NaAlO2、NaCIO溶液,堿性依次增強的順序為____,酸根陰離子依次增大的順序為____,結合平衡常數說明分析的思路。
②同pH的CH3COONa、NaAlO2、NaCIO溶液,電解質濃度依次增大的順序為____。
③將含Al3+、Fe3+的溶液與含HCO3-的溶液混合后可以發生雙水解反應。試解釋原因____。
⑥NH4Ac溶液為___性,NH4HSO3溶液為性,NH4HCO3溶液為___性,結合平衡常數說明分析的思路。
活動設計意圖:本任務的設計是讓學生面對有多種平衡共存的復雜體系時,能關注到體系里的各種平衡,基于平衡常數的分析建立動態平衡觀,形成系統的解決問題的思路:(1)依據體系中存在的物質類別,確定體系中存在的平衡類型;(2)書寫電離、水解等平衡的方程式,寫出相關反應的平衡常數的表達式;(3)尋找影響平衡移動的外界因素,將平衡常數K和濃度商O進行比較,將K作為核心工具進行定量分析。
4.用實驗外顯現象形成對概念的整體認知模型,發展學生“證據推理和模型認知”的核心素養
電解質溶液中存在的平衡體系多,平衡之間相互影響復雜,并且內容抽象,導致學生出現許多迷思概念。例如,在復習弱電解質的電離平衡時,學生的迷思概念主要是:(1)對電解質和非電解質的研究對象的范圍概念模糊;(2)對導電性與電解質之間的關系不理解;(3)無法辨別電解質和非電解質的本質區別。針對以上這些迷思概念,教師在復習中應充分利用各種實驗和技術手段,通過巧妙設計實驗讓不可見的實驗現象得到外顯,然后利用實驗證據引導學生進行推理,形成對概念的認知模型并學會遷移應用。
教學案例:
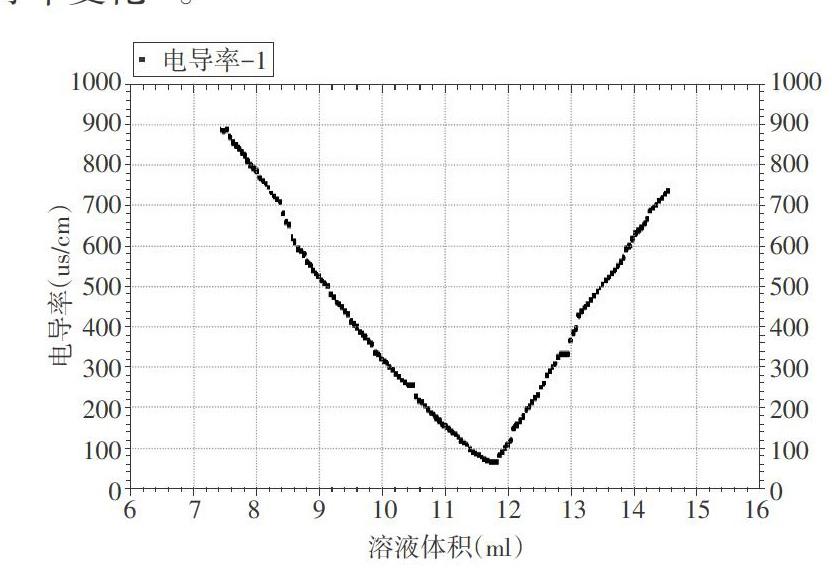
用數字實驗系統分別做兩組實驗。圖5為用等濃度氫氧化鋇滴定0.1mol·L-1硫酸溶液的電導率變化。圖6為用等濃度稀氨水滴定0.2mol·L-1醋酸溶液的電導率變化。
組織學生討論以下問題:
(1)分析兩張圖像中導電率變化的原因。
(2)思考溶液的導電能力與哪些因素有關?
(3)梳理各概念之間的關系,總結認知模型圖(圖7)。

