基于真實問題情境發展學生核心素養的教學
鄧君

摘要:以魔術及“麥片中含鐵粉是真的嗎?”為切入口,設置真實問題情境學習鐵鹽和亞鐵鹽的性質和它們在生產生活中的應用,開展以化學實驗為主的多種探究活動,提高學生解決實際問題的能力,促進核心素養的真正落實。
關鍵詞:核心素養;真實情境;鐵鹽;亞鐵鹽
文章編號:1008-0546(2021)04-0048-06 中圖分類號:G632.41 文獻標識碼:B
doi:10.3969/j.issn.1008-0546.2021.04.013
《普通高中化學課程標準(2017年版)》(簡稱新課標)指出:“重視開展素養為本的教學,倡導真實問題情境的創設,開展以化學實驗為主的多種探究活動[1]。新課標對高中化學教學提出了更高的目標和要求,明確了學生學習該學科課程后應達成的正確價值觀念、必備品格和關鍵能力。為此,教師在設計和開展教學活動時,根據教學內容為學生創設真實陌生的問題情境、設置挑戰性任務,運用必備知識和關鍵能力去解決實際問題,將學科素養的培養落到實處。關于“鐵鹽和亞鐵鹽”的教學設計層出不窮,文獻集中在離子轉化關系的教學[2-3]、高考復習的教學設計[4-5]、創設生活情境進行實驗探究的設計[6-7]。但是在諸多教學設計中,教師常常直接告知靜態結論或者忽視問題情境的復雜性、應用性,未能發展學生應對生活實踐問題情境與學習探索問題情境的綜合素養。
鑒于此,筆者將以“鐵鹽和亞鐵鹽”的教學為例,結合真實問題情境,采用“體驗—探究”教學模式,試圖為構建學生核心素養的教學設計提供參考。
一、教材分析
“鐵鹽和亞鐵鹽”選自人教版《化學1》第三章第二節“幾種重要的金屬化合物”,是在初中介紹的金屬和金屬材料的基礎上,進一步深化和提高,也是為物質的分類、離子反應、氧化還原反應等理論補充感性認識材料,更是對前面理論的應用和升華。本節課是在真實較為復雜的情境下進行Fe2+、Fe3+的檢驗及從氧化還原反應的視角認識Fe2+、Fe3+的性質,可以使學生在探究Fe2+和Fe3+的相互轉化的實驗方案中,對實驗現象進行分析推理,得出合理結論,最終目的讓學生在面臨與化學有關的問題時,能從化學的視角做出更理智、更科學的判斷或選擇。
二、教學目標
1.通過魔術“黃酒變紅酒”和“麥片中含鐵粉是真的嗎?”實驗探究,學會Fe2+和Fe3+的檢驗方法,能根據觀察和實驗獲得的現象,在分析過程中培養學生證據推理、科學探究的素養。
2.通過魔術揭秘及Fe2+和Fe3+相互轉化的實驗探究活動,對知識進行歸納整理,建構Fe2+和Fe3+的相互轉化模型,在過程中培養學生模型認知和變化觀念的素養。
3.通過了解實際生活生產中Fe2+和Fe3+的應用,體會理論知識在實際生活中的具體應用,培養學生科學態度與社會責任的素養。
三、教學策略
“體驗—探究”教學模式操作程序如下:
創設情境(激發體驗階段)→探究釋疑(實踐體驗階段)→實踐應用(體驗生成階段)→評價反思(反思體驗階段)
1.創設情境
魔術和網絡新聞這些真實的問題情境,能夠拉近學生與化學知識的距離,激發學生的好奇心,成為學生思考并解決問題的驅動力。
2.探究釋疑
創設有思維梯度的學習任務,讓學生進行不斷地深度探究,將本質性知識形成清晰的知識框架。
3.實踐應用
緊密聯系生產和生活實際,培養學生尊重事實和證據,具有獨立思考、敢于質疑和批判的創新精神。
4.評價反思
通過自我評價可以對外在的評價標準進行深刻領會,并使之轉化為自我可以接受的評價準則,從而更好地用它來指導課堂教學。
四、教學流程
教學流程如圖1所示。
五、教學過程
1.情境引入——明確課堂目標
【引入】我不是劉謙,但我也可以像劉謙一樣會變魔術,見證奇跡的時刻到了。這是一杯黃酒,另外一個是空酒杯,我將它倒進空酒杯,一杯純正的紅葡萄酒就出現了。我再加入維生素C粉末,紅酒就變成蘋果汁(見圖2)。
【學生】尖叫、鼓掌
【教師】秘密就在課本中,請大家打開課本第61頁,尋找答案。
【展示】硫酸鐵等含有Fe3+的鹽溶液遇到KSCN溶液時變成紅色,我們可以利用這一反應檢驗Fe3+的存在。
【板書】鐵鹽和亞鐵鹽
【教師】魔術的奧妙在哪里?誰能為我這個魔術來揭秘呢?
【學生】黃酒是Fe3+溶液,另一個酒杯裝有很少的KSCN溶液,看起來像空酒杯一樣,一混合紅葡萄酒就出現了。后來為什么變成蘋果汁就不知道了。
【教師】非常好!為什么葡萄酒會變成蘋果汁我們稍后揭秘。我們可以用KSCN溶液檢驗Fe3+,生成的硫氰化鐵是紅色的,注意不是沉淀。用K3[Fe(CN)6]溶液來檢驗Fe2+,產生藍色沉淀。另外,還有沒有其他方法來鑒別Fe2+,Fe3+呢?
【學生甲】觀察溶液顏色,亞鐵鹽是淺綠色的,鐵鹽是棕黃色的。
【學生乙】加入NaOH溶液,Fe(OH)2是白色沉淀迅速變為灰綠色,最終被氧化為紅褐色,而Fe(OH)3是紅褐色沉淀。
【教師】不錯。那我們就開啟實驗之旅吧。
設計意圖:通過魔術表演,激發學生的學習興趣,使樂學、善學這一核心素養在課堂上得以體現。
2.實驗探究——掌握化學原理
【實驗探究】有些商家為了將麥片中鐵含量增加,直接把鐵粉摻入麥片里。麥片中含有鐵粉是真的嗎?對人體是有益還是有害?請大家在20min內完成活動,各小組交流討論,然后匯報成果。
(1)閱讀麥片配料表(見圖3),思考如何提取鐵粉?如何溶解鐵粉?溶液中的鐵元素是Fe2+還是Fe3+?設計實驗檢驗Fe2+,Fe3+。
(2)通過教師引導設計流程圖(見圖4),完成實驗,記錄現象,得出結論。
實驗儀器:攪拌機、燒杯、試管、藥匙、玻璃棒、膠頭滴管、點滴板、密封袋、磁鐵
實驗試劑:麥片、稀硫酸、鐵氰化鉀溶液、硫氰化鉀溶液、氫氧化鈉溶液
實驗步驟:分別取各品牌麥片一包,加水充分溶解,倒入攪拌機攪拌約20s,將液體倒入密封袋中,用強力磁鐵放在密封袋上面,吸出黑色粉末并取出。
【實驗現象】如圖5所示
【板書】檢驗Fe2+,Fe3+
【教師】時間到了,大家非常積極,配合的也很默契,每組請一位同學進行匯報。鐵元素存在的價態有哪些?大家如何提取鐵粉?溶解過程有什么現象?請第1小組的成員分享你們的成果。
【成果匯報l】鐵元素有0,+2,+3價,存在形式為Fe、Fe2+、Fe3+。用磁鐵將鐵粉吸出來,然后選擇稀硫酸將其溶解,四種麥片中均有氣泡生成。
【教師】很好,請在黑板上寫出這個反應的化學方程式。
【學生板書】Fe+H2SO4=FeSO4+H2↑
【教師】如何檢驗所得溶液中的Fe2+和Fe3+?請第2組同學將本組探究情況跟大家交流匯報。
【成果匯報2】結果如表1所示。
【教師】根據實驗現象,為什么觀察法和沉淀法并沒有達到實驗的預期現象?
【學生丙】可能是鐵離子濃度過小,通過肉眼無法辨別顏色。
【學生丁】可能反應后溶液是Fe2+,Fe3+的混合溶液,Fe2+含量多,灰綠色沉淀掩蓋了Fe(OH)3紅褐色沉淀,不能觀察出來。
【教師】鑒別即兩種或兩種以上物質組合,通過實驗予以區分。同學們歸納出來的是鑒別Fe2+,Fe3+的方法。而此時我們得到的是一杯混合溶液,里面可能存在Fe2+可能存在Fe3+,要確定溶液中是否存在二者,這樣的過程稱之為檢驗。觀察法和沉淀法中兩種離子相互干擾無法檢驗出二者。那么大家覺得在這杯溶液中檢驗Fe2+,Fe3+最好選用什么試劑?流程中試劑1,2分別是什么?
【學生戊】試劑1可用鐵氰化鉀K3[Fe(CN)6]溶液來檢驗Fe2+,試劑2可用KSCN溶液檢驗Fe3+。這兩種方法比較靈敏,不相互干擾,用量少且現象明顯。
【教師】請第3組同學對四種不同麥片品牌中的Fe2+、Fe3+的檢驗進行匯報交流。
【成果匯報3】四種麥片的實驗數據(見表2)
【教師】這四種麥片中都含有Fe2+和Fe3+,分析產生Fe3+的原因是什么呢?
【學生】(1)麥片中加入的還原鐵不純,存在少量副產物。
(2)還原鐵有部分被氧化,或者生成Fe2+后被空氣氧化。
【教師】麥片中為何要添加還原鐵?
【學生】補鐵,還原鐵粉進入胃中會轉化為Fe2+,被人體所吸收。
【教師】還有其他作用嗎?提示:鐵露置在空氣中最終會生成什么?形成鐵銹的條件?
【學生】吸收空氣中的氧氣和水。
【教師】因此,還原鐵粉又稱為“雙吸劑”,糕點中常會放一包黑色粉末,用于食品保鮮。一般來說,Fe2+較Fe3+有利于人體吸收。如何將Fe3+轉化為更利于人體吸收的Fe2+呢?
設計意圖:利用生活實驗探究,不僅增進趣味性,更體現學以致用;既區別檢驗與鑒別的概念,又選出檢驗Fe2+,Fe3+的最佳試劑。本主題的設計是讓學生勤于反思,通過問題解決實現學生核心素養的達成。
3.實驗升華——形成知識框架
【教師】我們前面的魔術中,黃酒變紅葡萄酒,大家都明白了暗含的秘密。說明溶液中有Fe3+,我再加入維生素C粉末,紅酒就變成蘋果汁。此時,有沒有發生化學變化?溶液里還有沒有Fe3+呢?如果是化學反應,屬于什么反應類型?
【學生】有發生化學反應。紅酒里已經有硫氰化鉀,加入維生素C粉后,紅色褪去,說明反應后已沒有Fe3+。鐵元素的化合價有發生改變,為氧化還原反應。
【教師】說得很好!從化合價的變化角度看,維生素C片起什么作用?作什么劑?
【學生】加入維生素C,維C把Fe3+轉化為Fe2+,所以維C作還原劑。
【板書】Fe2+和Fe3+的轉化
【學生活動1】設計實驗將Fe3+轉化為Fe2+
試劑:Fe2(SO4)3溶液、維生素C片、銅片,KSCN溶液,K3[Fe(CN)6]溶液。
(1)從氧化還原反應角度分析,Fe3+能不能轉化為更利于人體吸收的Fe2+?
(2)驗證你的猜想。
【教師】請采用不同還原劑做實驗的第4組和第5組同學分別進行匯報交流。
【成果匯報4】取一支潔凈的試管,加入少量的Fea(SO4)3溶液,加入銅片,溶液由黃色變為淺綠色(耗時較長)。再滴入1滴K3 [Fe(CN)6]溶液,出現藍色沉淀(輔助檢驗)。說明鐵離子轉化為亞鐵離子(見圖6)。
【成果匯報5】取一支潔凈的試管,加入少量的Fe2(SO4)3溶液,滴入幾滴KSCN溶液,溶液變為紅色。加少量研磨后的維生素C粉,紅色褪去。再加入1滴K3[Fe(CN)6]溶液,出現藍色沉淀(如圖7)。說明維生素C粉、銅片這樣的還原劑可以將Fe3+還原為Fe2+。
【教師】銅片、維生素C等還原劑能夠將Fe3+轉化為Fe2+,更有利于人體吸收。那要加入什么試劑可以將Fe2+氧化成Fe3+?
【學生】要加入氧化劑,比如高錳酸鉀、氯水、過氧化氫等。
【學生活動2】設計實驗將Fe2+轉化為Fe3+
試劑:FeSO4溶液、新制氯水、雙氧水,KSCN溶液。
【教師】請最后一組同學來分享你們的活動成果。
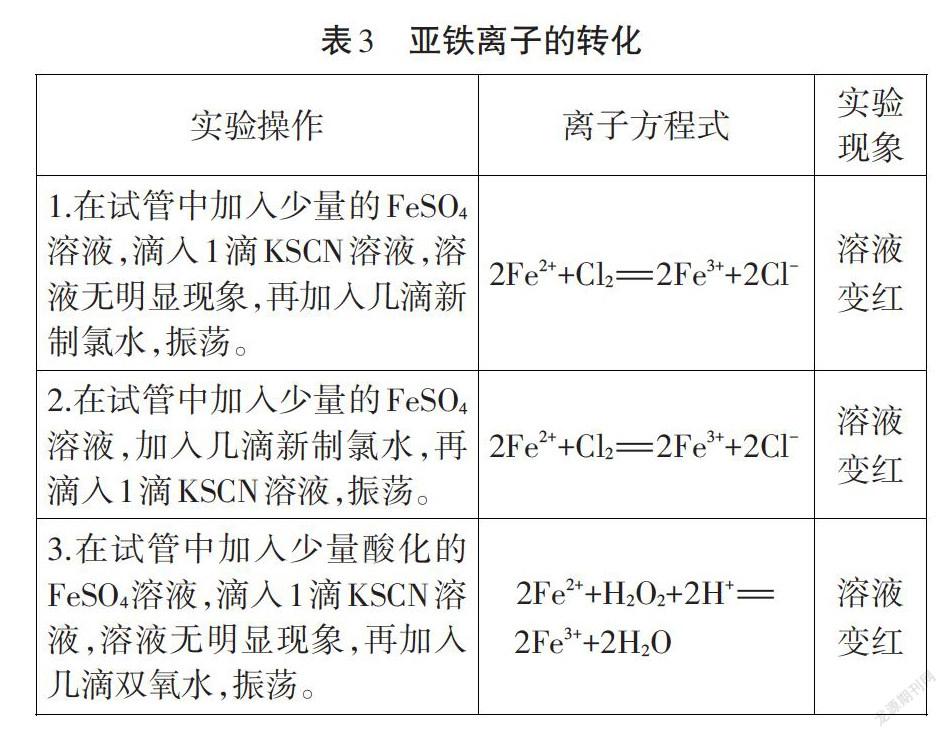
【成果匯報6】如表3所示
【教師】實驗操作1和2哪一種更好?為什么?
【學生己】實驗操作1更好,Fe2+易被氧化,先加KSCN溶液,溶液無明顯現象,可排除原溶液中Fe3+的干擾。
【教師】請按實驗操作3的同學來分享一下實驗現象。
【學生庚】剛開始跟大家一樣,溶液變紅,但是,一段時間后,溶液中有較多氣泡出現,并放熱,隨后有紅褐色沉淀生成。
【教師】不錯,同學觀察現象非常仔細。有同學可以分析一下產生的是什么氣體?產生氣泡的原因是什么?生成的紅褐色沉淀是什么?產生沉淀的原因又是什么呢?
【學生辛】可能雙氧水加多了分解生成氧氣。根據元素守恒和特殊的顏色現象可以判斷出來,生成的紅褐色沉淀應該是Fe(OH)3,原因是什么不清楚。
【教師】初中我們學過二氧化錳可以催化雙氧水分解產生氧氣,Fe3+也可以。感興趣的同學可以自行設計實驗進行驗證。生成紅褐色的原因是該分解反應放熱,促進Fe3+的水解平衡正向移動。鹽類的水解我們稍后會學習。
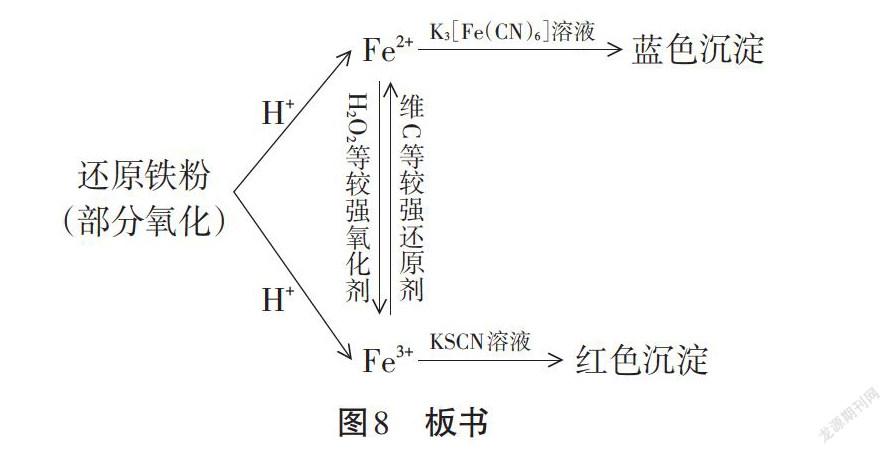
【板書】如圖8所示。
設計意圖:本節課模型構建的升華,掌握學習元素化合物的一般方法,同時拓展離子檢驗方法的思路及氧化還原理論的運用。
4.實驗應用——體驗知識達成
【教師】實驗室如何保存FeSO4溶液?
【學生壬】可以加入少量鐵粉,防止Fe2+被氧化。
【學生癸】在配制溶液時,用的蒸餾水應該要加熱煮沸除去溶解氧。
【學生十一】這種試劑盡量現用現配,因為容易被氧化。
【教師】大家回答的非常棒!請大家觀察這瓶FeSO4溶液的底部。
【學生】黑色粉末為鐵粉,防止溶液被氧化。
【教師】不錯,請同學們寫出該反應的離子方程式。
【學生】Fe+2Fe3+=3Fe2+
【教師】在生活中,兒童缺鐵性貧血醫生會建議服用小兒硫酸亞鐵糖漿,在服用時與什么同服更促進吸收?
【學生】維生素C片或富含維C的食物,維生素C可以將部分被氧化生成Fe3+轉化為Fe2+,促進鐵吸收。
設計意圖:真實情境的引入,拓展學生的視野,身邊處處有化學,升華學生對本節課學習方法的應用。
六、課后反思
1.創設情境,激活課堂教學
創設真實實驗情境,引導學生探究性學習,不僅讓學生體驗到化學學科的獨特魅力,也培養了學生實驗探究的思維。本節課的開始教師借助魔術表演及新聞報道的引入,激發學生的求知欲。通過閱讀麥片配料表,引導學生提取鐵粉,溶解鐵粉,設計實驗檢驗Fe2+,Fe3+。最終找到在一杯Fe2+,Fe3+都可能存在的溶液中檢驗二者的最佳試劑。以生活化的視野引導學生聯系實際生活,從生活中來,到生活中去,運用已有知識或合作探究能力來解決生活實踐中的應用性問題。
2.尊重事實,解決實際問題
化學是一門以實驗為基礎的自然科學,尊重客觀事實,用事實說話。通過“麥片中含鐵粉是真的嗎?”探究實驗,學生知道在麥片中添加鐵粉是真的,而且是有利于身體健康的。此外,既要充分利用學生的已有經驗開展教學,又要對有些經驗,尤其是有疑惑的內容進行實證,可以采用客觀事實、化學實驗等方式進行。在將Fe2+轉化為Fe3+環節時,KSCN溶液滴加的順序不一樣,得到的現象一樣,其實是某種實驗操作不夠嚴謹,沒有排除原溶液中Fe3+的干擾。選用雙氧水做氧化劑時,由于加入雙氧水的量過多,有同學觀察到其他現象。教師也應引導學生分析此產生現象的原因,對實驗現象進行深度挖掘。因此,筆者經常在課堂上有意放慢教學節奏,留有足夠的時間和空間讓學生進行探究,思考、討論,讓學生體會到解決實際問題往往具有層次性、復雜性。
3.構建網絡,體現思維進階
構建化學知識網絡可幫助學生理解化學,提高學習能力,提升科學素養。通過這節課鐵鹽和亞鐵鹽的知識學習,學生對所學知識進行系統的梳理、深化、整合,自主構建了Fe2+與Fe3+轉化關系,思維得到了進一步的提升。所以,教師在教學過程中不僅僅是解決探究任務的本身,同時也要不斷地聯系生活,升華內容,特別是在探究環節結束的時候引導學生進行網絡構建,使知識得以內化,情感得以提升。
參考文獻
[1]中華人民共和國教育部.普通高中化學課程標準(2017年版)[S].北京:人民教育出版社,2018
[2]姚建軍,仲淑嫻.“Fe2+和Fe3+的性質與轉化”教學設計及反思[J].化學教與學,2012(12):58-60
[3]趙仲霞,張澤俊,羅家剛.無機元素化合物知識教學設計研究——以鐵及其化合物的性質為例[J].中學化學教學參考,2017(12):22-24
[4]虞琦,倪娟.基于學科觀念培養的高三一輪復習課堂教學——以“鐵及其化合物”為例[J].中學化學教學參考,2013(8):27-29
[5]耿亞萍.基于生活問題情境的化學核心素養的培養研究——以鐵及其化合物復習為例[J].北學教育(中英文),2019,40(7):38-41
[6]王星喬,包朝龍,騰瑛巧.“補鐵劑的選購與含鐵量的測定”教學設計與實錄[J].化學教學,2013(11):46-48
[7]馬佩強,孟靜.巧用情境線索滲透核心素養創設生機課堂——以“鐵的重要化合物”的教學設計為例[J].化學教與學,2019(9):51-55
*本文系廣州市教育科學規劃“十三五”重點課題“基于學科核心素養的中學課堂教學策略轉型研究”(201811552)、廣東教育學會2018年度教育科研規劃小課題“核心素養理念下的元素化合物知識‘體驗—探究教學模式的研究”(GDXKT16781)的階段性研究成果。

