普羅帕酮與胺碘酮治療室上性心律失常患者心肌損傷情況對比分析
廖品容
【摘要】? 目的? ? 對比分析普羅帕酮(PF)與胺碘酮(AD)治療室上性心律失常(SA)患者心肌損傷情況。方法? ? 選擇2020年6月—2021年5月于萬年縣人民醫(yī)院治療的60例SA患者,按隨機(jī)數(shù)字表法將其分為PF組(30例)與AD組(30例),PF組采用PF治療,AD組采用AD治療。比較2組臨床療效、復(fù)律時(shí)間、復(fù)發(fā)次數(shù)、心肌損傷、炎性因子及不良反應(yīng)發(fā)生情況。結(jié)果? ? AD組治療總有效率高于PF組,AD組復(fù)律時(shí)間短于PF組,復(fù)發(fā)次數(shù)少于PF組,治療后AD組心肌肌鈣蛋白Ⅰ、肌酸激酶同工酶及腦鈉肽(BNP)低于PF組,治療后AD組腫瘤壞死因子-α(TNF-α)及超敏C反應(yīng)蛋白(hs-CRP)低于PF組,有統(tǒng)計(jì)學(xué)差異(P<0.05);2組患者的不良反應(yīng)發(fā)生率比較,無統(tǒng)計(jì)學(xué)差異(P>0.05)。結(jié)論? ? SA患者采用AD治療效果確切,可抑制炎癥反應(yīng),降低炎癥因子水平,減輕心肌損傷,降低復(fù)發(fā)次數(shù),且并未增加不良反應(yīng)。
【關(guān)鍵詞】? 室上性心律失常; 普羅帕酮; 胺碘酮; 心肌損傷; 炎性因子; 不良反應(yīng)
中圖分類號:R541.7? ? ? ? 文獻(xiàn)標(biāo)識碼:A
文章編號:1672-1721(2023)19-0052-03
DOI:10.19435/j.1672-1721.2023.19.017
室上性心律失常(SA)為常見的心血管疾病,可發(fā)生于任何年齡段,突然發(fā)作、突然終止為其發(fā)作特點(diǎn)。SA可由于酒精、運(yùn)動(dòng)及情緒等因素誘發(fā),輕度患者臨床癥狀表現(xiàn)較輕,往往難以察覺;重度患者會出現(xiàn)胸悶、低血壓癥狀,對心血管血液流變學(xué)形態(tài)影響較大,可能會誘發(fā)心肌梗死、心力衰竭等,甚至出現(xiàn)猝死[1]。故給予及時(shí)、有效、安全的治療為臨床研究的重點(diǎn)。目前,臨床針對SA以藥物治療為主,種類較多,但綜合考慮效果及安全性,多數(shù)藥物治療效果一般。普羅帕酮(PF)是一種廣譜高效的抗心律失常藥物,可對β受體進(jìn)行抑制,是治療心律失常的常用藥物[2]。胺碘酮(AD)屬于廣譜抗心律失常藥物,可對鉀離子外流進(jìn)行抑制,提高心室、心房及房室結(jié)的有效不應(yīng)期,減少信號折返激動(dòng),有效穩(wěn)定心率[3]。本研究對比分析PF與AD治療SA患者心肌損傷情況,旨在為臨床治療藥物的選擇提供參考,報(bào)告如下。
1? ? 資料與方法
1.1? ? 一般資料? ? 選擇2020年6月—2021年5月于萬年縣人民醫(yī)院治療的60例SA患者,按隨機(jī)數(shù)字表法將其分為PF組(30例)與AD組(30例)。PF組:男19例,女11例;年齡45~78歲,平均年齡(58.72±3.50)歲;發(fā)作至就診時(shí)間1~10 h,平均(4.71±1.63)h;體質(zhì)量指數(shù)(BMI)18.2~29.4 kg/m2,平均(24.11±1.52)kg/m2。AD組:男16例,女14例;年齡42~78歲,平均年齡(59.07±3.44)歲;發(fā)作至就診時(shí)間1~9 h,平均(4.65±1.68)h;BMI 18.1~29.7 kg/m2,平均(24.20±1.48)kg/m2。2組一般資料無統(tǒng)計(jì)學(xué)差異(P>0.05)。研究獲醫(yī)學(xué)倫理委員會批準(zhǔn)。
1.2? ? 入選標(biāo)準(zhǔn)? ? (1)納入標(biāo)準(zhǔn):①患者簽署知情同意書;②符合SA診斷標(biāo)準(zhǔn)[4];③能夠耐受PF、AD治療;④行為正常,無精神疾病,依從性較高;⑤患者年齡≥18歲。(2)排除標(biāo)準(zhǔn):①合并急慢性炎癥;②合并嚴(yán)重代謝系統(tǒng)疾病;③合并心肌梗死等其他心臟疾病;④合并呼吸系統(tǒng)疾病;⑤碘過敏或甲狀腺功能減退、亢進(jìn)患者;⑥合并惡性腫瘤。
1.3? ? 方法? ? PF組采用普羅帕酮(江蘇神龍藥業(yè)有限公司,國藥準(zhǔn)字H32020352)治療,靜脈注射11.5 mg/kg,若心律轉(zhuǎn)為竇性心律則停止注射,觀察10 min若無反復(fù)停止治療;若未終止,繼續(xù)靜注,但總劑量≤210 mg。AD組采用胺碘酮(江蘇漣水制藥有限公司,國藥準(zhǔn)字H32022397)治療,首先靜脈推注150 mg,靜推時(shí)間>10 min,觀察30 min,若未復(fù)律,以1 mg/min的劑量靜脈滴注。
1.4? ? 評價(jià)指標(biāo)? ? (1)臨床療效:治療后3 d評估療效,心悸、胸悶癥狀消失,心律恢復(fù)為竇性心律為顯效;臨床癥狀改善,心率下降>20%,但仍為室上性心律為有效;臨床癥狀未改善,心率下降≤20%為無效。總有效率=有效率+顯效率。(2)統(tǒng)計(jì)2組復(fù)律時(shí)間,治療后隨訪6個(gè)月,統(tǒng)計(jì)復(fù)發(fā)次數(shù)。(3)心肌損傷:治療前、治療后3 d采集2組靜脈血,采用化學(xué)發(fā)光法測定心肌肌鈣蛋白Ⅰ(cTnI)、肌酸激酶同工酶(CK-MB)、腦鈉肽(BNP)。(4)炎性因子:治療前、治療后3 d采集2組空腹靜脈血,分別采用酶聯(lián)免疫吸附法、散射比濁法測定腫瘤壞死因子-α(TNF-α)、超敏C反應(yīng)蛋白(hs-CRP)。(5)統(tǒng)計(jì)2組不良反應(yīng)(低血壓、嘔吐等)發(fā)生情況。
1.5? ? 統(tǒng)計(jì)學(xué)方法? ? 使用SPSS 22.0統(tǒng)計(jì)學(xué)軟件進(jìn)行數(shù)據(jù)分析,計(jì)量資料以x±s表示,行t檢驗(yàn),計(jì)數(shù)資料以百分比表示,行χ2檢驗(yàn),P<0.05為差異有統(tǒng)計(jì)學(xué)意義。
2? ? 結(jié)果
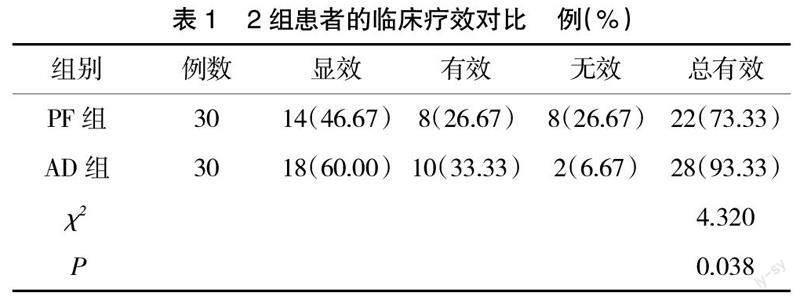
2.1? ? 2組患者的臨床療效比較? ? AD組患者的治療總有效率高于PF組,有統(tǒng)計(jì)學(xué)差異(P<0.05),見表1。
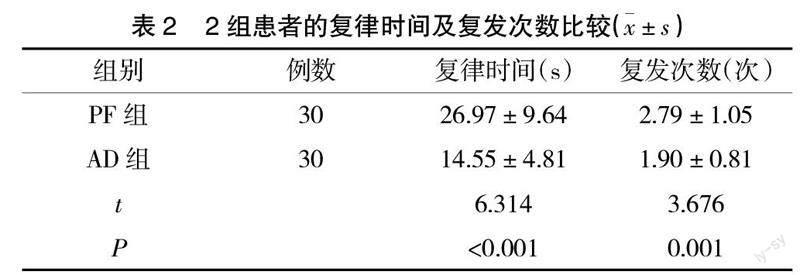
2.2? ? 2組患者的復(fù)律時(shí)間及復(fù)發(fā)次數(shù)比較? ? AD組患者的復(fù)律時(shí)間短于PF組,復(fù)發(fā)次數(shù)少于PF組,均有統(tǒng)計(jì)學(xué)差異(P<0.05),見表2。
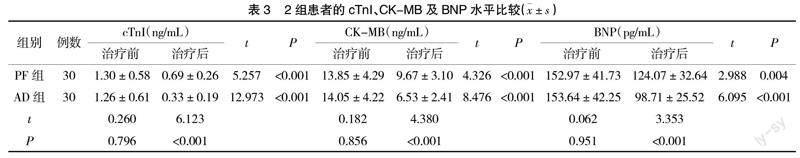
2.3? ? 2組患者的cTnI、CK-MB及BNP水平比較? ? 治療前,2組患者的cTnI、CK-MB及BNP水平比較,無統(tǒng)計(jì)學(xué)差異(P>0.05);治療后,2組患者的cTnI、CK-MB及BNP水平均低于治療前,且AD組低于PF組,有統(tǒng)計(jì)學(xué)差異(P<0.05),見表3。
2.4? ? 2組患者的TNF-α及hs-CRP水平比較? ? 治療前,2組患者的TNF-α及hs-CRP水平比較,無統(tǒng)計(jì)學(xué)差異(P>0.05);治療后,2組患者的TNF-α及hs-CRP水平均低于治療前,且AD組低于PF組,有統(tǒng)計(jì)學(xué)差異(P<0.05),見表4。
2.5? ? 2組患者的不良反應(yīng)比較? ? PF組不良反應(yīng)發(fā)生率為13.33%(4/30,低血壓及嘔吐各2例),AD組不良反應(yīng)發(fā)生率為6.67%(2/30,低血壓及嘔吐各1例),無統(tǒng)計(jì)學(xué)差異(χ2=0.185,P=0.389)。
3? ? 討論
SA屬于一種心肌功能障礙性疾病,會引起胸悶、低血壓等癥狀,甚至造成患者猝死。目前,治療SA藥物較多,主要包括β受體阻滯劑、鈉通道抑制劑及鈣通道拮抗劑等,均可在一定程度上改善臨床癥狀,保護(hù)患者心肌功能[5]。PF作為臨床上常用的Ⅰ類抗心律失常藥物,可通過阻斷鈉通道,減低傳導(dǎo)速度,延長動(dòng)作電位間期及有效不應(yīng)期,已成為治療SA的主要藥物[6]。AD屬于Ⅲ類抗心律失常藥物,屬于多通道離子阻滯劑,具有多種電生理效應(yīng),可對K+離子通道進(jìn)行阻斷,同時(shí)可阻滯Na+、Ca2+通道,減緩電沖動(dòng)傳導(dǎo)速度,延長電位時(shí)程,促使竇房結(jié)自律性降低[7]。
近年來,TNF-α及hs-CRP等炎性因子與心律失常間的關(guān)系受到臨床關(guān)注,可通過引起多種電生理途徑異常,進(jìn)而在細(xì)胞水平誘發(fā)SA,包括離子通道異常、折返環(huán)形成及動(dòng)作電位時(shí)間延長等。其中,TNF-α是由巨噬細(xì)胞、單核細(xì)胞合成,可阻滯心室肌細(xì)胞瞬時(shí)外向鉀電流,造成動(dòng)作電位時(shí)程(APD)平臺期延長,使復(fù)極離散度增加,誘發(fā)折返,影響心肌內(nèi)、外膜的單向動(dòng)作電位,導(dǎo)致復(fù)極異常[8]。hs-CRP可通過抑制肌漿網(wǎng)鈣離子交換,導(dǎo)致細(xì)胞內(nèi)鈣超載,并可對超氧化物歧化酶活性進(jìn)行抑制,發(fā)揮促心律失常的作用,是預(yù)測惡性心律失常的重要指標(biāo)[9]。本次研究結(jié)果顯示,AD組治療總有效率高于PF組,AD組復(fù)律時(shí)間短于PF組,復(fù)發(fā)次數(shù)少于PF組,治療后AD組cTnI、CK-MB、BNP及TNF-α、hs-CRP水平低于PF組(P<0.05)。提示AD治療SA效果優(yōu)于PF,有利于降低炎性因子水平,減輕炎癥反應(yīng)及心肌細(xì)胞損傷,并可縮短復(fù)律時(shí)間,預(yù)防疾病復(fù)發(fā),與龍琴等[10]研究結(jié)果具有一致性。分析原因可能為,AD具有多種電生理效應(yīng),具有鈣離子通道阻滯作用,可對心房炎癥反應(yīng)進(jìn)行抑制;同時(shí),AD作為一種磷脂酶A1、A2、C的抑制劑,可對花生四烯酸的產(chǎn)生進(jìn)行抑制,發(fā)揮抗炎效果[11]。與PF相比,AD在維持竇律方面效果良好,能夠?qū)跔顒?dòng)脈及其周圍血管進(jìn)行擴(kuò)張,延長動(dòng)作電位時(shí)程及有效不應(yīng)期,減少復(fù)發(fā),減輕對患者心肌的損傷。在用藥安全性方面,目前臨床上普遍認(rèn)為作為藥物復(fù)律及維持竇律的一線用藥,PF藥物不良反應(yīng)少,但該藥物用于老年患者中可能會引發(fā)肝腎功能損傷及血壓下降,在心源性休克、嚴(yán)重充血性心力衰竭等患者中禁用。AD不能用于高度房室傳導(dǎo)阻滯并未安裝起搏器、雙支傳導(dǎo)阻滯患者,同時(shí)對碘過敏及甲狀腺功能異常患者也不可使用[12]。不良反應(yīng)發(fā)生率為評估藥物治療效果的重要指標(biāo),不良反應(yīng)發(fā)生率高會對患者治療依從性造成影響,進(jìn)而影響治療效果。本次研究結(jié)果顯示,PF組與AD組患者的不良反應(yīng)發(fā)生率相近(P>0.05)。這可能與納入病例數(shù)少及治療周期短等有關(guān)。隨著AD用藥療程的延長,相關(guān)副作用發(fā)生率是否可能增加還有待繼續(xù)研究分析。
綜上所述,AD治療SA效果優(yōu)于PF,可對炎癥反應(yīng)進(jìn)行抑制,降低炎癥因子水平,減輕患者心肌損傷,降低復(fù)發(fā)次數(shù),有效控制病情進(jìn)展,安全可靠。
參考文獻(xiàn)
[1]? ? 王月平,李德平,任星星,等.穩(wěn)心顆粒聯(lián)合胺碘酮對心肌梗死合并室性心律失常治療效果及hs-CRP水平的影響[J].現(xiàn)代生物醫(yī)學(xué)進(jìn)展,2020,20(7):1339-1342.
[2]? ? 趙子明,袁義強(qiáng),尹曉盟,等.持續(xù)性心房顫動(dòng)射頻消融術(shù)后抗心律失常藥物應(yīng)用時(shí)程與預(yù)后的相關(guān)性分析[J].臨床心血管病雜志,2019,35(1):60-64.
[3]? ? 陳小麗,施林生,張清,等.胺碘酮治療老年急性心肌梗死室性心律失常的療效及短期預(yù)后的危險(xiǎn)因素分析[J].藥物生物技術(shù),2020,27(6):539-542.
[4]? ? 中華醫(yī)學(xué)會心血管病學(xué)分會,中國生物醫(yī)學(xué)工程學(xué)會心臟病學(xué)分會,中華心血管病雜志編輯委員會.室上性快速心律失常治療指南[J].中華心血管病雜志,2005,33(1):2-15.
[5] FIELD M E,HOLMES D N,PAGE R L,et al.Guideline-Concordant Antiarrhythmic Drug Use in the Get With The Guidelines-Atrial Fibrillation Registry[J].Circ Arrhythm Electrophysiol,2021,14(2):e008961.
[6]? ? 張麗,李筠,王健怡,等.普羅帕酮聯(lián)合普萘洛爾治療兒茶酚胺敏感性多形性室性心動(dòng)過速1例報(bào)告并文獻(xiàn)復(fù)習(xí)[J].臨床兒科雜志,2020,38(3):209-212.
[7]? ? CABELLO I,JACOB J,ARRANZ M,et al.Impact of emergency department management of atrial fibrillation with amiodarone on length of stay.A propensity score analysis based on the URGFAICS registry[J].Eur J Emerg Med,2020,27(6):429-435.
[8]? ? 賴曉峰,劉文.血清炎性因子水平與慢性心力衰竭并OSAS患者室性心律失常的關(guān)系及穩(wěn)心顆粒的干預(yù)作用[J].河北醫(yī)藥,2019,41(1):19-23.
[9]? ? 許麗娜,李娟,潘文.急性心肌梗死患者Tp-Te心電圖特征、CD40L、TNF-α與室性心律失常的關(guān)系[J].內(nèi)蒙古醫(yī)科大學(xué)學(xué)報(bào),2020,42(5):522-525.
[10]? ? 龍琴,方凱,李慶,等.普羅帕酮與胺碘酮治療室上性心律失常療效及對血?dú)庵笜?biāo)和心肌損傷標(biāo)志物的影響[J].昆明醫(yī)科大學(xué)學(xué)報(bào),2020,41(5):136-139.
[11]? ? 錢碧云,陳良川,王明偉,等.普羅帕酮與胺碘酮治療陣發(fā)性室上性心動(dòng)過速的療效與安全性[J].心血管康復(fù)醫(yī)學(xué)雜志,2019,28(2):221-224.
[12]? ? MARCELINO G P,COLLANTES C M C,OOMMEN J K,et al.Amiodarone-Induced Syndrome of Inappropriate Antidiuretic Hormone:A Case Report and Review of the Literature[J].P T,2019,44(7):416-423.
(收稿日期:2023-04-07)

