急性腦梗死病人遲發性癲癇發生現狀及Nomogram模型的構建


Status of delayed epilepsy in patients with acute cerebral infarction and Nomogram model construction
CHEN Ke,DONG Yuzhi,LI YuanyuanNanjing Drum Tower Hospital Group Suqian Hospital,Jiangsu 223800 ChinaCorresponding Author CHEN Ke,E-mail:chenkechenke9@163.com
Keywords acute cerebral infarction;delayed epilepsy;risk factors;Nomogram model;influencing factor
摘要 目的:探討急性腦梗死(ACI)病人遲發性癲癇的發生現狀及其危險因素,并以此構建Nomogram模型。方法:選取2022年7月—2023年6月在我院急診搶救的140例ACI病人列為模型組,2023年7月—2023年10月在我院急診搶救的60例ACI病人列為驗證組。采用多因素Logistic回歸分析探究ACI病人發生遲發性癲癇的影響因素,應用R語言軟件繪制列線圖,以此構建Nomogran風險預警模型。同時繪制受試者工作特征(ROC)曲線、校準曲線及臨床決策曲線,以評估該模型的預測性能和臨床適用性。結果:140例ACI病人中,43例發生遲發性癲癇,發生率為30.71%。Logistic回歸分析結果顯示,美國國立衛生研究院卒中量表(NIHSS)評分>15分、梗死部位為顳葉、病灶累及皮質、意識障礙、發熱是ACI病人發生遲發性癲癇的危險因素(Plt;0.05)。基于以上5個獨立危險因素構建風險預測模型,其ROC曲線下面積(AUC)為0.812[95%CI(0.735,0.889),Plt;0.001],敏感度為67.40%,特異度為82.50%,H-L擬合優度檢驗結果顯示,χ2=10.153,P=0.180,差異無統計學意義,表明該模型的擬合情況良好;校準曲線結果顯示,模型預測概率與實際發生情況具有良好的一致性;臨床決策曲線結果顯示,模型具有較高的臨床適用性。結論:NIHSS評分>15分、梗死部位為顳葉、病灶累及皮質、意識障礙、發熱是ACI病人發生遲發性癲癇的危險因素,據此構建的預測模型對于ACI病人的臨床管理具有較高的應用價值。
關鍵詞 急性腦梗死;遲發性癲癇;危險因素;Nomogram模型;影響因素
doi:10.12102/j.issn.2095-8668.2024.24.024
急性腦梗死(acute cerebral infarct,ACI)是指腦血管突發性閉塞導致腦部血液供應中斷,引起腦組織局部缺血和缺氧,造成腦功能障礙的臨床病癥[1]。癲癇的特征是大腦神經元異常放電引起的反復發作性癲癇發作,表現為短暫的大腦功能障礙,包括痙攣、抽搐、意識喪失等癥狀。腦梗死后癲癇發作是指發生腦梗死前無癲癇發作或無癲癇病史,但癲癇發作時間位于腦梗死后且與腦梗死有關[2]。根據首次癲癇發作時間不同可分為早發性癲癇發作和遲發性癲癇發作。通常把梗死事件發生7 d后出現的癲癇判定為遲發性癲癇發作[3]。有研究發現,腦梗死后癲癇發作會使病人住院時間延長、醫療費用增加、死亡率增加、生活質量下降、癡呆風險增加等,對病人產生各種負面影響[4]。故探究ACI后癲癇發作的危險因素十分必要。因此,本研究深入探究ACI后遲發性癲癇發生的危險因素,并據此構建Nomogram模型,旨在為此類病人的診斷、治療和預防提供參考。現報道如下。
1 對象與方法
1.1 研究對象
選取2022年7月—2023年6月在我院急診搶救的140例ACI病人作為研究對象,列為模型組,2023年7月—2023年10月搶救的60例ACI病人列為驗證組。納入標準:1)符合《中國急性缺血性腦卒中診治指南2018》[5]中ACI的診斷標準,且經影像學檢查確診;2)遲發性癲癇的診斷應符合2017年國際抗癲癇聯盟制定最新標準,即在腦梗死發生gt;7 d后發生的癲癇[6];3)發生腦梗死的時間<48 h;4)年齡≥20歲。排除標準:1)既往存在癲癇病史;2)合并嚴重的心、肝、腎功能不全或多臟器功能異常者;3)存在其他原因引起的癲癇發作或有中樞系統疾病者;4)既往有顱腦手術者。依據自變量為因變量的5~10倍原則,并考慮10%~20%的樣本量流失[7],本研究共納入18個自變量,最終確定應納入140例樣本量。同時依據模型組與驗證組的樣本量比例為7∶3的原則,故驗證組應納入60例病人。本研究已通過南京鼓樓醫院集團宿遷醫院醫學倫理委員會批準。
1.2 調查內容
調查內容包括性別、年齡、體質指數(body mass index,BMI)、美國國立衛生研究院卒中量表(National Institutes of Health Stroke Scale,NIHSS)評分、高血壓、糖尿病、心房顫動、吸煙史、飲酒史、梗死部位[顳葉、其他部位(額葉、頂葉、枕葉、基底節區等)]、病灶累及皮質情況、意識障礙情況、發熱情況、血清電解質指標、TOAST(Trial of Org 10172 in Acute Stroke Treatment)分型,并采用全自動生化分析儀(廠家為貝克曼,型號為DXC8000)對血清清蛋白、血紅蛋白、超敏C反應蛋白水平進行分析測定。
1.3 資料收集方法
由2名經過統一學習和培訓的研究員進行資料收集。通過我院的電子病歷數據庫查閱研究對象的病歷和護理記錄,按照要求填寫臨床資料調查表,并交叉核對。若有相關數據遺漏或錯誤,立即追溯原始資料進行補充和修正,以保證數據的準確性。
1.4 統計學方法
采用SPSS 21.0軟件處理數據。符合正態分布的定量資料用均數±標準差(x±s)表示,兩組數據比較行t檢驗;定性資料用例數和百分比(%)表示,采用χ2檢驗。采用多因素Logistic回歸分析探究影響ACI病人遲發性癲癇發生的獨立危險因素。采用R 3.5.3軟件包和rms程序包構建列線圖模型,并繪制受試者工作特征(receiver operating characteristic,ROC)曲線和決策曲線(decision curve analysis,DCA),采用Hosmer-Lemeshow檢驗進行擬合優度檢驗,并繪制校準曲線以評估預測模型的一致性。以P<0.05為差異有統計學意義。
2 結果
2.1 ACI病人遲發性癲癇發生現狀
140例ACI病人中,43例發生遲發性癲癇,發生率為30.71%,將其列為癲癇組。
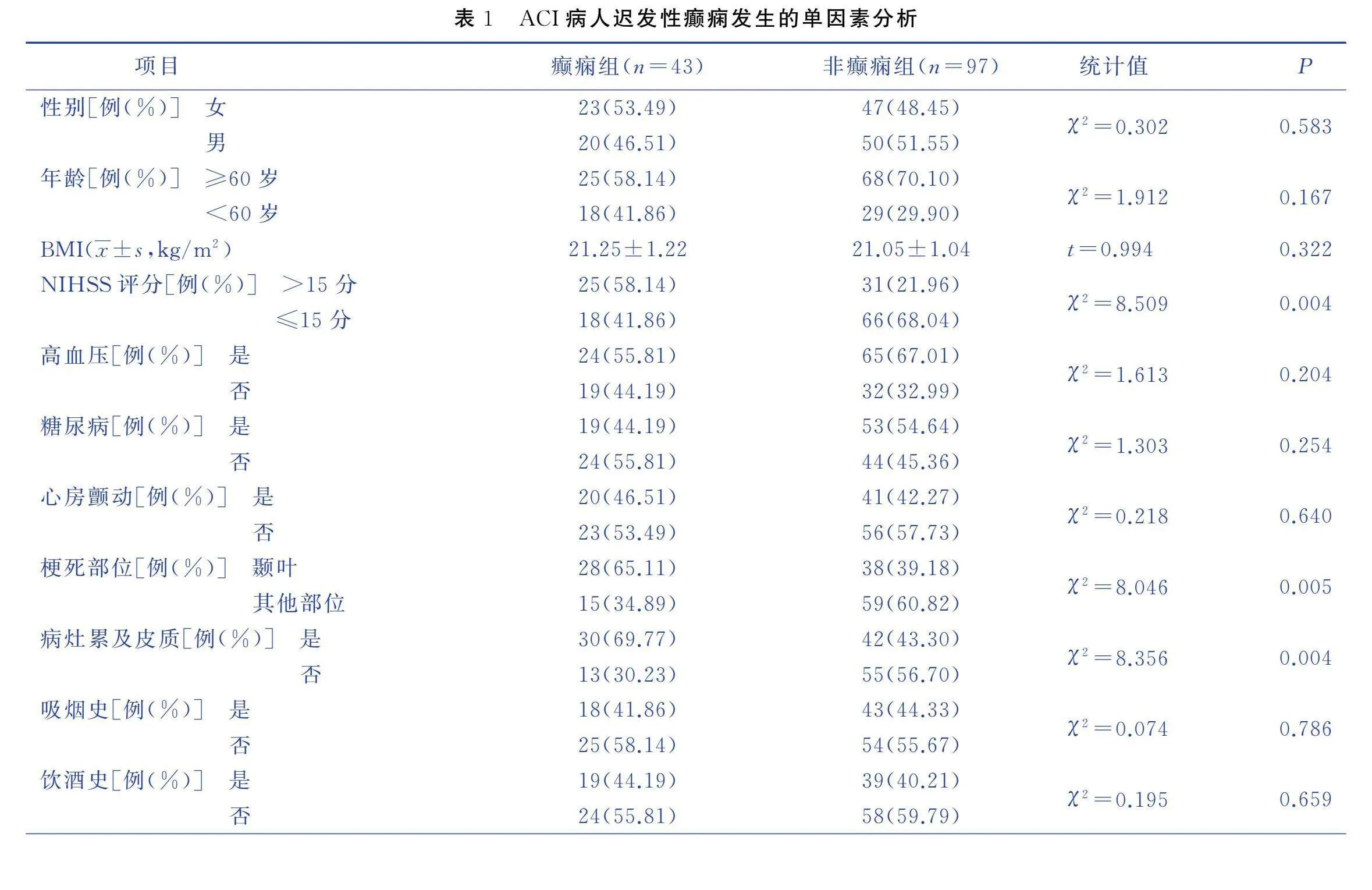
2.2 ACI病人遲發性癲癇發生的單因素分析
單因素分析結果顯示,NIHSS評分、梗死部位、病灶是否累及皮質、意識障礙情況、發熱情況均是ACI病人遲發性癲癇發生的影響因素(Plt;0.05)。見表1。
2.3 ACI病人遲發性癲癇發生的Logistic回歸分析
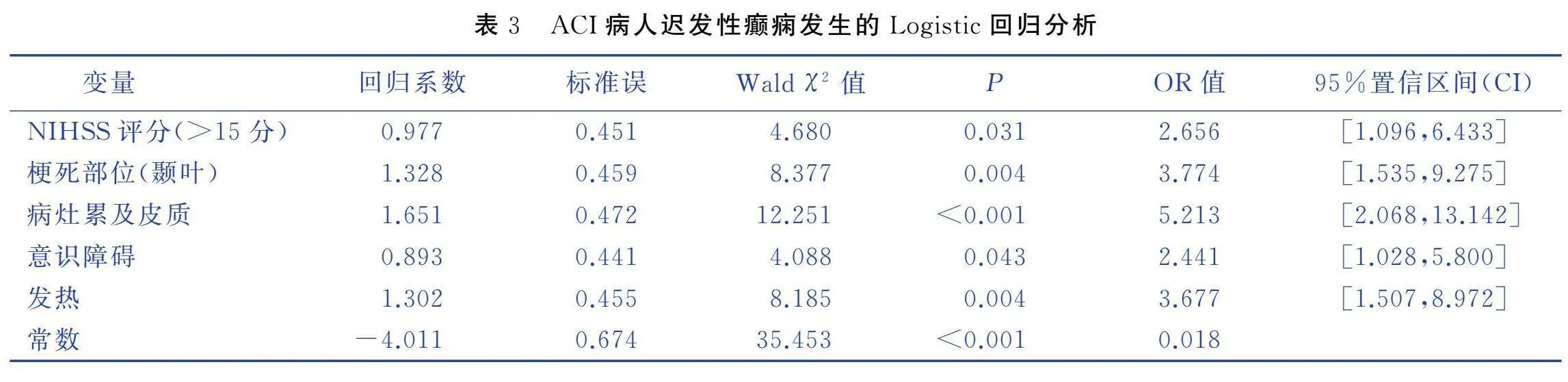
以有無發生遲發性癲癇為因變量(發生=1、不發生=0),將單因素分析中Plt;0.05的因素列為自變量進行Logistic回歸分析,自變量賦值情況見表2。Logistic回歸分析結果顯示,NIHSS評分>15分、梗死部位為顳葉、病灶累及皮質、意識障礙、發熱是ACI病人遲發性癲癇發生的危險因素(Plt;0.05),見表3。
2.4 ACI病人遲發性癲癇發生風險預測模型的構建
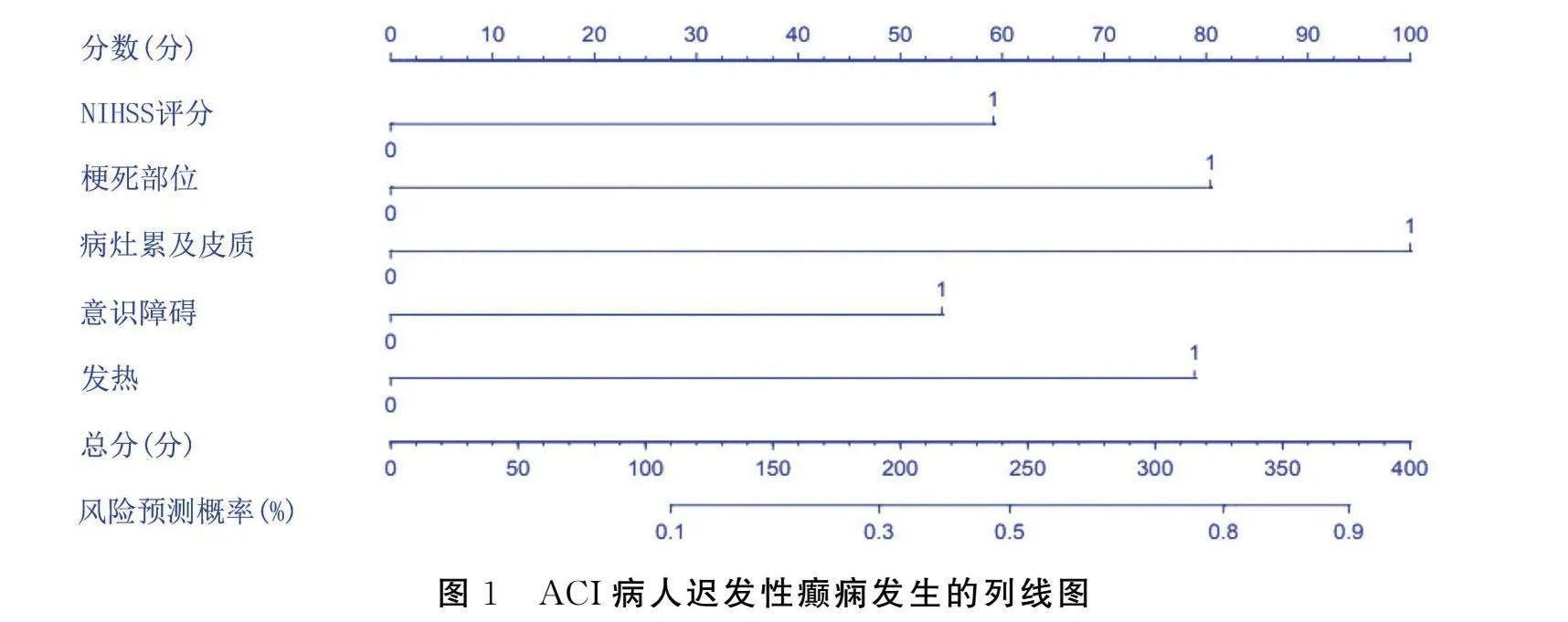
基于多因素Logistic回歸分析構建模型方程:Logit(P)=-4.011+0.977×NIHSS評分(>15分)+1.328×梗死部位(顳葉)+1.651×病灶累及皮質+0.893×意識障礙+1.302×發熱。基于此繪制列線圖,見圖1。
2.5 ACI病人遲發性癲癇發生風險預測模型的驗證
2.5.1 擬合優度檢驗
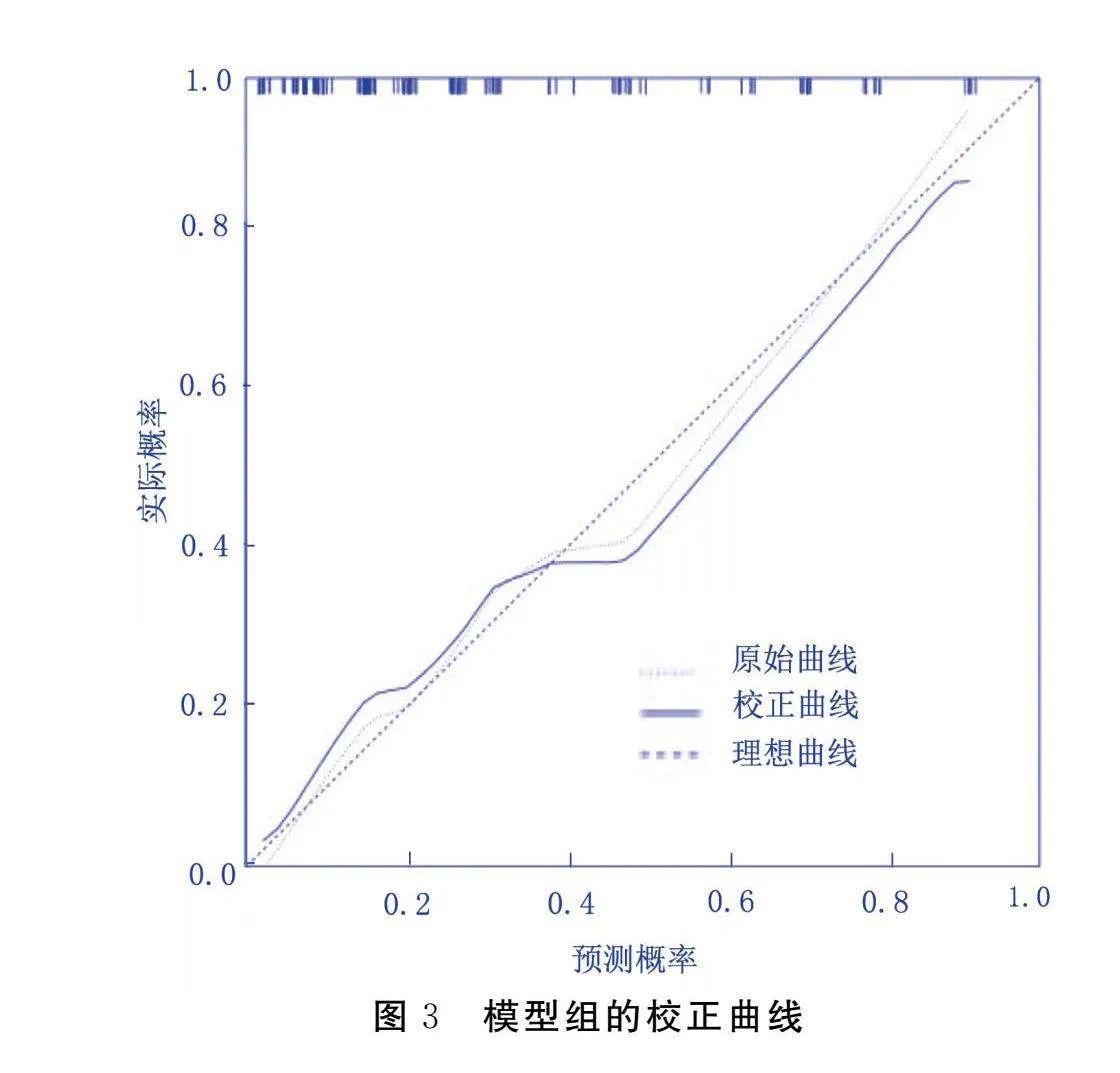
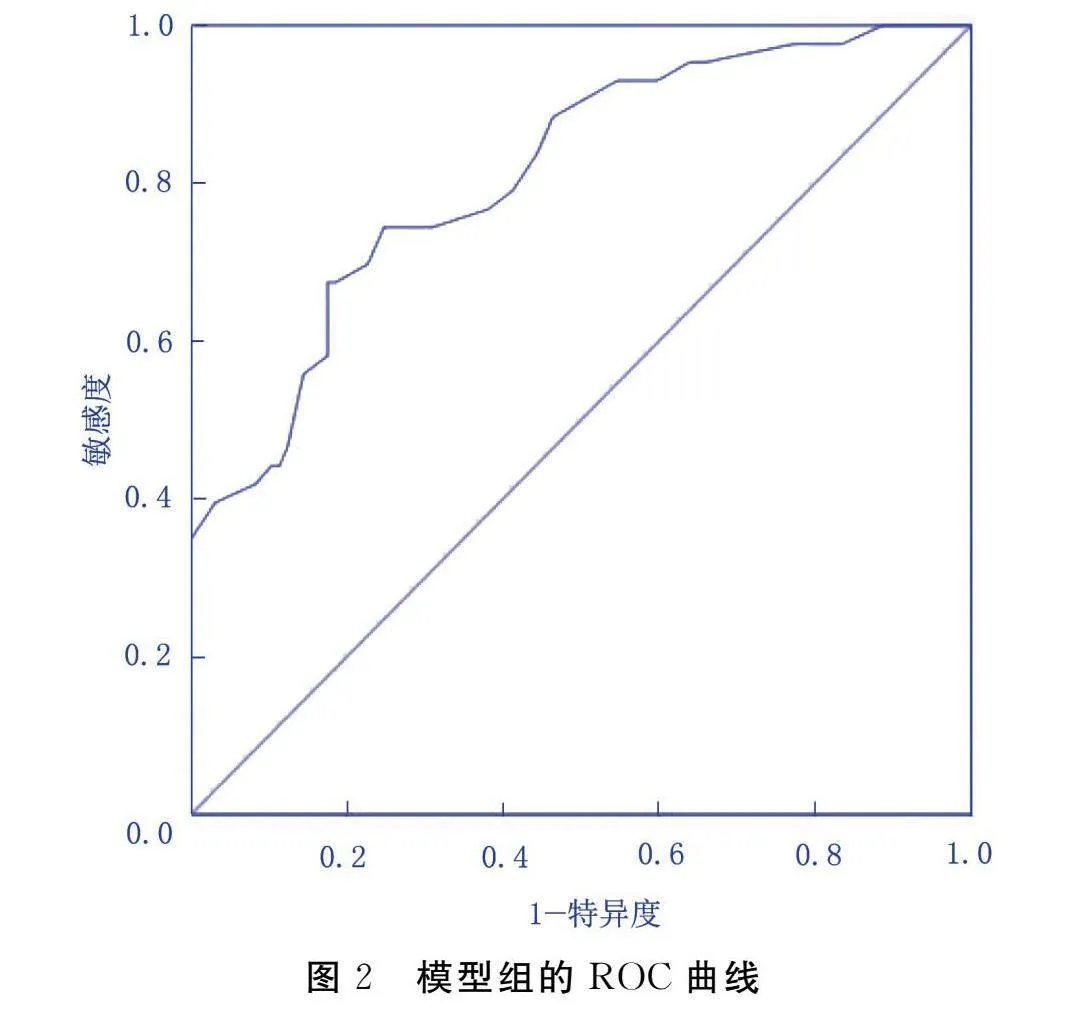
繪制模型組的ROC曲線,其ROC曲線下面積(AUC)為0.812[95%CI(0.735,0.889),Plt;0.001],敏感度為67.40%,特異度為82.50%,見圖2。擬合優度檢驗結果顯示,χ2=10.153,P=0.180,表明模型擬合情況良好,見圖3。
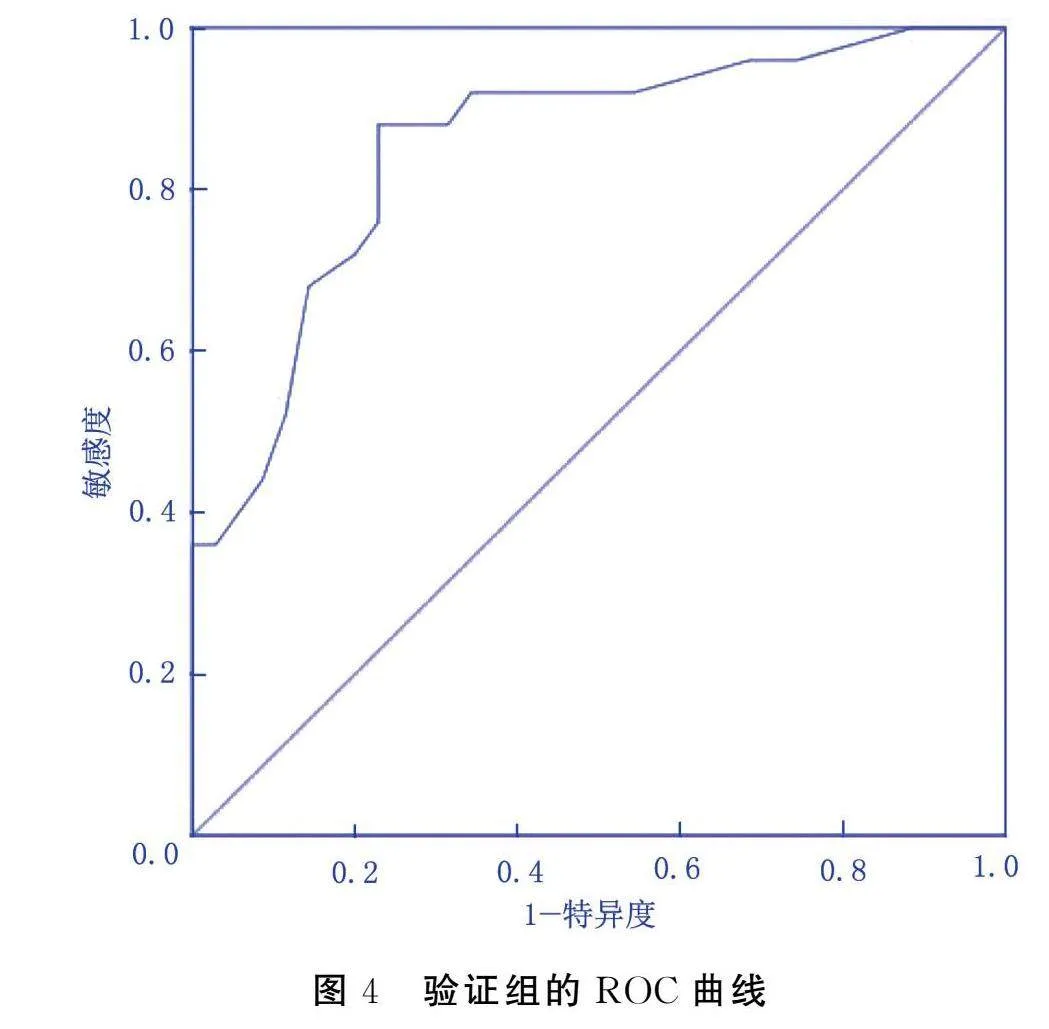
2.5.2 驗證組驗證
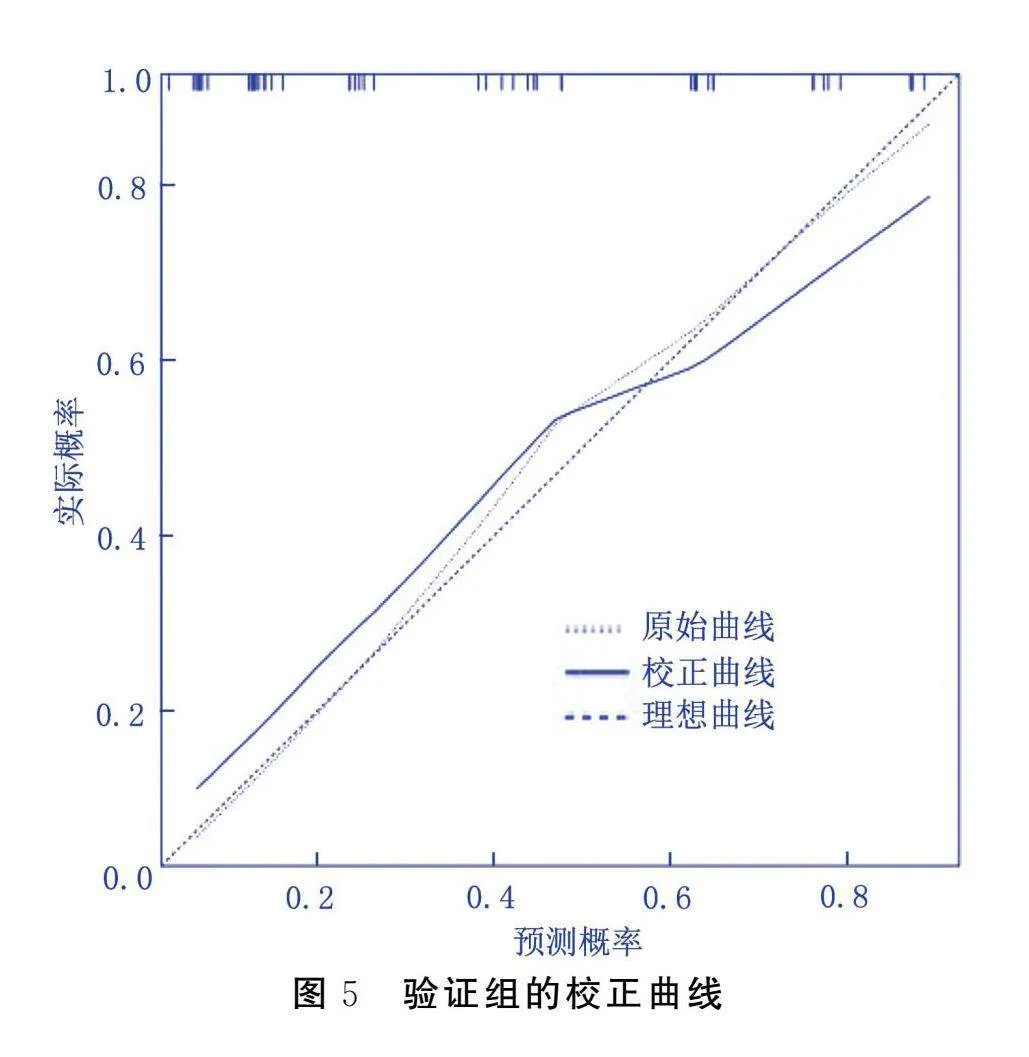
將已構建的風險預測模型在驗證組中進行驗證。其AUC為0.854[95%CI(0.755,0.952),Plt;0.001],敏感度為88.00%,特異度為68.60%,見圖4。擬合優度檢驗結果顯示,χ2=4.679,P=0.791,表明模型擬合情況良好,見圖5。
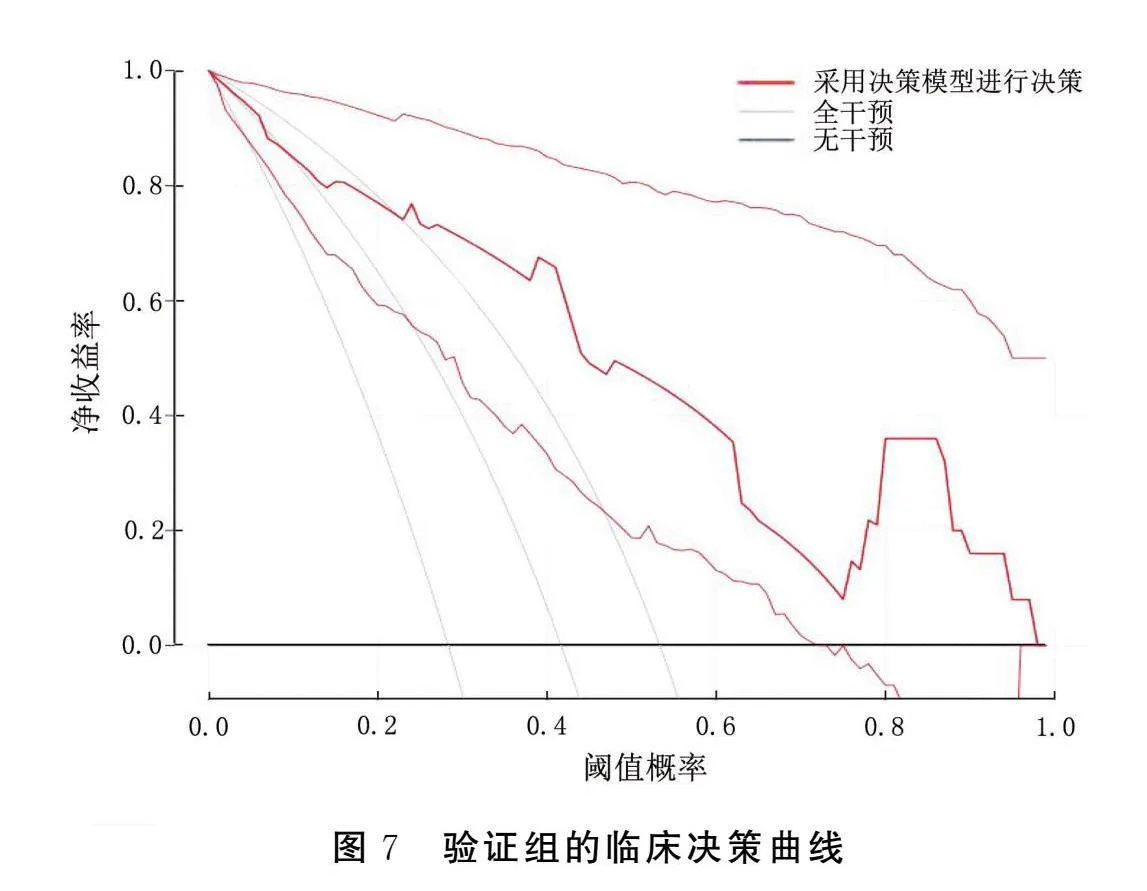
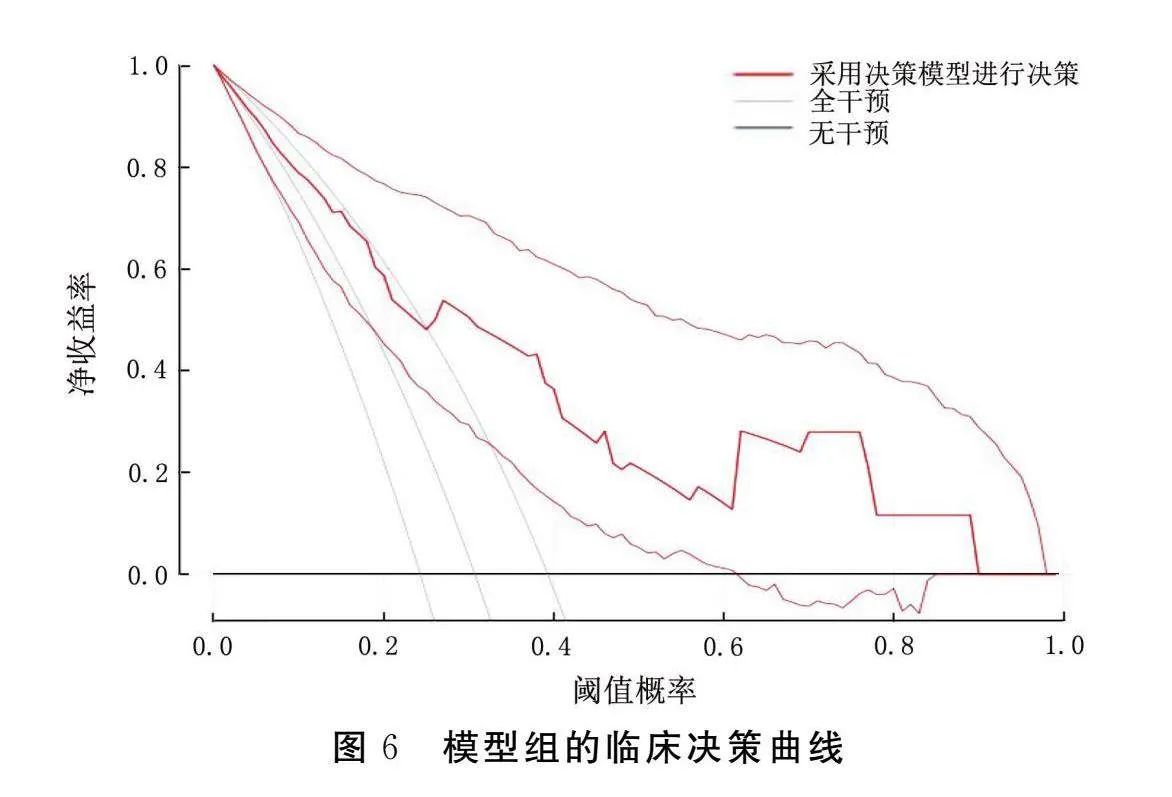
2.5.3 ACI病人遲發性癲癇發生風險預測模型的臨床適用性
模型組和驗證組的臨床決策曲線見圖6、圖7。結果顯示,對高風險病人進行及時干預可以使大部分病人受益,該模型具有較高的臨床應用價值。
3 討論
3.1 構建ACI病人遲發性癲癇發生風險預測模型的重要性
ACI病人遲發性癲癇均發生在腦梗死7 d后,其發生機制可能是星形膠質細胞的增加、神經突觸的調整及血腦屏障的破壞導致異常的興奮傳導通路激活、基因易感性增加及腦網絡連接的改變[8]。有研究表明,既往出現遲發性癲癇發作的ACI病人再次出現非誘發性癲癇發作的風險較高,癲癇發作后可能會加劇腦組織的缺氧、缺血,進而導致出現更多的神經損傷,對病人疾病預后及生活質量造成嚴重影響,甚至導致病人死亡[9]。本研究結果發現,140例在本院急診搶救的ACI病人中,43例發生遲發性癲癇,發生率為30.71%,與許育偉等[10]的研究結果相似,表明ACI病人遲發性癲癇仍具有較高發生率。因此,針對ACI病人遲發性癲癇發生的危險因素進行預防和護理是防治疾病所必要的。
3.2 ACI病人發生遲發性癲癇的影響因素
本研究結果顯示,NIHSS評分>15分、梗死部位為顳葉、病灶累及皮質、意識障礙、發熱均是ACI病人遲發性癲癇發生的獨立危險因素(Plt;0.05),與栗靜[11]的研究結果類似。
3.2.1 NIHSS評分
本研究結果顯示,NISHH>15分時ACI病人發生遲發性癲癇的風險增加。NIHSS主要用于評估病人的神經功能狀態,gt;15分通常表示病人神經功能受到嚴重損害,提示腦梗死情況嚴重,可能導致異常炎性因子和神經遞質在腦內的表達和釋放[12-13]。炎癥貫穿腦梗死的全過程,炎癥因子逐漸累積,且在癲癇發作中起重要作用,更增加了癲癇發作的風險。
3.2.2 梗死部位、病灶
本研究結果顯示,梗死部位為顳葉、病灶累及皮質是ACI病人遲發性癲癇發生的獨立危險因素。De-Reuck等[14]的研究表明,急性缺血性腦卒中后遲發性癲癇發作常發生在受累于大腦中動脈顳支區域的缺血性腦卒中病人中。神經元細胞體具有超興奮性,主要聚集在皮質層和顳葉,當梗死部位在顳葉累及皮質部位,會使皮層發生結構和功能上的改變,導致皮質興奮性的增加或抑制性神經元活動的減弱,從而增加癲癇發作的風險[15-16]。故對于顳葉梗死及病灶累及皮質的病人需要密切監測其癲癇的發生,及時給予干預和治療。
3.2.3 意識狀態、是否發熱
本研究結果顯示,意識障礙和發熱是ACI病人遲發性癲癇發生的獨立危險因素,與張偉國[17]的研究結果相似。分析原因可能是意識障礙病人的神經元興奮性增加可能導致癲癇閾值下降,從而增加癲癇發作的風險。可能與大腦受損、代謝紊亂、藥物使用等因素有關[18]。發熱也影響著ACI病人遲發性癲癇的發生,表明二者之間存在一定關系。發熱是ACI病人常見的并發癥。有研究表明,高熱會加重腦部缺血、缺氧情況,加速神經元損傷和炎癥反應的發展,從而增加癲癇的發生風險;特別是在腦組織受損后的恢復過程中,發熱可能會加劇腦部神經元的異常放電,誘發遲發性癲癇的發生[19]。因此,對于ACI病人,臨床護理人員應及時有效地采取降溫措施以減輕病人腦部缺血、缺氧的程度,有助于降低遲發性癲癇的發生。
3.3 ACI病人遲發性癲癇發生風險預測模型的預測能力
本研究結果顯示,模型組AUC為0.812[95%CI(0.735,0.889),Plt;0.001],敏感度為67.40%,特異度為82.50%,H-L擬合優度檢驗結果顯示,χ2=10.153,P=0.180(gt;0.05),表明模型擬合情況良好;校正曲線顯示模型預測概率與實際發生情況間具有良好的一致性;臨床決策曲線顯示模型具有較高的臨床實用價值。目前,關于ACI病人腦卒中后癲癇的研究多數為發病機制的研究,關于癲癇預警模型的相關研究較少,而關于預防遲發性癲癇發作的預測模型研究則更少。本研究通過分析ACI病人遲發性癲癇發生的危險因素,據此構建風險預測模型,更具有針對性,該模型的臨床應用價值較高。臨床護理人員應密切監視病人的神經狀態及癲癇發作跡象,及時采用亞低溫療法或神經保護藥物治療等措施,防止腦組織受損進一步惡化,減少遲發性癲癇的發生風險。
4 小結
綜上所述,ACI病人遲發性癲癇的發生與NIHSS評分、梗死部位、病灶累及皮質情況、意識狀態、發熱情況等有關,應該及時采取相應措施以降低遲發性癲癇的發生風險。本研究構建的風險預測模型具有較高的預測價值,可為臨床制定防治措施提供依據;但由于本研究樣本量有限,且僅納入本院收治的病人,可能對結果的準確性和推廣性產生影響。建議今后應進一步進行大規模、多中心的臨床研究以驗證本研究結論。
參考文獻:
[1] 李嵐欣,李波,茍偉.急性缺血性腦卒中后癲癇發作臨床特點及危險因素分析[J].臨床和實驗醫學雜志,2023,22(19):2021-2025.
[2] 劉震,尚偉.卒中后癲癇發作與卒中后癲癇[J].中國卒中雜志,2017,12(4):332-335.
[3] ZHAO L Q,LI J W,KLVIINEN R,et al.Impact of drug treatment and drug interactions in post-stroke epilepsy[J].Pharmacology amp; Therapeutics,2022,233:108030.
[4] 任重.腦卒中后癲癇發作的臨床特點、腦電圖表現及危險因素分析[J].中西醫結合心血管病電子雜志,2021,9(20):72-75.
[5] 中華醫學會神經病學分會,中華醫學會神經病學分會腦血管病學組.中國急性缺血性腦卒中診治指南2018[J].中華神經科雜志,2018,51(9):666-682.
[6] 李靜波,王玉,劉紅權.癲癇的診斷、命名及分類[J].中國臨床醫生雜志,2019,47(10):1140-1142.
[7] 胡雁,王志穩.護理研究[M].5版.北京:人民衛生出版社,2017:1.
[8] 劉英,向小爽,沙永紅.卒中后癲癇的研究進展[J].臨床醫藥實踐,2022,31(10):778-782.
[9] 林斯革,歐小凡.腦卒中后癲癇的危險因素長期隨訪[J].神經損傷與功能重建,2020,15(4):224-226.
[10] 許育偉,何文貞,李馥淳,等.急性缺血性腦卒中后遲發性癲癇發作的相關危險因素分析[J].汕頭大學醫學院學報,2023,36(3):169-171.
[11] 栗靜.腦梗死患者繼發性癲癇的危險因素分析及預警模型建立[D].太原:山西醫科大學,2023.
[12] 王羚,孫偉,劉昱君,等.卒中后癲癇發作和癲癇的危險因素與預測模型[J].國際腦血管病雜志,2022,30(9):689-694.
[13] 曾榕,刁麗梅.缺血性腦卒中后癲癇危險因素及預測模型研究[J].醫學研究雜志,2024,53(2):173-177.
[14] DE REUCK J,DE GROOTE L,VAN MAELE G,et al.The cortical involvement of territorial infarcts as a risk factor for stroke-related seizures[J].Cerebrovascular Diseases,2008,25(1/2):100-106.
[15] 龍亞德,陳國光,關春紅,等.80例卒中后癲癇的臨床特點及危險因素分析.廣東醫科大學學報,2018,36(3):244-246.
[16] 張靜,鮑婕妤,蔡萌萌,等.老年急性缺血性腦卒中后癲癇發作患者的臨床特點和危險因素[J].中風與神經疾病雜志,2023,40(6):512-517.
[17] 張偉國.腦卒中后癲癇發作的危險因素及預防對策探討[J].中國實用醫藥,2019,14(4):31-32.
[18] 付萌萌,汪銀洲,李永坤,等.早發性及遲發性急性缺血性卒中后癲癇的臨床特點分析[J].中國醫藥導報,2019,16(20):84-87.
[19] 張亮.缺血性腦卒中后癲癇臨床特點及相關危險因素分析[J].系統醫學,2020,5(20):62-64.
(收稿日期:2024-03-27;修回日期:2024-11-27)
(本文編輯趙奕雯)

