改進初中化學“溶解度”教學的實踐

摘 要:溶解度是初中化學的一個重點和難點,在教學的過程中,如何科學合理的突破重點和難點是教師需要重點研究和推敲的.在教學中需要分析難點的難,難在何處,重點的價值與地位又是如何?只有知己知彼,方能巧妙而輕松的突破重難點,達到減負高效的效果.
關鍵詞:溶解度;教學策略;初中化學
中圖分類號:G632文獻標識碼:A文章編號:1008-0333(2021)11-0088-02
作者簡介:劉建紅(1984.1-),女,江蘇省張家港人,本科,中小學一級教師,從事初中化學教學研究.
“溶解度”作為初中化學教學中的一個關鍵知識要點,也是歷年來中招考試中的必考點之一,且占據著較大的分值比例,能夠直接影響到整體化學成績.在新課標背景下的初中化學溶解度教學中,教師需花費更多心思、精力與時間改進教學形式與流程,幫助學生牢固掌握溶解度的相關知識,使其在解題時可以做到靈活自如的應用,從而改善整體教學成效.
一、精心設計探究活動,輔助學生夯實基礎
在初中化學溶解度教學中,為實現預期教學目標,教師首先需做的是輔助學生掌握基礎理論知識,讓他們輕松應對深層次的研究,為后續的解題訓練和中考做準備.初中化學教師應以教材為基本依托精心設計探究性學習活動,做到理論講授與實驗操作雙管齊下,引領學生以透徹理解溶解度的概念為前提,探究影響溶解度的條件,讓他們加深對條件的認識.
例如,在展開“溶解度”的概念教學時,教師先提問:平時把白糖或食鹽加到熱水中,能不能無限制的溶解到水中?為什么食鹽很容易溶解在水中,油卻不行呢?相同量的一杯熱水和冷水中能溶解的食鹽會一樣多嗎?要求學生列舉一些常見溶液中的溶質與溶劑,使其結合生活常識回答問題和思考原因.接著,教師演示實驗:在室溫下,向盛有20 mL水的燒杯中加入5 g氯化鈉攪拌,等完全溶解后,再加5 g的氯化鈉攪拌,觀察現象,然后加入15 mL的水,攪拌觀察現象.學生注意觀察和記錄,認識飽和溶液與不飽和溶液的概念,隨后組織他們繼續結合實驗探尋溶解度的必要條件,即為溫度一定,水的質量相同,均達到飽和,使其把100 g水中溶解的最大量計算出來,順利得出溶解度的概念.
上述案例,教師精心設計探究活動,引領學生由舊及新、由淺及深的學習新知識,通過溶解食鹽的實驗方法讓他們建立溶解度的概念,突破難點,并用溶解對比的方法加強認知.
二、適當設置思維訓練,理清概念內涵外延
在初中化學溶解度教學過程中,針對溶解度概念的學習與應用,對學生的思維水平要求較高,要有一定的思維深度,教師需適當設置一些思維訓練活動,圍繞課本知識與教學目標巧妙設置一系列問題,由淺及深的引領學生探索溶解度的概念,并搭配實驗操作,指導他們采用控制變量法設計、操作和完成實驗,借此發展化學思維,使其全面掌握該部分內容.
比如,在“溶解度曲線”教學中,教師談話導入:大家已經知道溶解度是定量比較物質溶解能力大小的量度,那么如何表示物質的溶解度呢?多媒體課件中同步展示物質在不同溫度下的溶解度數據表,要求學生回憶數學課中的列表法,同時利用信息技術手段演示描點畫曲線的過程,指導他們自主練習把列表法轉變為曲線法表示.接著,教師在課件中展示多種物質在同一坐標體系中的圖像,提問:利用這樣的溶解度曲線圖給我們能做些什么?鼓勵學生自由討論,激活他們的化學思維,并出示氯化銨、氯化鉀、硼酸、硝酸鉀、硝酸鈉等物質的溶解度曲線,搭配一組有關溫度、溶解度的問題,使其結合溶解度曲線分析和回答,體會用途,討論固體物質溶解度受溫度變化影響情況.
對于上述案例,教師借助問題串設置思維訓練活動,極力發揮問題的導向功能,讓學生的思維始終處于活躍狀態,使其形成科學的思維方法,幫助他們初步學會應用溶解度曲線.
三、科學歸納所學知識,便于學生記憶運用
知識的歸納與總結屬于課堂教學中的一個常規環節,還是一個慣用手段,是從多個個別事物中概括出一般性規律、結論、原則或概念的思維方法.在初中化學溶解度教學中,教師需指導學生科學、嚴謹的歸納所學知識,目的有兩個,一方面進一步挖掘溶解度的本質,使其加深掌握溶解度的外延與內涵,另一方面便于他們更好的記憶與運用溶解度相關知識.
以探究“影響固體溶解度的因素”為例,由于教材中明確給出溶解度的定義,在課堂小結環節,教師可引導學生根據具體定義對影響固體溶解度大小的因素進行以下歸納:溶質與溶劑本身的性質屬于內因,溫度則屬于外因.這時要設置疑問:難道影響固體物質溶解度大小的外部因素只有一個溫度嗎?假如溶液中含有兩種或多種溶質,各個溶質之間是否也會對溶解度產生的一定的影響?學生知道在兩種含有相同離子的鹽溶于水時,它們的溶解度與平常相比均會有所降低,如:在一樣的溫度下,氯化鈉在氯化鉀溶液中的溶解度與在水中相比就較小,同樣氯化鉀在氯化鈉溶液中的溶解度和在水中相比也較小,所以溫度只是影響溶解度的外因之一.
在上述案例中,教師引領學生科學歸納所學知識,使其在歸納中反思和討論,發現存在的不足和問題,借此彌補不足和查漏補缺,確保總結的科學性,方便以后用來探究和解題.
四、合理選擇習題訓練,提升學生熟練程度
對于初中化學溶解度教學而言,要想有效改進教學質量與效果,不能僅僅停留在理論知識的講授方面,還需合理選擇一些練習題組織學生訓練,使其通過解題進一步鞏固溶解度,訓練他們的學習方法與化學思維.初中化學教師需圍繞溶解度科學設置一系列高水平的練習題,且注重習題的質量,而并非數量,讓學生結合個人所學解題,提升他們的熟練程度.
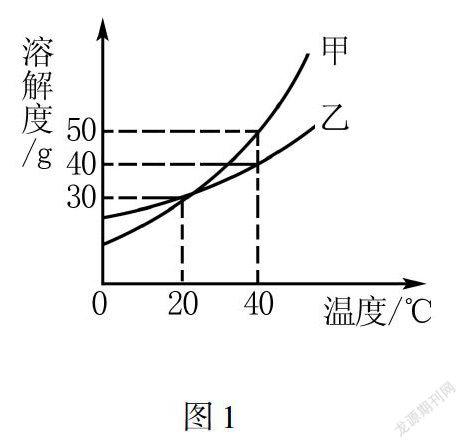
例1 甲、乙兩種固體物質的溶解度曲線如圖1所示,下列說法不正確的是().圖1
A.40℃時,甲的溶解度大于乙的溶解度
B.甲、乙物質的溶解度都隨溫度的升高而增大
C.20℃時,甲乙溶液中溶質的質量分數一定相等
D.將40℃時乙的飽和溶液降溫至20℃,仍然是飽和溶液
解析 對于A,根據溶解度曲線可知,40℃時甲的溶解度比乙的溶解度大,故正確;對于B,結合溶解度曲線得知,甲、乙兩種物質的溶解度都隨溫度的升高面增大,也正確;對于C,沒有確定溶液的狀態,無法判定20℃時,甲、乙溶液中溶質的質量分數,所以錯誤;對于D,乙的溶解度隨溫度降低而減小,將40℃時乙的飽和溶液降溫至20℃,有晶體析出,仍然是飽和溶液,同樣正確.故選C.
如此,教師圍繞溶解度設置練習題,指導學生仔細看圖后找到關鍵信息,需要注意是要掌握溶解度曲線圖的看法,使其通過思考和分析判斷每一項,在練習中慢慢提升熟練程度.
五、注重知識實踐應用,促使學生深化理解
在化學知識體系中,溶解度是一個定量表示物質溶解性強弱的化學概念,內涵相當豐富,只有通過一些實際應用,才能夠促使學生深化理解這一概念,讓他們學會運用溶解度相關知識分析和處理一些實際問題,真正實現學以致用的教學效果.初中化學教師需引入一些生活中有關溶解度的化學現象,引導學生從定量視角來解析,使其學會運用溶解度處理問題.
例2 在20℃的環境下,往飽和食鹽水中通入足量的二氧化碳與氨,為什么會有碳酸氫鈉晶體析出?
解析 這其實就是侯氏制堿法的原理,要想解決這一問題,就需用到溶解度的相關知識.
解:已知溫度為20℃,食鹽中主要成分氯化鈉的溶解度是36g/100g水,碳酸氫鈉的溶解度是9.7g/100g水,在這里可以假設20℃時,氯化鈉的飽和溶液是136g,則:
NaCl+NH3+CO2+H2ONaHCO3+NH4Cl
58.51884
36 gm(H2O)m(NaHCO3)
58.536g=18m(H2O)=84m(NaHCO3)
解得m(H2O)≈11.1g,m(NaHCO3)≈51.7 g.
通過計算能夠發現136 g氯化鈉飽和溶液中通入足量的二氧化碳與氨,溶劑的質量將會減少11.1 g,這時最多可以溶解碳酸氫鈉8.6 g,而實際上生成的碳酸氫鈉質量是51.7g,遠遠大于8.6g,所以會導致晶體析出.
針對上述案例,教師結合生活化問題引出溶解度知識的實際運用,讓學生認識到生活中處處與化學,使其意識到化學知識的實用性和價值,促使他們掌握有關溶解度的計算方法.
總而言之,在初中化學教學活動中,“溶解度”既是一大重點,還是難點之一,教師需結合學生實際情況科學合理的運用教學方法與模式,使其順利建立飽和溶液和不飽和溶液的概念,了解溶解度的含義和溶解度曲線的應用,助推他們真正學習好關于溶解度的知識.
參考文獻:
[1]龍昌華.例談溶解度曲線的化學涵義解讀[J].化學教學,2017(08):90-92+97.
[2]王文婭.淺議初中溶液教學中抽象概念的形象化[J].化學教與學,2017(01):82-83+90.
[責任編輯:季春陽]

