發(fā)展學(xué)生證據(jù)推理素養(yǎng)的項(xiàng)目式教學(xué)
江合佩 陳寒與 張賢金


















摘要: 以“科學(xué)家首次通過視頻捕捉到原子的形成和化學(xué)鍵的斷裂”作為真實(shí)情境,解構(gòu)其中蘊(yùn)含的化學(xué)鍵等學(xué)科難點(diǎn)問題,設(shè)計(jì)成能力不斷進(jìn)階的四個(gè)挑戰(zhàn)性學(xué)習(xí)任務(wù)。通過建立數(shù)據(jù)、圖像與核心知識(shí)的有效關(guān)聯(lián),進(jìn)行證據(jù)推理,形成對(duì)原子間相互作用的知識(shí)系統(tǒng)化、結(jié)構(gòu)化認(rèn)識(shí),發(fā)展學(xué)生的證據(jù)推理意識(shí),培養(yǎng)學(xué)生的科學(xué)探究與創(chuàng)新意識(shí)素養(yǎng)。
關(guān)鍵詞: 情境解構(gòu); 模型建構(gòu); 證據(jù)推理; 創(chuàng)新意識(shí); 項(xiàng)目式教學(xué)
文章編號(hào): 1005-6629(2022)05-0050-08
中圖分類號(hào): G633.8
文獻(xiàn)標(biāo)識(shí)碼: B
1 項(xiàng)目教學(xué)主題分析
我國(guó)基礎(chǔ)教育化學(xué)課程改革的基本走向之一是課程內(nèi)容重視反映化學(xué)知識(shí)的創(chuàng)新與發(fā)展,既縮小中學(xué)化學(xué)與現(xiàn)代化學(xué)的距離,又重視中學(xué)生的可接受性,讓學(xué)生更好地適應(yīng)現(xiàn)代生活化學(xué)化的現(xiàn)實(shí)[1]。《普通高中化學(xué)課程標(biāo)準(zhǔn)(2017年版)》在“基本理念”中指出“以發(fā)展化學(xué)學(xué)科核心素養(yǎng)為主旨,選擇體現(xiàn)基礎(chǔ)性和時(shí)代性的化學(xué)課程內(nèi)容”[2]。分子及其聚集態(tài)逐漸成為現(xiàn)代化學(xué)主要研究對(duì)象,構(gòu)成分子及其聚集態(tài)的微粒運(yùn)動(dòng)越來越受到人們的關(guān)注。科學(xué)家第一次通過視頻捕捉到了原子的形成和化學(xué)鍵的斷裂[3],使得過去只能靠猜測(cè)和想象的微觀原子間化學(xué)鍵的演化、斷裂和形成過程變得清晰可見。這樣具有鮮明時(shí)代特征和高度挑戰(zhàn)的情境素材如果引入真實(shí)的課堂教學(xué),設(shè)計(jì)成項(xiàng)目式學(xué)習(xí),無(wú)疑對(duì)培養(yǎng)學(xué)生的科學(xué)探究與創(chuàng)新意識(shí)素養(yǎng)有著不可估量的價(jià)值與意義。
科學(xué)理論和規(guī)律是不同類型的科學(xué)知識(shí),但兩者都有證據(jù)支持,可以根據(jù)新的證據(jù)或數(shù)據(jù)解釋進(jìn)行修正[4]。所謂證據(jù)是“一系列可用的事實(shí)或信息,表明某個(gè)信念或主張是真實(shí)或有效的”,其具有真實(shí)性、關(guān)聯(lián)性、唯一性和同一性[5]。本項(xiàng)目式學(xué)習(xí)可作為選擇性必修《物質(zhì)結(jié)構(gòu)與性質(zhì)》第二章“微粒間相互作用與物質(zhì)性質(zhì)”單元復(fù)習(xí)課,通過設(shè)計(jì)探究活動(dòng)與小組合作學(xué)習(xí),主動(dòng)發(fā)現(xiàn)有用的數(shù)據(jù)和圖像信息,并與已學(xué)核心知識(shí)建立有效關(guān)聯(lián),形成證據(jù)推理,得出結(jié)論。其操作流程如圖1所示。
2 項(xiàng)目教學(xué)目標(biāo)
根據(jù)課程標(biāo)準(zhǔn)的內(nèi)容和學(xué)業(yè)要求,結(jié)合學(xué)生實(shí)際的認(rèn)知基礎(chǔ),制定教學(xué)目標(biāo)如下:
(1) 通過用于微觀結(jié)構(gòu)測(cè)定和分析儀器介紹,嘗試結(jié)合圖像證據(jù)和數(shù)據(jù)證據(jù),了解微粒間相互作用的情況,建立科學(xué)探究的一般程序,構(gòu)建化學(xué)科學(xué)研究過程的方法模型。
(2) 利用科學(xué)探究方法模型,引導(dǎo)學(xué)生大膽猜想,尋找證據(jù),推理論證,進(jìn)一步認(rèn)識(shí)共價(jià)鍵的特點(diǎn)。
(3) 通過對(duì)Re2分子在電鏡下后續(xù)的異常行為進(jìn)行深入分析,進(jìn)而推測(cè)化學(xué)鍵轉(zhuǎn)變的可能性,培養(yǎng)學(xué)生敢于質(zhì)疑和批判,拓展分析和解決問題的角度與思路,激發(fā)學(xué)生探索未知世界的熱情。
3 項(xiàng)目任務(wù)及教學(xué)流程
根據(jù)教學(xué)目標(biāo),遴選“科學(xué)家首次捕捉到原子化學(xué)鍵的形成和斷裂視頻”真實(shí)情境,抽提出原子間相互作用的相關(guān)學(xué)科核心知識(shí),將其轉(zhuǎn)化為驅(qū)動(dòng)性問題,設(shè)計(jì)四個(gè)不斷進(jìn)階的學(xué)習(xí)活動(dòng)任務(wù),教學(xué)思路如圖2所示。
4 項(xiàng)目實(shí)施及學(xué)生學(xué)習(xí)結(jié)果
4.1 情境引入: 科學(xué)家首次捕捉到原子化學(xué)鍵形成和斷裂視頻
[情境導(dǎo)入]請(qǐng)欣賞宏觀的冰晶體與微觀的水分子結(jié)構(gòu)之間的差異(圖略),分析宏觀特征與微觀結(jié)構(gòu)之間的關(guān)系?
[生]宏觀特征反映微觀結(jié)構(gòu),微觀結(jié)構(gòu)決定宏觀特征。
[追問]水分子內(nèi)H—O鍵的鍵長(zhǎng)只有0.1~0.3nm,是頭發(fā)絲60萬(wàn)分之一,能否用肉眼直接觀測(cè)得到?
[提供信息]研究物質(zhì)微觀結(jié)構(gòu)的工具: 透射電子顯微鏡(TEM),可觀察物質(zhì)表面結(jié)構(gòu)、解析原子的位置、時(shí)空連續(xù)性采樣成像。
[播放視頻]播放2個(gè)錸原子形成化學(xué)鍵并斷裂的視頻。
[設(shè)疑]原子以化學(xué)鍵的形成和斷裂而聞名,這一過程對(duì)宇宙萬(wàn)物來說至關(guān)重要。但因?yàn)樗l(fā)生在非常小的范圍內(nèi),所以很難對(duì)其展開研究和記錄。前不久,來自諾丁漢大學(xué)的安德烈·霍爾比斯托夫教授和烏爾姆大學(xué)的曹克誠(chéng)博士首次通過視頻捕捉到了原子的形成和化學(xué)鍵的斷裂。如何辨識(shí)其微粒間的相互作用力呢?
設(shè)計(jì)意圖: 以宏觀世界冰晶體與微觀世界水分子內(nèi)作用力的關(guān)系引發(fā)學(xué)生對(duì)微觀世界探秘的興趣;播放錸原子化學(xué)鍵的形成和斷裂視頻,設(shè)計(jì)挑戰(zhàn)性任務(wù),激發(fā)學(xué)生主動(dòng)探究的愿望。
4.2 任務(wù)1: 辨識(shí)微粒間作用力
[活動(dòng)與探究]觀察2個(gè)錸原子與錸金屬簇運(yùn)動(dòng)以及核間距的差異性(如圖3),提出合理的猜想。你是根據(jù)哪些證據(jù)得到相關(guān)結(jié)論的?
[組1]2個(gè)錸原子為獨(dú)立的原子,猜想是弱作用力即范德華力。
[組2]2個(gè)錸原子雖然為獨(dú)立的原子,查閱錸原子半徑為0.188nm,測(cè)得其核間距為0.22nm<0.376nm(原子半徑之和),因此猜想是強(qiáng)作用力即化學(xué)鍵。
[師]非常好,組1是從定性的視角、組2是從定量的視角,到底是哪一組的分析是正確的呢?證據(jù)是否充分呢?
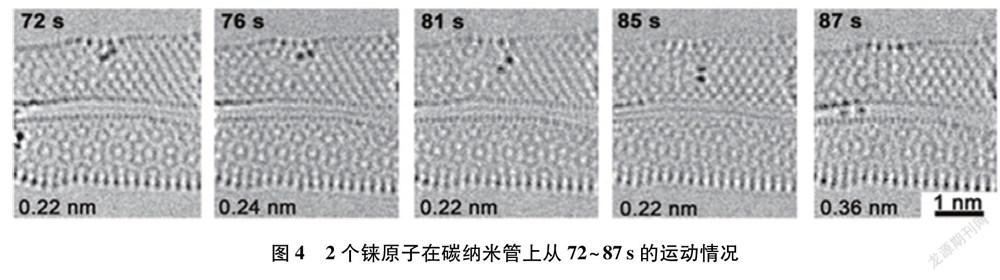
[提供信息]錸原子在碳納米管基底上從72~87s的運(yùn)動(dòng)情況如圖4所示。
[生]根據(jù)圖4可獲得“在電子束激發(fā)下,兩原子以整體形式移動(dòng)”的證據(jù),由此可推理得出2個(gè)錸原子間存在強(qiáng)作用力即化學(xué)鍵。
[方法導(dǎo)引]科學(xué)研究的一般過程如圖5所示。
[提供信息]錸(Re),原子序數(shù)為75,過渡金屬元素,電負(fù)性為1.9,原子半徑為0.188nm。
[追問]2個(gè)錸原子間的化學(xué)鍵屬于哪種類型,提出猜想,提供證據(jù),分析得出合理結(jié)論。
[組1]無(wú)得失電子情況,不屬于離子鍵。
[組2]不存在“自由電子”和金屬陽(yáng)離子之間的強(qiáng)相互作用,不屬于金屬鍵。
[組3]觀察到兩個(gè)錸原子沿著碳納米管移動(dòng),原子振動(dòng)過程中從圓形變?yōu)闄E圓形,說明有電子云重疊,因此可從電子云形狀判斷為共價(jià)鍵。
[組4]分析數(shù)據(jù): (1)電負(fù)性1.9,接近2.0;(2)核間距<半徑之和,因此傾向于共用電子;又原子軌道重疊,所以化學(xué)鍵為共價(jià)鍵。
設(shè)計(jì)意圖: 通過呈現(xiàn)2個(gè)錸原子在碳納米管上的運(yùn)動(dòng)數(shù)據(jù),有效關(guān)聯(lián)化學(xué)鍵、范德華力;離子鍵、共價(jià)鍵、金屬鍵等核心知識(shí),通過證據(jù)推理,得出合理結(jié)論,打破學(xué)生認(rèn)為金屬原子之間作用力為金屬鍵的錯(cuò)誤認(rèn)知,發(fā)展學(xué)生證據(jù)推理意識(shí),培養(yǎng)學(xué)生創(chuàng)新思維。
4.3 任務(wù)2: 共價(jià)鍵模型的再認(rèn)識(shí)
[提供信息]Re2分子鍵長(zhǎng)與成鍵數(shù)目的關(guān)系見表1。
[設(shè)疑]結(jié)合圖4和表1數(shù)據(jù),分析81s時(shí)碳納米管上吸附的Re2分子中錸原子間的共價(jià)鍵數(shù)目及類型。
[組1]透射電鏡中呈現(xiàn)出的Re2分子中Re—Re鍵平均鍵長(zhǎng)為0.22nm,因此Re2主要形成四重鍵。
[組2]兩原子間形成共價(jià)鍵,原子軌道僅能形成一個(gè)“頭碰頭”重疊,其余為“肩并肩”重疊,因此Re2分子內(nèi)含有1個(gè)σ鍵、3個(gè)π鍵。原子軌道重疊程度大,鍵能大。
[拓展分析]分子軌道理論認(rèn)為,有d軌道參與成鍵,形成的是1個(gè)σ鍵、2個(gè)π鍵、1個(gè)δ鍵,如圖6所示。
[提供信息]錸原子在碳納米管基底上從89~132s的運(yùn)動(dòng)情況(如圖7所示)。
[提問]根據(jù)圖7電鏡圖像,找出異常現(xiàn)象,并推測(cè)Re原子間作用力變化情況。
[組1]分析89~94s透射電鏡圖可知,89s時(shí),原子變橢圓,核間距略大于單鍵鍵長(zhǎng);94s時(shí),原子變圓,核間距大于2倍半徑,基于以上證據(jù)可得共價(jià)鍵逐漸斷裂。
[組2]分析94~132s運(yùn)動(dòng)情況可知,94s時(shí),原子為圓形,核間距略大于2倍半徑;132s時(shí),原子變橢圓,核間距接近單鍵與四重鍵鍵長(zhǎng),基于以上證據(jù)可得共價(jià)鍵逐漸形成。
[師]非常好,89~132s過程中,核間距增大→軌道重疊減小(89s)→原子伸縮振動(dòng)→共價(jià)鍵斷裂(94s)→形成共價(jià)單鍵(97s)→碰撞、軌道重疊→軌道進(jìn)一步重疊、核間距減小,形成共價(jià)四鍵(132s),通過圖像證據(jù)觀察到了共價(jià)鍵斷裂與形成的真實(shí)過程。
[提問]Re2分子中
四重鍵鍵能很大,為何會(huì)自行斷裂?大膽猜想,收集證據(jù)進(jìn)行合理推理。
[生]通過化學(xué)鍵成鍵與斷裂的過程可知,Re2分子中四重鍵斷裂可能是因?yàn)槭艿酵饬ψ饔没蛭疹~外能量。
[活動(dòng)與探究]Re2分子受到哪些外力作用,找出相應(yīng)的證據(jù),進(jìn)行合理的推斷;Re2分子可能會(huì)采取哪種方式吸收能量,找出相應(yīng)的證據(jù),進(jìn)行合理的推斷。
[小組合作]提出猜想,尋找證據(jù),進(jìn)行分析推理。
[師]哪個(gè)小組愿意分享成果?請(qǐng)用表格進(jìn)行展示。
[組1]見表2。
[組2]見表3。
[追問]根據(jù)表4提供的數(shù)據(jù)分析,碳納米管中碳原子雜化類型是什么?隨著碳納米管管徑的增大,碳原子雜化類型的變化趨勢(shì)是什么?據(jù)此分析碳納米管具有導(dǎo)電性的原因。
[生]碳納米管的碳碳鍵長(zhǎng)介于金剛石(sp3雜化)和石墨(sp2雜化)之間,且更接近于石墨的碳碳鍵鍵長(zhǎng),因此以sp2雜化為主,類似于單層石墨烯,具有離域大π鍵,具有很好的電學(xué)性能。
設(shè)計(jì)意圖: 通過“Re2分子內(nèi)共價(jià)鍵類型”“共價(jià)鍵斷裂與形成的真實(shí)過程”“穩(wěn)定的四重鍵為何會(huì)斷裂”三個(gè)學(xué)習(xí)活動(dòng)的設(shè)計(jì),層層深入,利用數(shù)據(jù)與核心知識(shí)層層推進(jìn),尋找證據(jù),有序推理,深度解構(gòu)該學(xué)術(shù)前沿問題探索情境的內(nèi)核與價(jià)值。
4.4 任務(wù)3: 化學(xué)鍵的轉(zhuǎn)變
[提問]根據(jù)圖8觀測(cè)可知,錸原子在電鏡上的黑點(diǎn)距離變小(無(wú)法測(cè)量N/A),錸原子軌道能否進(jìn)一步重疊,由四重鍵轉(zhuǎn)變?yōu)槲逯劓I?提出你的猜想并進(jìn)行實(shí)驗(yàn)?zāi)M。
[活動(dòng)與探究]錸原子在電鏡上的黑點(diǎn)距離變小的原因是什么?嘗試從電鏡視角進(jìn)行如下模擬實(shí)驗(yàn)(如表5): (1)推測(cè)Re2分子可能的運(yùn)動(dòng)形態(tài);(2)繪制運(yùn)動(dòng)形態(tài)的俯/側(cè)視圖。
[提供信息]模擬Re2與碳納米管相互作用的運(yùn)動(dòng)形態(tài)如圖9所示。
[生]從原子軌道重疊角度,如果錸原子核間距進(jìn)一步減小,極有可能是錸原子軌道進(jìn)一步重疊,轉(zhuǎn)變?yōu)槲逯劓I,但是受限于原子核以及電子之間的排斥,錸原子軌道無(wú)法進(jìn)一步重疊,四重鍵無(wú)法轉(zhuǎn)變?yōu)槲逯劓I。
[提問]根據(jù)圖10所示,Re2最終并入了錸原子簇,錸原子間作用力發(fā)生了什么變化?
[提供信息]單層錸原子簇排列情況的電鏡圖像如圖11。
[生]Re2分子并入錸原子簇時(shí),共價(jià)鍵轉(zhuǎn)化為金屬鍵,證據(jù)是單層的錸原子簇呈現(xiàn)單層晶體錸的密置層緊密排列。
設(shè)計(jì)意圖: 通過“化學(xué)鍵的轉(zhuǎn)變”兩個(gè)活動(dòng)與探究,進(jìn)一步學(xué)會(huì)尋找有效數(shù)據(jù)與核心知識(shí)建立有效關(guān)聯(lián),形成證據(jù),進(jìn)行合理的推理,得出化學(xué)鍵在一定條件下可以相互轉(zhuǎn)化的結(jié)論,向縱深處發(fā)展學(xué)生證據(jù)推理的化學(xué)學(xué)科核心素養(yǎng)。
4.5 任務(wù)4: 構(gòu)建探尋微觀化學(xué)鍵的奧秘分析模型
[師生歸納]從探尋微觀化學(xué)鍵的奧秘,帶領(lǐng)學(xué)生體驗(yàn)科研過程,運(yùn)用最新技術(shù)探尋化學(xué)模型的證據(jù)中抽提出基于證據(jù)推理構(gòu)建化學(xué)鍵模型的一般思路,從原子間作用力辨識(shí)、共價(jià)鍵的斷裂與形成、化學(xué)鍵的相互轉(zhuǎn)化三個(gè)視角構(gòu)建分析模型,如圖12所示。
設(shè)計(jì)意圖: 從學(xué)術(shù)探索情境抽提出核心知識(shí)并尋找證據(jù),建立知識(shí)與證據(jù)之間的邏輯關(guān)系,進(jìn)行演繹推理,建構(gòu)思維模型,從解決具體問題遠(yuǎn)遷移至解決更加開放、復(fù)雜的問題。
5 項(xiàng)目式教學(xué)效果及反思
本項(xiàng)目通過設(shè)計(jì)四個(gè)進(jìn)階的學(xué)習(xí)任務(wù),從學(xué)生已有的認(rèn)知出發(fā),以解決學(xué)術(shù)探索情境問題——“人類第一次觀察到化學(xué)鍵的斷裂與形成”為主線,精心設(shè)計(jì)探究活動(dòng),在問題解決過程中,形成基于證據(jù)推理構(gòu)建化學(xué)鍵的思維模型。學(xué)生在學(xué)習(xí)過程中獲得以下三個(gè)方面的成長(zhǎng)。
一是激發(fā)了主動(dòng)探究的欲望。以前對(duì)于學(xué)生來說,科學(xué)家正在做的事情高不可攀,總覺得科研工作神秘感特強(qiáng)。本項(xiàng)目帶領(lǐng)學(xué)生利用核心知識(shí)尋找證據(jù),有序推理,層層抽絲剝繭,最終實(shí)現(xiàn)了問題解決。實(shí)踐表明,精心設(shè)計(jì)挑戰(zhàn)性的學(xué)習(xí)任務(wù),不僅不會(huì)嚇跑學(xué)生,相反會(huì)激發(fā)學(xué)生內(nèi)在的學(xué)習(xí)動(dòng)力,引導(dǎo)學(xué)生像科學(xué)家一樣思考問題,從基于知識(shí)的教學(xué)走向基于發(fā)展學(xué)生化學(xué)學(xué)科核心素養(yǎng)的教學(xué)。
二是打破了知識(shí)之間的壁壘,實(shí)現(xiàn)了知識(shí)的結(jié)構(gòu)化。化學(xué)鍵由于概念抽象難以理解,因此在日常教學(xué)中教師們習(xí)慣將離子鍵、共價(jià)鍵、金屬鍵等基本概念用表格的形式進(jìn)行嚴(yán)格的區(qū)分,并讓學(xué)生強(qiáng)行記憶,這樣的結(jié)果是學(xué)生面對(duì)真實(shí)復(fù)雜情境的時(shí)候往往一籌莫展,解決問題的思路和方法過于僵化。學(xué)生在學(xué)習(xí)本項(xiàng)目之前,解答2017年海南卷第21題“結(jié)合SiX4的沸點(diǎn)和PbX2的熔點(diǎn)的變化規(guī)律(如圖13),可推斷: 依F、 Cl、 Br、 I次序,PbX2中的化學(xué)鍵變化趨勢(shì)”這一設(shè)問的時(shí)候,大部分學(xué)生找不到解決問題的角度,有少部分學(xué)生雖然找到解決問題的思路和方法,但又因?yàn)槿粘=虒W(xué)中教師對(duì)離子鍵、共價(jià)鍵的界限區(qū)分太嚴(yán)格,沒有勇氣從“化學(xué)鍵的離子性減弱、共價(jià)性增強(qiáng)”進(jìn)行闡述,嚴(yán)重阻礙學(xué)生創(chuàng)新思維的發(fā)展。創(chuàng)新的前提是知識(shí)的結(jié)構(gòu)化,即知識(shí)的有效融通,從知識(shí)的結(jié)構(gòu)化走向知識(shí)的功能化。怎么打通知識(shí)之間的壁壘,選擇一個(gè)適切的情境就顯得很有必要。本項(xiàng)目很好地從“化學(xué)鍵→化學(xué)鍵種類→共價(jià)鍵的斷裂→金屬鍵的形成”思路出發(fā),將真實(shí)情境問題解決與知識(shí)結(jié)構(gòu)化雙線并行,打通了學(xué)生的認(rèn)知壁壘,破除了前概念的束縛,實(shí)現(xiàn)了知識(shí)
的多點(diǎn)結(jié)構(gòu)向拓展抽象結(jié)構(gòu)進(jìn)階。
三是實(shí)現(xiàn)了知識(shí)的功能化向素養(yǎng)化的進(jìn)階。本項(xiàng)目實(shí)施后,通過“科學(xué)家合成聯(lián)苯烯(如圖14)”[6]之間的相互作用力分析,探查學(xué)生分析“物質(zhì)b之間可采取‘HF拉鏈’相互識(shí)別活化位點(diǎn)的原因”等問題的理解,實(shí)驗(yàn)班95%以上都能找到“電負(fù)性”與“靜電作用”并進(jìn)行有效關(guān)聯(lián),65%以上的學(xué)生從“共用電子,電子對(duì)偏向”的角度進(jìn)行準(zhǔn)確的闡述,而對(duì)照班的學(xué)生因?yàn)樵撉榫尺^于前沿,設(shè)問過于新穎,基本沒有角度或者思路,整個(gè)問題的難度陡然上升。通過對(duì)照實(shí)驗(yàn)說明在教學(xué)中引入前沿學(xué)術(shù)情境,實(shí)行“情境解構(gòu),模型建構(gòu)”雙線并行的教學(xué)策略在幫助學(xué)生形成認(rèn)知角度和認(rèn)識(shí)思路方面效果顯著。這也告訴我們,進(jìn)行教學(xué)設(shè)計(jì)的時(shí)候,不應(yīng)僅僅聚焦某個(gè)具體問題的解決,而要在具體問題解決的基礎(chǔ)上,抽提出解決一般問題的思路和方法,遠(yuǎn)遷移到更加真實(shí)、復(fù)雜、陌生的情境,實(shí)現(xiàn)知識(shí)的功能化向素養(yǎng)化發(fā)展。
參考文獻(xiàn):
[1]吳俊明. 芻議新階段我國(guó)基礎(chǔ)教育化學(xué)課程的發(fā)展走向[J]. 化學(xué)教學(xué), 2021, (7): 1~7.
[2]中華人民共和國(guó)教育部制定. 普通高中化學(xué)課程標(biāo)準(zhǔn)(2017年版2020年修訂)[S]. 北京: 人民教育出版社, 2020: 2, 90~91.
[3]Cao K., Skowron S.T., Biskupek J., et al.. Imaging an unsupported metal-metal bond in dirhenium molecules at the atomic scale [J]. Science Advances, 2020, 6(3): eaay5849.
[4]裴新寧, 鄭太年. 國(guó)際科學(xué)教育發(fā)展的對(duì)比研究——理念、主題與實(shí)踐的革新[J]. 中國(guó)科學(xué)院院刊, 2021, 36(7): 771~778.
[5]李曉明. 淺析化學(xué)教學(xué)中證據(jù)應(yīng)具有的“四性”[J]. 化學(xué)教學(xué), 2021, (7): 27~32.
[6]Qitang Fan, Linghao Yan, Matthias W. Tripp, et al. Biphenylene network: A nonbenzenoid carbon allotrope [J]. Science 2021, 6(3): 852~856.

