基于學科核心素養的初三化學微觀專題復習內容研究


摘要:教學要注重發展學生的學科觀念,專題復習更要注重培養學生的學科核心素養。文章基于“宏觀辨識與微觀探析”相結合的觀念,以初三化學中考復習課為例,對微觀專題復習內容進行研究。
關鍵詞:學科核心素養;初三化學;微觀;專題復習
2014年,教育部首次提出將組織研究各學段學生發展核心素養體系,明確學生應具備的適應終身發展和社會發展需要的必備品格和關鍵能力。在此新形勢下,教師在教學過程中不僅要高度重視提高學生的學習質量、學習成績,還要重視培養學生的學科核心素養。如此,才能有效提升學生的綜合素質。
化學核心素養是化學這門學科的本質素養,是學生在學習化學知識的過程中形成的解決生活中實際問題最有用的化學能力和思維。其實,在化學新授課教學中,并不缺少對學生邏輯思維、抽象概括能力、推理論證能力、分析問題和解決問題能力的訓練和培養。但是進入中考化學復習階段,如何利用有限的課堂時間提升學生的化學核心素養是我們化學老師關注的問題。
例如,“宏觀辨識與微觀探析”是化學學科重要的核心素養。它是從分子、原子層面對物質結構、性質、能量轉變等及其相互關系的基本認識,既是化學學科重要的觀念,又是化學問題解決的思維視角。將宏觀、微觀和化學用語、化學實驗聯系在一起是化學學科的特點。基于培養學生這一核心素養能力,提高微觀專題的復習課效率,筆者對這一專題的復習進行了如下研究。
一、 由表及里,從微觀角度認識物質組成
化學學科核心素養提出的五大素養之一“宏觀辨識與微觀探析”,要求學生既要有研究物質組成與性質的宏觀視角,也要有研究物質微觀結構的微觀視角,從而深化結構決定性質的學科思想。
【例1】(2009年南京市)下列各圖中“○”和“●”分別表示兩種質子數不同的原子,其中能表示由兩種化合物組成的混合物的圖是(B)
啟示:初中化學作為化學學科的啟蒙,首先就是從組成上學會認識物質。宏觀上,由不同種物質組成的是混合物;微觀上,不同種分子構成混合物。結合“宏觀辨識與微觀探析”這一核心素養,通過例1從微觀角度認識物質。
二、 從宏觀到微觀,復習化學反應的微觀實質
初中化學課程標準明確指出:學生應能夠認識物質的微粒性;知道物質是由分子、原子、離子構成的;它們之間在一定條件下能夠相互轉化;能用微粒的觀點解釋某些常見的現象。
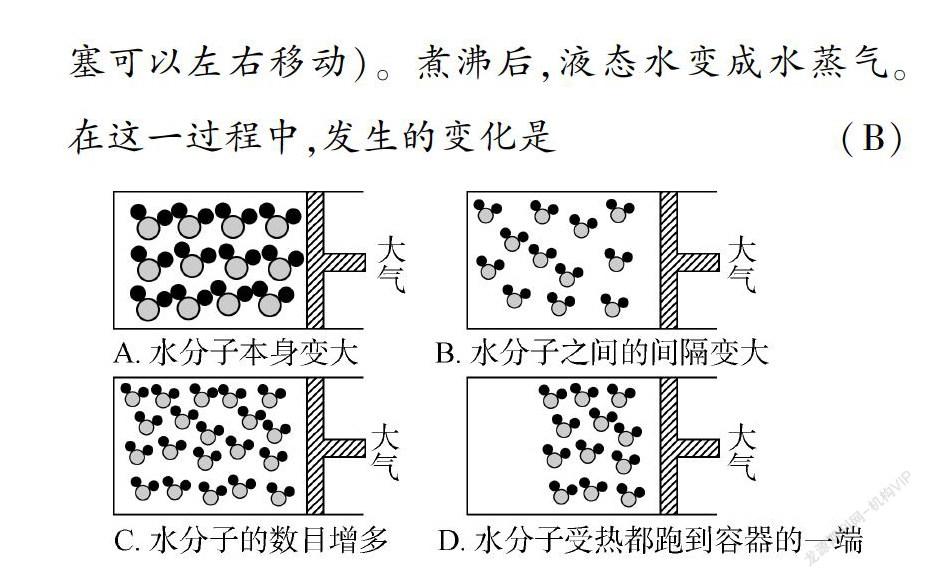
【例2】(2010年南京市)圖中表示封閉在某容器中的少量液態水的微觀示意圖(該容器的活塞可以左右移動)。煮沸后,液態水變成水蒸氣。在這一過程中,發生的變化是(B)
【例3】(模擬題)某化學反應的微觀示意圖為,關于該反應的說法正確的是(D)
A. 涉及五種物質B. 分子的種類不變
C. 屬于復分解反應D. 原子的種類不變
啟示:學生在人教版九年級化學第三單元課題1《分子和原子》中學過化學反應的微觀本質。由于“宏-微”相結合的學科特色,要求教師在新授課上反復與學生強調,所以學生在課堂上能夠較為容易地說出化學反應的微觀本質是分子分解成原子,原子重新組合構成新的分子或者原子也可以直接構成新物質。
三、 從理論到實踐,畫出化學反應的微觀過程
學會運用符號表示物質及其變化是“宏微結合”這一化學核心素養的具體要求。課堂內容可設計為根據九年級化學教材P50頁圖3-6和圖3-7,結合化學反應的微觀實質,要求學生畫出上述兩個反應的微粒變化具體過程。
【例4】根據下圖,寫出反應的方程式并畫出微觀反應過程。
基于學科核心素養的初三化學微觀專題復習內容研究
啟示:對于這樣的課堂練習,學生顯然非常感興趣,畫得不僅整潔、美觀,更為重要的是在練習中強化理解了具體化學反應的微觀過程,能夠較好的形成物質的微粒觀,從而理解化學變化的微觀本質。
【例5】(2020玄武二模)建立“宏觀—微觀”間的聯系,是化學學習的重要方法。我國科學家研究二氧化碳和氫氣在催化劑、加熱條件下可轉換為化工原料乙烯(C2H4),其反應微觀過程如下圖所示。
請寫出該反應的化學方程式2CO2+6H2催化劑△C2H4+4H2O。
啟示:通過本題強化訓練,學生對化學學科的特色題目“宏—微—符”會有較全面的理解,從表象到整合的應用,能夠在培養學科觀念的同時較為完整地構建解題的一般思維模型。
四、 透過現象看本質,深入理解復分解反應的發生條件
復分解反應是學生在酸堿鹽這一部分知識中學習的四大基本反應類型之一。復習時,教師需注意引導學生將知識進行歸納、總結,并在此基礎上深刻理解復分解反應的發生條件以及反應的實質,從而能夠自主建構完整的知識體系。其實,復分解反應的本質同樣可以用微粒的觀點進行理解,而且,學生在化學反應的微觀本質基礎上認識復分解反應的實質,能夠使問題變得更加簡明和清晰,減輕學生的理解負擔。為了達到復習目標,進一步培養學生的“宏觀辨識與微觀探析”的化學核心素養,設計如下例題。
【例6】
學生反饋圖2
該反應的實質是:H++OH-H2O。
【例7】(2020鼓樓一模)初中化學中,我們學習了稀鹽酸和氫氧化鈉溶液(如上圖所示)發生中和反應的實質是:H++OH-H2O,像這種用實際參加反應的離子符號來表示反應的式子叫離子方程式。以稀鹽酸和氫氧化鈉溶液反應為例,離子方程式的書寫一般按以下步驟:
Ⅰ. 寫出稀鹽酸與氫氧化鈉溶液反應的化學方程式HCl+NaOHNaCl+H2O;
Ⅱ. 把易溶于水且易電解的物質寫成離子形式,把難溶的物質、氣體和水等仍用化學式表示。上述方程式可改寫成:H++Cl++Na++OH-Na++Cl-+H2O;
Ⅲ. 刪去方程式兩邊不參加反應的離子,繼續改寫成:H++OH-H2O;
Ⅳ. 檢查方程式兩邊各元素的原子個數和電荷總數是否相等。則稀鹽酸和氫氧化鈉溶液反應的離子方程式為:H++OH-H2O。請回答:
(1)寫出稀鹽酸和碳酸鈣發生反應的離子方程式:2H++CaCO3Ca2++H2O+CO2↑;
(2)酸、堿、鹽在水溶液中發生的復分解反應實質上就是兩種化合物在溶液中相互交換離子的反應,生成物中有水或氣體或沉淀生成時,復分解反應才可以發生。
啟示:酸、堿、鹽在溶液中發生的反應大多為復分解反應,可以通過明顯的現象觀察到反應的發生,比如產生氣泡或者生成沉淀。有些不明顯的反應也可借助指示劑顏色的變化等讓學生較為直觀的感受到。那么宏觀現象中隱藏的微觀實質究竟是什么呢?從肉眼看不見的離子、分子或原子等角度對復分解反應的實質進行微觀解釋,這也是“宏微觀結合”最典型的例子之一。透過顯性的外在現象發掘事物發展的隱性本質,確實是需要傳授給學生的學科核心素養。
學生通過這一節化學微觀專題的學習,能夠由淺入深地理解物質的微粒觀并做到熟能生巧的運用。一方面對中考必考知識有了更為深刻的理解和掌握,另一方面在復習中更好地培養和提升自己的化學學科素養,如此,才真正達到了本節課的學習目標。
學科核心素養在某種程度上表明了新形勢下化學學科的教學目標、育人要求,將化學知識轉化為一種具體的能力用以解決生活、工作和學習中的具體問題。基于化學學科核心素養之一“宏觀辨識與微觀探析”的專題學習,其核心目標要求教師能夠對學生實現從“獲取知識”到終極目標“必備品格和關鍵能力”的培養。對于化學這門學科來說,教師要通過有效的教學方法,讓學生對化學學習產生興趣,并且在學習化學知識的過程中掌握化學思維和能力,從而提升學生的綜合素養。
參考文獻:
[1]尹歡歡,高曉瑩,吳春峰.指向宏微結合觀念建構的化學智慧課堂[J].化學教與學,2020(11):49-52.
作者簡介:
季曉春,江蘇省南京市,南京市金陵中學岱山分校。

