新解“金屬與鹽溶液的置換反應”
摘 要:“金屬的化學性質”是初中化學第八單元的核心內容.金屬與鹽溶液的化學反應,是金屬化學性質的重要體現,因此在各個大型考試中必然出現,但題目的難度較大.在教學中,學生的解題方法大多是按一定的“程序”,即將反應的各種情況一一羅列出來,解題過程繁瑣.現嘗試提出新的解題方法,旨在于響應“雙減”政策,減輕學生的課業負擔.
關鍵詞:解題;金屬;鹽溶液;初中化學
中圖分類號:G632 文獻標識碼:A 文章編號:1008-0333(2023)17-0113-03
收稿日期:2023-03-15
作者簡介:張欣(1983-),女,湖北省武漢人,本科,中學一級教師,從事初中化學教學研究.
1 金屬與鹽溶液的化學反應
金屬的化學性質包括金屬與氧氣反應、金屬與酸溶液的反應、金屬與鹽溶液的反應.金屬與酸溶液的反應、金屬與鹽溶液的反應在基本反應類型上均屬于置換反應,但金屬與鹽溶液的反應則因其多樣性更能考查學生能力,故而頻繁出現在各大考試中.在日常教學中,將課本內容簡化為活動性強的金屬可以置換出活動性弱的金屬,學生在單一反應的題目中均有較高的正確率.但近年來的考試中會涉及到多個反應,解題時還需同時考慮反應順序的問題,因此成為考試中的難點.在多個反應中,最活潑的金屬會最先將最不活潑的金屬置換出來.同樣,如果將活動性不同的幾種金屬加入到一種鹽溶液中,最活潑的金屬會先發生反應.學生在教學中會按照上述結論將解題程序化.以下舉兩個例子,分別對應一種金屬兩種鹽和兩種金屬一種鹽的反應。
例題1 在Fe(NO3)2、Cu(NO3)2的混合溶液中投入一定量的鋅粉,充分反應后得到濾渣和濾液.關于濾渣和濾液的下列說法中,正確的是().
A.濾渣中一定有銅和鐵
B.濾渣中一定有銅,可能有鐵
C.濾液中一定為淺綠色
D.濾液中不可能有三種溶質
例題2 將一定質量的Al和Fe的混合粉末加入AgNO3溶液中,充分反應后得到濾渣和濾液.關于該濾渣和濾液的下列幾種說法中,正確的是().
A.在濾渣中加入稀硫酸,一定有氣泡產生
B.濾渣中一定含有Ag
C.在濾液中加入稀鹽酸,一定有白色沉淀產生
D.濾液中一定含有Fe(NO3)2和Al(NO3)3,一定不含AgNO3
2 教學常見解法
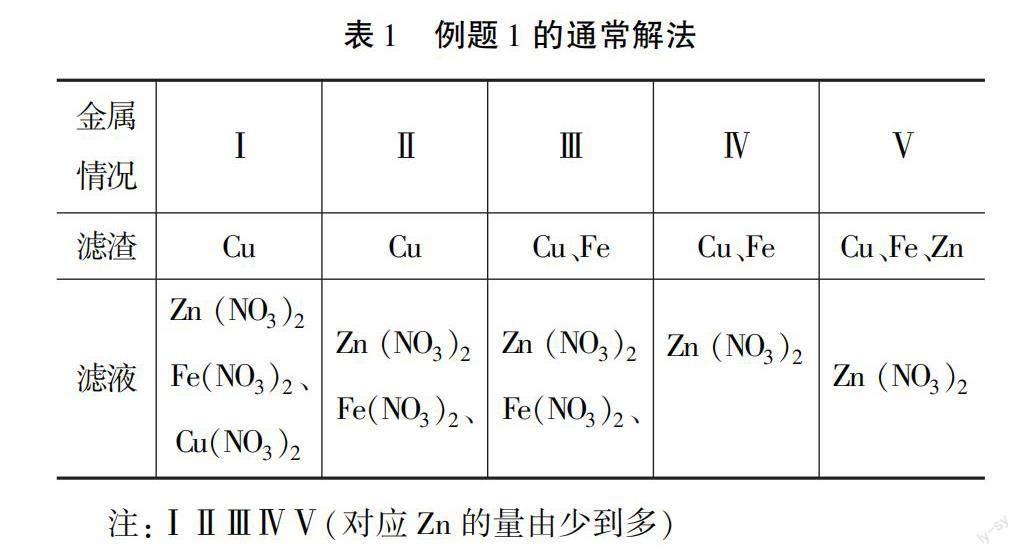
例題1中由于鋅粉的量為“一定量”,在化學上包括有少量、適量、過量的幾種情況,因此對于此類問題,在以往聽課的過程中,教師教授學生根據鹽溶液中的金屬的活潑程度按從小到大排列(考慮反應的先后順序),然后根據各自的量對各自的濾渣和濾液進行羅列,最后按照結果將題目的選項一一比對.如對于以上例題,通常解法見表1.
A.錯誤.濾渣中不一定有鐵,如情況Ⅰ、Ⅱ;B.正確;C.錯誤.濾液可能為無色,如情況Ⅳ、Ⅴ;
D.錯誤,如情況Ⅰ.
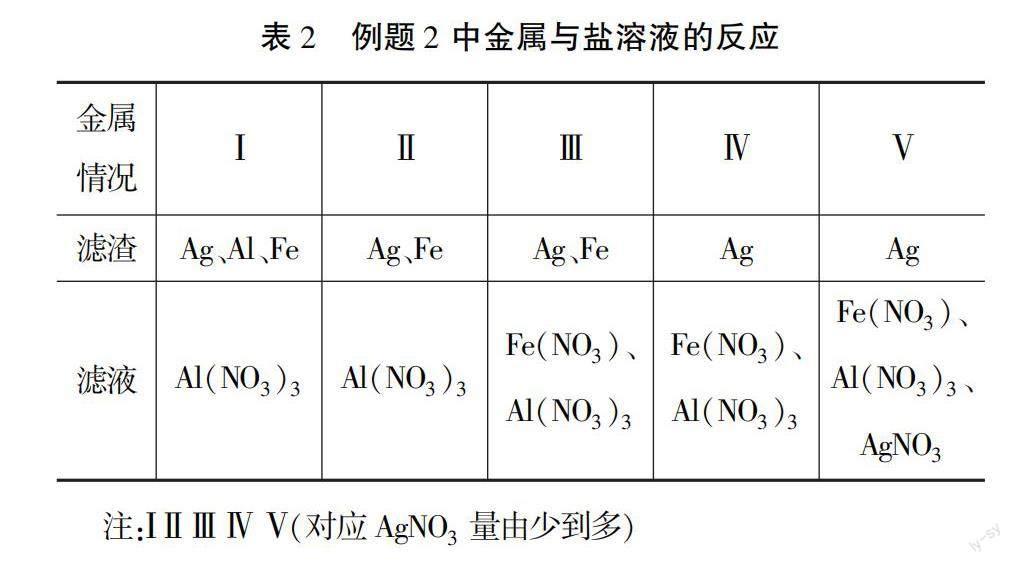
而對于例題2將金屬按活潑程度排列,與鹽溶液反應(見表2).
A.只有在濾渣中存在活潑金屬的情況下,加入酸溶液才可能會產生氣泡,而情況Ⅳ、Ⅴ在濾渣中加入酸溶液均不可能產生氣泡,錯誤;B.正確;
C.只有在溶液中存在有硝酸銀時,加入稀鹽酸才可能產生沉淀,而只有情況Ⅴ才符合,錯誤;
D.看分析,濾液中的溶質一定含有Al(NO3)3,其余兩種均為可能產生,錯誤.
從上述過程可以看出這樣的解法,除了要掌握多個置換反應發生的先后順序規律外,還要能夠正確分析出每一種情況對應的濾渣濾液情況,這對于優生問題不大,因為他們理解到位,基礎扎實,思路清晰;但對于大部分普通學生而言,無論是作業中還是考試中,都需要花費較多的時間,影響學生的成績.在實際的教學過程中,教師也發現這類學生往往會有“聽得懂,不會做”的困惑.
3 新的解題思路
在現在的考試中,也已經不滿足于一種金屬、兩種鹽的情況,出現了多種金屬與多種鹽反應的情況,且題目通常描述為“一定量”(如上述例題),因此一一羅列的情況會更加復雜.已知金屬反應的先后順序由金屬的活動性順序決定,可以引導學生仔細想想為什么題目中濾渣和濾液的成分有“一定”“可能”的區別呢?通過對上述解題的圖表分析出某些物質一定存在,這是因為某個反應確定發生了,那么該反應的產物一定會存在于相應的濾渣或濾液中,但其反應物是否發生完全,無法確定(但兩種反應物不能同時存在);而某些反應無法判斷其是否發生,則該反應的產物只能是可能存在于相應的濾渣或濾液中(發生了就存在,不發生就不存在).
這里仍以前文例題為例說明此思路:
例題1整個反應涉及三種金屬,其金屬的活動性順序排列為Zn>Fe>Cu,
所以無論金屬量多量少,一定發生的化學反應是:
Zn+Cu(NO3)======2Cu+Zn(NO3)2
因此在濾渣里一定有金屬Cu,濾液里一定有Zn(NO3)2.
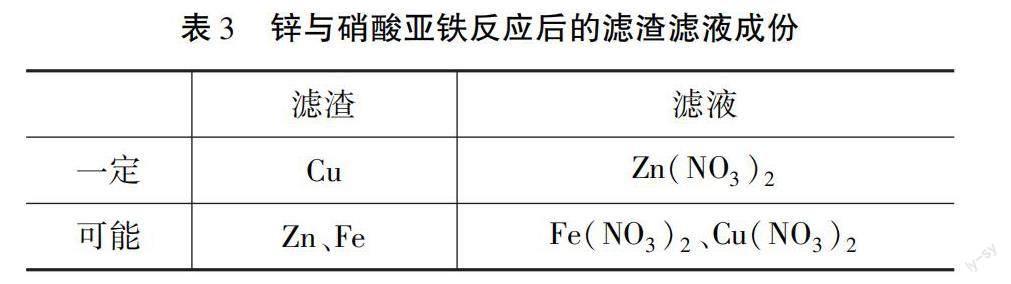
而鋅是否與硝酸亞鐵反應不確定,其產物鐵可能存在于濾渣中,則對于反應后濾渣濾液的成分判斷見表3.
因此,例題1中只有選項B正確.
通過觀察能發現,錯誤的選項在設置上主要是將因為無法判斷是否發生反應而不能確定的物質描述為一定存在,或將能確定發生了反應一定存在的物質描述為可能存在,根據以上的方法,這個題目的解題過程就會相當地簡單快速.
對于例題2中的兩種金屬與一種鹽反應的情況也同樣適用.
例題2中同樣涉及三種金屬,其金屬的活動性順序為Al>Fe>Ag,
因此在過程中一定發生的化學反應為:
Al+3AgNO3=======3Ag+Al(NO3)3
由上述反應可以得出在濾渣中一定含有Ag,而在濾液里一定有Al(NO3)3(見表4).
A.濾渣中有活潑金屬加酸才可能有氣泡,而鋁和鐵只是可能存在,錯誤;B.正確;C.AgNO3只是可能存在,因此只能說可能產生沉淀,說法錯誤;
D.濾液中能確定一定存在的只有硝酸鋁,說法錯誤.
無需列舉所有情況,只需根據活動性順序就可以解題.對于更復雜的情況,例如前文中提到多種金屬與多種鹽的反應,如果用原有的方法,因為反應多,幾乎羅列所有情況.
例題3
某廢液中含有硝酸銅和硝酸銀,向該廢液中加入一定量的鋅粉與鋁粉,充分反應得到濾渣和濾液,關于濾渣與濾液的下列說法中正確的是().
A.若濾液為無色,則濾液中可能含有三種溶質
B.若向濾液中滴加氯化鈉溶液產生白色沉淀,則濾渣可能是混合物
C.若濾渣中含有三種金屬組成,則濾液可能呈藍色
D.若向濾渣中滴加稀硫酸無氣泡冒出,則濾液中可能含有兩種陽離子
如何按新的方法解題呢?先按上述解法:
整個反應涉及四種金屬,其金屬的活動性順序為Al>Zn>Fe>Cu,
所以在整個過程中一定發生的一個反應是:
Al+3AgNO3======3Ag+Al(NO3)3
即無論金屬量多量少,該反應一定是發生了,因此在濾渣里一定有Ag,濾液里一定有Al(NO3)3.
但選項中還包括了新的條件,如A選項中溶液的顏色等.新的條件給出的目的是為了說明還有哪些反應是確實發生了,發生到了哪個程度,或者哪些物質是還沒有反應.
如選項A中描述濾液為無色,說明溶液中的硝酸銅也已經完全發生了反應,硝酸銀也已經反應完,則濾液中一定沒有硝酸銅和硝酸銀,一定有硝酸鋁,而其他物質無法確定,故濾液中最多含有硝酸鋁和硝酸鋅兩種物質.
選項B中向濾液中滴加氯化鈉溶液產生白色沉淀,說明濾液中還有硝酸銀剩余,則說明能與硝酸銀反應的金屬都已經反應完全,且硝酸銅沒有發生反應,因此固體中只有銀,是一種純凈物,錯誤.
選項C若濾渣由三種金屬組成,根據活動性順序,出現的金屬為銀、銅和鋅.活潑金屬鋅剩余,說明硫酸銅已經完全與鋅發生了反應,故溶液不可能為藍色,錯誤.
選項D若向濾渣中滴加稀硫酸無氣泡冒出,說明活潑金屬均已反應完,再根據前面提示可知濾渣中一定有銀,可能有銅,一定沒有鋅和鋁,濾液中一定有硝酸鋁和硝酸鋅,其余成分均為可能存在,溶溶液中陽離子可能含兩種或更多,正確.
4 方法總結
該方法要求首先理解金屬的活動性順序,然后根據活動性順序判斷一定發生的反應,則可以首先推出一定有的濾渣和濾液成分,其余成分均為可能含有,避免多次列舉耗費時間;若題目有更多的條件,則同樣根據題目給定的條件來判斷一定發生的反應還有哪些,再考慮一定有的濾渣和濾液成分,而對于無法判斷的反應,其濾渣和濾液成分只能表述為可能存在.簡化解題的步驟,避免學生機械化地重復模仿,將更多地思考還給學生,使學生能真正理解金屬的活動性順序對于反應順序的影響,促進學生對化學知識的理解和思考,提升學生的解題效率.
參考文獻:
[1]張春霞.金屬與鹽溶液反應類型題目的解題技巧[J].數理化學習(初中版),2013(04):49-50.
[2] 魯欣.淺談金屬活動性順序的探究[J].中學課程資源,2015(05):56.
[3] 龍曉輝.“金屬與鹽溶液反應后成分判斷”解法新探[J].數理化解題研究,2021(11):82-83.
[責任編輯:季春陽]

