“苯酚”的教學再設計
魏良怡 劉敏

摘要:通過生活中的藥品和知識回顧引入苯酚的概念,運用“基團間相互作用”的思路分析苯酚的結構和預測苯酚的化學性質,設計環環相扣的實驗來探究和驗證苯酚的性質,利用比較法引導學生學習知識間的相互聯系,努力培養學生學習有機物的分析能力、推理能力、觀察能力和應用能力。
關鍵詞:苯酚;基團間相互作用;有機物性質;實驗探究;教學設計
文章編號:1008-0546(2016)09-0063-06 中圖分類號:G633.8 文獻標識碼:B
doi:10.3969/j.issn.1008-0546.2016.09.023
一、設計思路
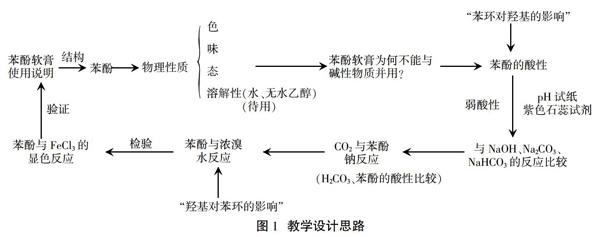
本節課總體設計思路為“結構決定性質,性質決定用途,用途反映結構”。“用途”是指生活中的藥品苯酚軟膏,“結構”是指“苯酚基團間的相互作用”。以藥品引入、分析苯酚結構、預測反應、設計實驗方案、分組和演示實驗并進行驗證。本節課的設計思路如圖:
目前,研究苯酚的教學多是集中在結構決定性質的單一角度,或由用途引入問題,用實驗探究苯酚的性質[1],縱然有研究“基團間相互作用影響有機物性質”的一般思路和方法[2],但未形成較完整的教學設計,并未應用于課堂教學中。筆者將此教學設計應用于課堂教學,教學完成后進行反思和改進,形成最終的教學設計,具有“實踐性”的說服力。在教學過程中,一方面讓學生通過實驗探究學習苯酚的性質和有關化學知識,另一方面引導學生樹立正確使用化學藥品的科學觀。讓學生在學習中能夠辯證地看待化學與生活的關系,這正是我們學習化學和使用化學的目的。
二、教材及學情分析
在蘇教版選修3《有機化學基礎》的設置來看,“酚的性質和應用”被安排在“醇”之后,學生已經學過“苯和苯的同系物性質”。學生在學習“乙醇和鈉的反應”內容中已初步掌握了官能團對有機物性質的影響,對乙醇中羥基的結構特點和斷鍵方式有了一定的了解[3]。在“甲苯與濃硝酸反應”的內容中已學過甲基對苯環的定位效應,在“苯酚”教學中運用類比的方式預測羥基對苯環也有類似的定位效應。類比假設與實驗探究相結合,不僅可以幫助學生形成前后聯系的完整知識體系,還能培養他們的推理、實驗、觀察、分析、應用的能力,這為以后學習羧酸和酯的性質提供較好的學習方法。
三、三維目標
1. 知識與技能
①掌握苯酚的分子結構、物理性質。
②通過實驗掌握苯酚的化學性質及檢驗方法。
③了解苯酚在日常生活及工農業生產中的重要作用。
2. 過程與方法
通過實驗培養動手能力、觀察和對實驗分析的能力,并形成自主探究、合作學習的良好習慣。
3. 情感態度價值觀
通過實驗探究培養實事求是的科學態度,同時通過“結構決定性質”的分析,加深對辯證唯物主義觀點的理解。
四、教學過程
1. 引入
【實物展示】這是我們生活中使用的“水楊酸苯酚軟膏”,它主要用于治療手足皮癬病。這是它的說明中的注意事項,其中有這樣幾條值得我們關注一下(如圖2,橫線)。苯酚與我們的生活息息相關,它有什么樣的結構、性質、用途?這節課我們一起來學習苯酚。
【知識回顧】 我們在有機化合物的分類中已經認識了醇和酚,二者都含有官能團羥基。下面兩個物質哪個屬于醇類?哪個屬于酚類?(圖3)
【生】甲屬于醇類,醇指烴分子中飽和碳原子上的氫原子被羥基取代形成的化合物。乙屬于酚類,酚指分子中羥基與苯環(或其他芳環)碳原子直接相連的有機化合物。
【師】回答得非常好。醇類和酚類物質都含有官能團羥基,但羥基的位置不同,酚是在裝純(醇)!(傳來一片笑聲)
【設計意圖】從生活中的藥品“水楊酸苯酚軟膏”的說明書引入情景,激發學生對生活中的物質進行探究的興趣和愿望。讓學生利用已學過的知識對兩個同分異構體進行判斷,何為醇類?何為酚類?將生活和知識相結合,達到“溫故而知新”、“學以致用”的目的。
2. 苯酚的結構
【師】(PPT投影)。這是苯酚的球棍模型和比例模型(圖4),請同學們寫出苯酚的分子式、結構簡式。(藍色為碳原子,白色為氫原子,紅色為氧原子)
【設計意圖】直觀地展示苯酚的結構,寫出苯酚的分子式和結構簡式。培養學生運用化學術語進行表達的能力。
3. 苯酚的物理性質
【過渡】 在我們的實驗桌上的試劑瓶中裝有苯酚藥品,請同學們看一看、聞一聞,并進行投影中的探究實驗,觀察實驗現象,與小組同學討論并總結苯酚的物理性質。
【PPT投影】苯酚的物理性質(小組實驗)
【生】 小組匯報實驗結論,并總結苯酚的物理性質。
【師】 我們可以根據苯酚的物理性質解釋一下苯酚軟膏說明書中的兩個注意事項了:
① 為何用后需擰緊瓶蓋,注意避光?
② 若身體局部有不適,應立即停藥,用什么藥物洗凈?為什么選擇它呢?
【生】①苯酚容易被空氣中的氧氣氧化而變質。
②可以用酒精擦洗,因為苯酚易與有機溶劑互溶。
【設計意圖】通過小組探究實驗,讓學生從色、味、態、溶等角度去看一看、聞一聞、試一試、比一比,全面了解苯酚的物理性質。引導學生學會研究物質物理性質的一般方法,培養學生實驗操作能力。通過實驗現象,總結苯酚的物理性質,老師又從“苯酚軟膏說明書中的兩個注意事項”出發,讓學生學會思考問題和解決問題,達到“學以致用”的目的。這樣的設計擺脫了課堂中一貫的平鋪直敘地描述物質物理性質的弊端。
【師】 在苯酚軟膏使用中,它不能與堿性藥物并用。那苯酚的酸堿性如何?
【生】 可能呈現酸性。
【師】為何苯酚可能具有酸性?如何檢驗苯酚的酸性?苯酚的酸性強弱如何?想要知道這些,我們先從苯酚的結構著手分析一下!
【設計意圖】從說明書中的注意事項出發,推測出苯酚可能具有酸性。苯酚的酸性需要通過化學實驗來驗證和探究,而此時從物質的“用途”體現物質的“結構”的思想,利用有機物分子中“官能團相互作用”的原理對苯酚的結構進行分析,從物質的“結構”決定了物質的“性質”的思想,為下面探究苯酚的化學性質做好鋪墊,此處起到了承上啟下的作用。
4. 苯酚的化學性質
【PPT投影】
【師】 由兩個基團組成,“—OH”(羥基)和“苯基”。它與乙醇和甲苯的結構有相似之處但又有本質區別。乙醇可以與鈉反應,鈉與乙醇分子中羥基中的氫原子置換出氫氣,苯酚可以與鈉反應嗎?甲苯中苯環與—CH3(甲基)相互影響:苯環使甲基上的氫原子活化,使得甲苯容易被酸性KMnO4氧化而使其褪色;甲基的引入也活化了苯環,使得苯環上甲基的鄰對位上的氫原子比較活潑,當甲苯與濃硝酸發生硝化反應時得到的主要產物為2,4,6-三硝基甲苯。那么,苯基與羥基之間是否存在相互作用呢?我們首先探究苯酚與鈉是否反應,以此展開苯酚化學性質的探究。
(1) 苯酚與鈉反應
【生】小組實驗(苯酚與鈉反應)
【板書】
【設計意圖】 通過苯酚與鈉反應和乙醇與鈉反應的實驗對比,探究苯環對羥基的影響。利用“有機物基團間相互作用”的思路,引導學生觀察對比兩者的反應速率,從而證明了苯環對羥基的影響。苯酚的乙醇溶液與鈉的反應速率快于乙醇與鈉反應,說明苯酚中羥基H比乙醇中的羥基H活潑,證實了推測苯環對羥基起到了活化作用。此處由“結構推測”,再通過實驗驗證性質,運用了“結構”決定“性質”的思想。
(2)苯酚的酸性
【過渡】我們從反應方程式中可以看出,鈉將苯酚羥基上的氫原子置換出來生成氫氣,說明苯環對羥基上的氫原子作用,使其電離形成自由的氫離子,我們可以寫出苯酚的電離方程式。由此可以看出苯酚呈酸性,它還有個俗名叫“石炭酸”。
【板書】
【師】 根據這一性質我們就可以解釋說明書中的注意事項“不能與堿性藥物并用”了。我們有哪些方法檢驗溶液的酸堿性呢?
【生】 可以用pH試紙檢驗,紫色石蕊和酚酞指示劑,與堿和鹽反應等等。
【師】 同學們回答得非常好,我們通過實驗來驗證一下吧!
【師】 演示實驗(圖6)。
【設計意圖】通過pH試紙和紫色石蕊試劑驗證苯酚的酸性,由實驗檢驗理論的推斷,能培養學生的思考能力、判斷能力和探究能力。
【師】通過pH試紙的比色卡對比,苯酚的pH大約5左右,但紫色石蕊試劑沒有變色,如何評價苯酚的酸性呢?
【生】它是弱酸!
【師】苯酚的酸性很弱,我們可以通過實驗來“體會”這個“弱”字!
【生】小組實驗(苯酚的酸性)
【師】我們通過堿(NaOH)、鹽(NaHCO3和Na2CO3)與苯酚反應探究苯酚的酸性,它能與NaOH、Na2CO3反應,體現了酸的通性,但根據強酸制取弱酸的原理,我們并未觀察到氣泡,即無CO2氣體生成。而從實驗7的結果可以判斷苯酚與NaHCO3沒有發生反應。這些實驗現象告訴我們苯酚酸性真的是很“弱”啊!那么請大家根據苯酚的電離原理和實驗現象寫出苯酚與NaOH、Na2CO3反應的方程式。
【板書】
【師】 如果將CO2氣體通入到苯酚鈉中會有什么現象呢?
【師】 演示實驗(CO2與苯酚的酸性強弱比較)
【生】 溶液變渾濁了!
【師】 說明CO2與苯酚鈉溶液反應生成什么了呢?請大家用反應方程式說明。
【板書】
【師】由此請大家比較HCl、H2CO3、苯酚、NaHCO3的酸性強弱大小
【生】HCl > H2CO3 >苯酚> NaHCO3
【設計意圖】 通過苯酚酸性的檢驗,根據酸的通性,利用強酸制取弱酸的原理,對苯酚的酸性之“弱”展開探究和討論,在分組實驗和演示實驗中,讓學生能認識到“弱”的意義。
(3)苯酚與濃溴水反應
【過渡】 從上面的實驗我們知道:“苯環”對“-OH”的影響是增強了羥基“H”的活性,使得羥基“H”更容易電離成H+,這才使苯酚呈弱酸性。苯環上—CH3(甲基)的引入使其鄰對位較活潑,那么“-OH”對苯環有沒有類似的影響呢?
【師】 苯和溴水不發生反應,在催化劑作用下,苯與液溴才發生反應,我們比較一下苯酚與濃溴水反應(圖8和表4)。
【師】:白色不溶于水的沉淀物是2,4,6-三溴苯酚。該反應速率快且能定量完成,工業上常用于對溶液中的苯酚進行定性和定量測定。
【板書】
【設計意圖】根據“基團間相互作用影響”的思路:苯環對羥基的影響,使羥基氫原子電離成H+;羥基對苯環的影響,是否跟甲苯類似,具有鄰對位的定位效應。將“苯酚與濃溴水”的實驗與已學過的“苯與液溴”的實驗進行對比,從反應試劑、反應條件、反應速率、生成物、取代氫原子數五方面定性地比較,得出羥基對苯環也具有相同的定位效應。
(4) 苯酚的顯色反應
【師】由于濃溴水有較大的毒性,在使用時要考慮環保的問題。在工業上還有更靈敏的試劑檢測苯酚,且它無毒,它就是三氯化鐵。三氯化鐵與苯酚溶液會迅速的反應而呈紫色,該顯色反應非常靈敏,常用于工業廢水中酚類物質的檢驗。我們這節課的探究目的是水楊酸苯酚軟膏中苯酚的性質,那我們用顯色反應來檢驗一下它吧,看看有什么現象發生。(圖9)
【生】哇,紫色的溶液!
【設計意圖】利用苯酚與氯化鐵的顯色反應,檢驗課堂中引入的“道具”水楊酸苯酚軟膏。以生活中的實際問題為切入點,再利用學習的化學知識應用到生活中去,此處啟發學生的思維,注重學生的實踐,這是我們學習化學知識的重要目的。
5. 苯酚的用途
【材料1】苯酚是一種重要的有機合成原料,苯酚還有很多工業用途:醫藥、防腐劑、染料、合成香料、合成纖維、消毒劑、制備酚醛樹脂等等。
【材料2】苯酚的廢水對環境造成嚴重的污染,日本利用蟹殼清除工業苯酚廢水。
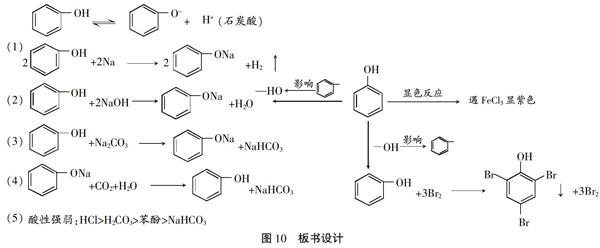
6. 板書設計
7. 作業布置
①只用一種試劑把下列四種無色溶液鑒別開:苯酚、乙醇、NaOH、KSCN,現象分別怎樣?
②怎樣分離苯酚和苯的混合物?
③查閱有關處理酚類廢水的資料,了解工業上處理廢水的常用方法,寫一份關于解決酚類污染的調研報告。
五、教學反思
1. “從生活走向化學,從化學走向生活”
本節課從“水楊酸苯酚軟膏的說明書”創設情境,從“酚”的定義著手,展示苯酚的結構,通過“基團間相互作用”的思想分析苯酚的結構,讓學生感覺苯酚“似曾相識”但有不同。老師引導學生提出的問題和學生分組實驗的探究活動均體現了學生是學習主體的思想。本節課最大的特色是以理論指導實驗,以實驗探究為手段,層層深入,處處鋪墊,環環相扣,讓學生參與實驗探究,主動地吸收知識,符合認識認知規律[4]。在學習了苯酚這節課的內容后,能讓學生辯證地看待化學藥品的使用,讓學生在學習中體會到學習化學的意義[5]。
2. 不足和改進之處
本節課的教學目標明確,教學過程的開展按教學設計很好地進行,基本達到預期的效果。學生參與課堂的積極性很高,師生互動和生生互動也較多。但學生們的實驗操作不太嫻熟,出現了不少問題如:1mL不知取多少;滴管伸進了試管中;加入藥品的量太過量;pH試紙不知如何使用等等,這些都需要以后實驗課進行糾正。另外,本節課的實驗內容較多,課堂容量大,上課時間緊湊,需要更好地提煉語言、合理安排組織實驗。從這節課中我還學習到:在以后的教學中,應該多調動學生的積極性,多培養學生的實驗設計能力、分析推理能力,確保更好地完成課堂教學。
參考文獻
[1] 李春燕,李發順. 從苯酚軟膏說起—“苯酚的性質和應用”教學與思考[J]. 化學教育,2014,(17):8-12
[2] 張麗麗,徐敏. 促進學生對“有機物分子內基團間相互作用”認識的教學研究—以“苯酚”教學為例[J]. 化學教學,2015,(6):46-49
[3] 白金有. 苯酚教學設計[J]. 中學化學教學參考,2015,(2):37
[4] 葉長軍. 新理念下的“苯酚”的教學設計[J]. 化學教學,2007,12:43-45
[5] 劉光影,錢勝. 平常、平實而不平庸—2014年全國高中化學優質課觀摩之“苯酚”說課[J].化學教與學,2015,(7):29-31

