基于物質轉化觀的教學新思考
馬媚媚

摘要:梳理元素化合物的教學(以鐵及其化合物為例)的相關文獻,文獻中呈現的教學案例都能注重核心知識的教學和發展學生的思維能力、科學探究能力。文章試圖從情境教學、學科理解和實驗細節三個方面闡述對物質轉化教學的一些新的思考。
關鍵詞:物質轉化;情境教學;科學精神;學科理解
文章編號:1008-0546(2022)07-0014-03中圖分類號:G632.41文獻標識碼:B
doi:10.3969/j.issn.1008-0546.2022.07.003
“物質轉化觀”是化學學科觀念之一,化學的核心問題是物質及其相互轉化。《普通高中化學課程標準(2017年版2020年修訂)》(以下簡稱“新課標”)在主題2“常見的無機物及其應用”中要求“結合實例認識金屬、非金屬及其化合物的多樣性,了解通過化學反應可以探索物質的性質、實現物質的轉化,認識物質及其轉化在促進社會文明進步、自然資源綜合利用和環境保護中的重要價值”[1]。在教學中以典型的元素及其化合物為代表,學習物質的性質、轉化、制備、檢驗、除雜及應用等內容,學生不僅可以探尋物質及其轉化的基本規律,還可以學習相關概念原理知識,建構物質及其轉化的科學理論,同時提高實驗探究能力。
高中化學必修1 的“鐵及其化合物”這一內容是非常典型的元素化合物課型,也是非常典型的氧化還原反應的重點課。筆者對近十年的核心期刊文獻中關于“鐵及其化合物”的課堂實踐研究發現,在教學中教師都能借助真實情境素材開展系列的探究活動,教學的核心知識都是 Fe2+、Fe3+的檢驗及 Fe2+和 Fe3+的相互轉化。從學科的角度再來思考這節課,有很多新的想法與大家分享。
一、情境教學的思考
在教學中需要創設真實的情境,讓學生在真實的情境中來解決具體的化學問題,教師設計真實情境下不同層次的問題,來引導學生進行實驗探究、討論交流等活動,找出解決問題的方法,促進學生思維的發展。
新課標中給出了許多鐵及其化合物的情境素材建議,如:補鐵劑;實驗室中硫酸亞鐵的保存與使用;印刷電路板的制作;打印機(復印機)使用的墨粉中的鐵的氧化物(利用磁性性質);菠菜中鐵元素的檢驗等[1]。課堂中老師還可以使用青磚紅磚、紫砂泥、植物補鐵花肥、食品脫氧劑等情境素材,可謂是眼花繚亂。如何利用好情境素材,讓情境素材發揮它應有的功能,筆者認為主要應從三方面思考。
1.提高情境的選擇力
情境素材一定要有所取舍,找到一個核心情境貫穿到底,不要被光怪陸離的情境所迷惑,要回到學科的本位來思考。教學中最怕的是情境的大拼盤,每解決一個學科問題就展示一個情境,沒有一個完整的解決問題的主情境。情境的使用是為了讓問題更有價值,是為了引導問題的產生,是為了使教學活動順利展開,是為了使學生的思維不斷提升。因此,選擇一個好的情境相當重要。
如某案例以實驗室里變質的綠礬晶體作為情境素材,以感知綠礬—檢驗綠礬—保存綠礬作為教學主線,通過設置問題情境將整個教學內容融合其中。表1是設計的問題情境和蘊含的素養目標。
這個案例選取的情境簡潔直觀,與化學實驗室的綠礬試劑保存息息相關,以往對于綠礬的情境使用,僅僅在介紹應用的時候閃現一下,而本節課在教學中從始至終圍繞綠礬設計了一系列的“問題串”,緊扣主題,讓學生不斷在“為什么”和“是什么”的問題思考中,激起自主探究的欲望。
2.突出學科本質
在這節課的教學中會遇到這樣一個問題,如何檢驗 Fe2+?學生通過 Fe3+的檢驗很容易想到用 KSCN溶液,那么先加 KSCN溶液還是先加氯水氧化呢?這里面就涉及化學檢驗當中的邏輯問題,Fe2+檢驗中先加 KSCN溶液,有兩個功能:一是作為未來產品的檢驗試劑,即用于生成的產物Fe3+的檢驗。二是作為排除劑,排除檢驗的試劑中有沒有Fe3+。學生理清這兩個功能后,就很容易得出先加氯水、雙氧水等氧化劑顯然違背了物質檢驗的邏輯。
緊接著拋出另一個問題,Fe2+和Fe3+混合溶液中,如何檢驗Fe2+?學生如果還用Fe2+的檢驗邏輯是行不通的,學生會想到排除干擾,可不可以把Fe3+除去再檢驗呢?化學學科的本質就是科學邏輯問題,物質檢驗的核心問題就是排除干擾。
3.體現科學精神
什么是科學精神?堅持以科學的態度看待問題、評價問題而不借用非科學或偽科學的手段。科學精神的核心是實事求是、開拓創新,這需要實驗的嚴格檢驗和理性的無情審查。所以科學精神的兩大支柱是實證精神和理性精神。科學需要實證。要證明溶液中有 Fe3+,借助 KSCN 溶液,看到有血紅色產生,說明溶液中一定有Fe3+。在化學教學中,有獨特的實證精神,就是用物質來證明物質,如 SCN-遇到 Fe3+有血紅色現象,就是用SCN-證明Fe3+的存在。科學需要理性。理性是靠縝密的邏輯,如Fe2+的檢驗,當學生先加氯水,再加 KSCN溶液,發現溶液也變成血紅色,說明一定有Fe3+,但是不代表Fe3+就是氧化生成的Fe3+,Fe3+怎么來的?也有可能是溶液中本身就存在Fe3+,你得到了你所想要的現象不一定能夠證明Fe3+的存在,這就是科學的理性。理性精神促進科學的誕生和發展,科學的成長又反過來發揚光大理性精神。讓學生通過實驗探究不斷地對已學的知識進行實證,并不斷地進行理性思考是我們教學的最終目標。
二、學科理解的思考
化學學科理解是指教師對化學學科知識及其思維方式和方法的一種本原性、結構化的認識,它不僅僅只是對化學知識的理解,還包括對具有化學學科特質的思維方式和方法的理解[1]。站在學科理解的高度,鐵及其化合物這節內容在教材中的地位不容小覷,最重要的核心地位就是在氧化還原反應中怎么實現Fe2+和Fe3+的相互轉化以及轉化的動力問題。
1.轉化的認知
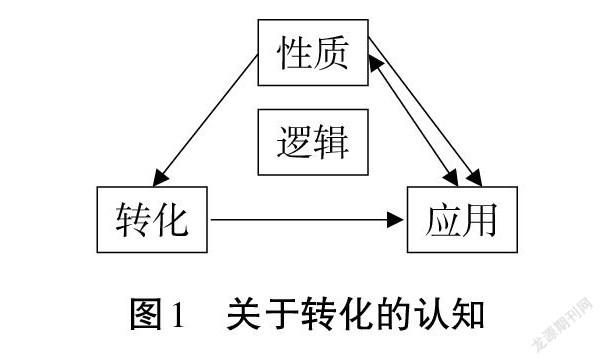
在 Fe2+和 Fe3+的相互轉化這一環節教學中,教師習慣于先提供試劑給學生,提供常見的氧化劑和常見的還原劑,讓學生設計實驗方案,分析方案的可行性后,學生再動手做實驗。學生能夠設計實驗方案實現轉化是基于學生對 Fe2+和 Fe3+的性質的掌握,性質掌握后驅動它的應用,通過探究轉化的方式進行應用,對 Fe2+和 Fe3+的轉化應作為一個系統,不要把它割裂開,在應用中整合,性質、轉化、應用三者之間靠什么驅動,就是邏輯(見圖1)。
2.轉化的動力
Fe2+和 Fe3+的相互轉化背后的推手是什么?轉化后面有什么樣的規律?轉化的動力是什么?是我們這節課需要深入思考的點。通過這一節課,我們進一步認識了氧化性和還原性,氧化劑和還原劑的相對強弱問題應該要得到鞏固和加強,由此可以引導學生思考這樣的問題:Fe2+有還原性,Fe2+→Fe3+的轉化是很容易自發的,比如在空氣中被氧化,學生通過實驗知道氯氣、雙氧水、溴水可以把Fe2+氧化,通過這些反應可以得出這幾種氧化劑的氧化性與Fe3+的關系,這幾種氧化劑之間也有強弱順序,值得進一步深思,這一節課有個基本的序:MnO4->Cl2>Br2>Fe3+,應該在教學中讓學生明白。Fe3+→Fe2+的轉化要控制還原劑的種類,從還原性的序可以得出:Mn2+ 三、相關實驗的思考 在這節課的教學中涉及很多的探究實驗,實驗過程中的細節處理也是不容忽視的。 1.Fe粉與FeCl3溶液的反應 教學中講到 Fe3+→Fe2+的轉化時不可避免地要讓學生做 Fe粉與 FeCl3溶液反應的實驗,這個實驗短時間內想要看到Fe2+的淺綠色很難,由于鐵粉的原因會渾濁一片,如何處理呢?如果教室里有個離心機或者直接過濾,溶液的淺綠色看得很明顯,很多時候條件是不允許的,這時如果用一團小棉花或者濕紙巾,往里面搗一搗,就達到過濾的效果了,快速便捷。還是這個反應,在教學中讓學生觀察現象時,學生會說有氣泡產生,與你想要的答案相差甚遠,怎么辦?很多老師在教學中視而不見、不回答。這個現象不能視而不見,為什么有氣泡?是什么氣泡呢?或直接告訴學生這個氣泡是氫氣,為什么會有氫氣?顯然 FeCl3溶液是酸性,而且酸性比較強,Fe 粉加入以后不僅和 Fe3+反應,還和 H+反應,這兩個反應同時開始,沒有所謂的先后,因為H+作為質子,擴散速率是很高的。 2.Cu粉與FeCl3溶液的反應 銅還原 FeCl3溶液的實驗,蘇教版教材中設計了如下活動與探究:用毛筆蘸取少量30%的 FeCl3溶液,在銅片上畫一個“+”,放置片刻后,用少量水將銅片上的溶液沖至小燒杯中。學生能夠觀察到的現象是:“+”處有明顯的被腐蝕痕跡,沖洗后的溶液藍色不是很明顯。 現行人教版必修1教材中設計如下的實驗:取一小塊覆銅板,用油性筆在覆銅板上畫上設計好的圖案,然后浸入盛有 FeCl3溶液的小燒杯中。過一段時間后,取出覆銅板并用水清洗干凈,學生能夠觀察到的現象是:油性筆未畫過的覆銅板被腐蝕了,但是小燒杯中的FeCl3溶液其實短時間內變化不明顯。 這兩個方案的設計關鍵是反應物量的問題,在教學中可以換用 Cu粉與 FeCl3溶液的試管實驗,溶液中的藍色可以很清晰地看出,如果進一步追問怎么檢驗反應后的溶液中是否含有 Fe3+?顯然滴加 KSCN 溶液,這時會發現有異常現象,產生白色沉淀,白色沉淀是什么呢?會不會是CuCl?會不會是CuSCN?這里0價的銅被氧化的過程中,價態升高的時候不一定全部變成了+2價的銅,主要與 FeCl3溶液的濃度有很大關系。當然通過比較CuSCN的Ksp=4.8×10-15,CuCl的Ksp=1.72×10-7,溶液中 SCN-的濃度太低,Cl-濃度大得多,生成CuSCN可能性不大。 3.H2O2溶液與FeCl2溶液的反應 實驗探究 Fe2+→Fe3+的轉化時,氧化劑如果選擇 H2O2溶液,先滴加 KSCN溶液,再滴加 H2O2溶液,往往血紅色溶液看不出,顯然不是Fe2+不被H2O2溶液氧化,而是又發生氧化還原反應,KSCN被 H2O2溶液氧化為硫氰酸根(SCNO-),在教學中可以與學生探討是 Fe3+繼續被氧化了,還是SCN-被氧化了?只需向溶液中繼續滴加KSCN溶液,如溶液變成血紅色,則可以證明。 化學知識是培養學生化學學科核心素養的重要載體,在現行的課堂教學中,對化學教師的專業素養提出了更高的要求,要求教師進一步增進化學學科理解。這節課關于實驗方面的細節點還有很多,當然一節課也不一定要把細節都處理掉,教學是無止境的。 美國課程專家埃里克森認為“學生的學習重心應該從記憶事實轉移到可遷移的核心觀念和對更為根本的知識結構進行深層理解,培養和發展思維能力”[2]。元素化合物的知識是進行物質轉化教學的有效載體,在教學中不能單純只記憶相關轉化的反應物質、反應方程式,更多地要結合化學實驗,帶領學生探究實驗現象背后蘊藏的化學原理、化學本質,用反應原理來解釋物質轉化的一般邏輯,使學生的認識能夠基于知識又超越知識,實現認識事物方式的轉變和加強對化學學科的理解,這是提升學生解決問題能力和化學思維能力的重要教學策略[3]。 參考文獻 [1] 中華人民共和國教育部.普通高中化學課程標準(2017年版2020年修訂)[S]. 北京:人民教育出版社,2020. [2] 田長明.基于“物質轉化觀”的元素化合物教學——以“奇妙的碘”為例[J].化學教學,2016(7):47-49. [3] 何彩霞,余麗蓉.多角度地認識化學反應[J]. 教學儀器與實驗,2014(9):3-7.

