雙線統攝,多維探究
繆徐

摘 要:情境真實化、知識結構化,是《義務教育化學課程標準(2022年版)》倡導的教學理念。針對初中化學核心概念教學中知識的結構性、思維的深刻性的提高,做了相關的探索。滬教版初中化學九年級下冊《溶液組成的表示》第一課時的教學,教學情境具有貫穿性,教學流程以活動線統攝,教學活動聚焦學生思維的流動。
關鍵詞:初中化學;教學情境;認知維度;大概念;《溶液組成的表示》
* 本文系江蘇省教育科學“十四五”規劃課題“‘雙減背景下素養式化學教學方式變革的課例研究”(編號:Ec/2021/44)的階段性研究成果。
情境真實化、知識結構化,是《義務教育化學課程標準(2022年版)》(以下簡稱“新課標”)倡導的教學理念。如何提高初中化學核心概念教學中知識的結構性、思維的深刻性,實現“知識傳授”到“素養提升”的轉變?筆者做了相關的探索。現結合滬教版初中化學九年級下冊《溶液組成的表示》第一課時的教學實例,做闡釋說明。
一、 教學思路
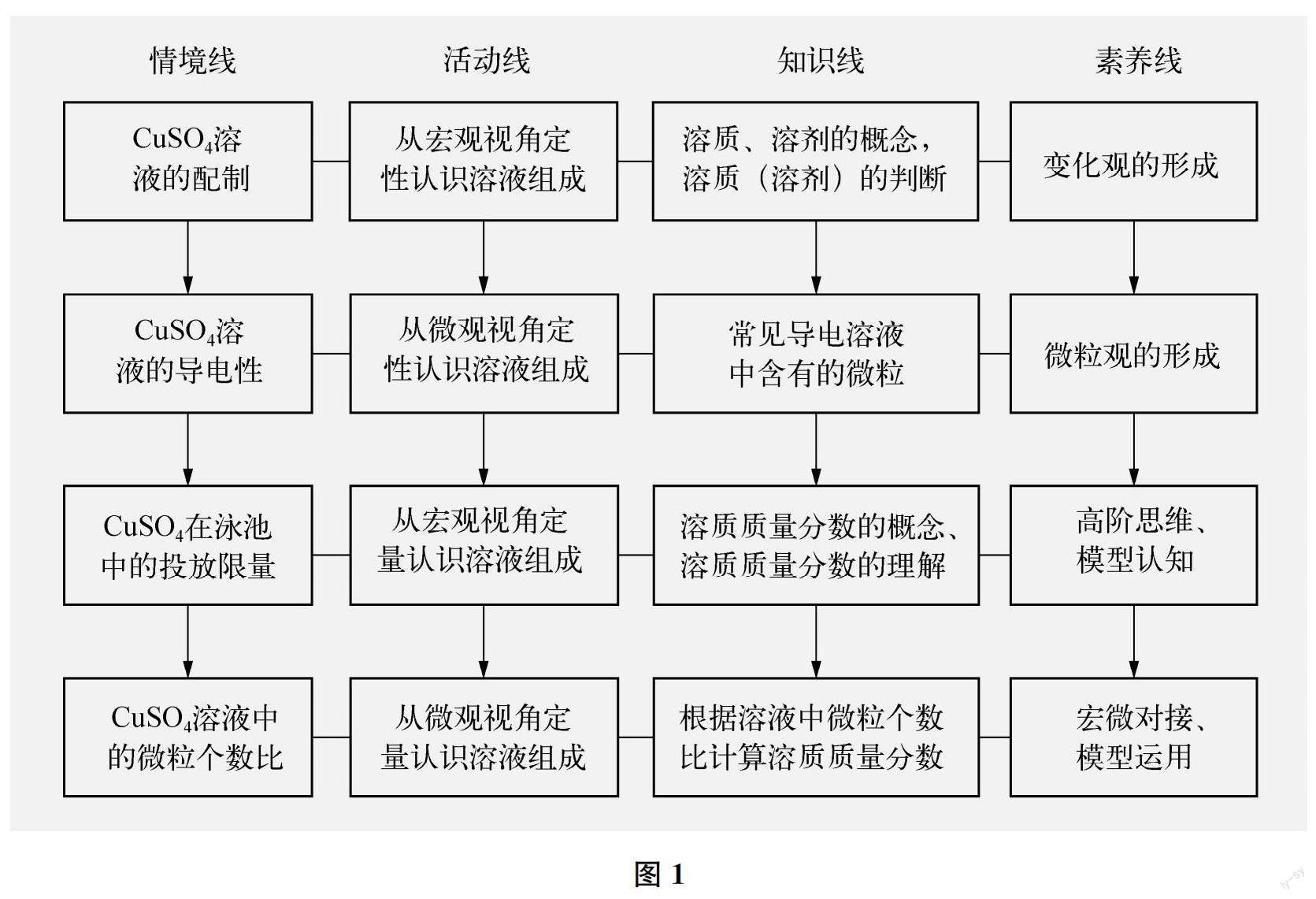
溶質、溶劑、溶質質量分數,是滬教版初中化學九年級下冊《溶液組成的表示》第一課時中的3個核心概念。教學時,可以用學生較為熟悉的硫酸銅溶液創設情境線,用“多維度認識溶液組成”(溶液組成有宏觀、微觀兩種認識視角及定性、定量兩種表征形式)的大概念視角創設活動線,以此來統攝3個核心概念的教學。具體思路見下頁圖1。
二、 教學過程
(一) 從宏觀、定性的視角認識溶液組成
師 同學們,(展示硫酸銅溶液)
這瓶藍色溶液在前面的學習中曾出現過兩次,還記得嗎? ?(學生回顧、交流。)
師?今天,我們將以硫酸銅溶液為線索來研究新的問題——溶液組成的表示。
師?(課件呈現硫酸銅溶液配制過程的示意圖)
在硫酸銅溶液的配制過程中,被溶解的物質、能溶解其他物質的物質分別是什么?
生?硫酸銅、水。
師?對照教材上溶質、溶劑的概念,說一說這兩種物質的歸類。
生?硫酸銅是溶質,水是溶劑。
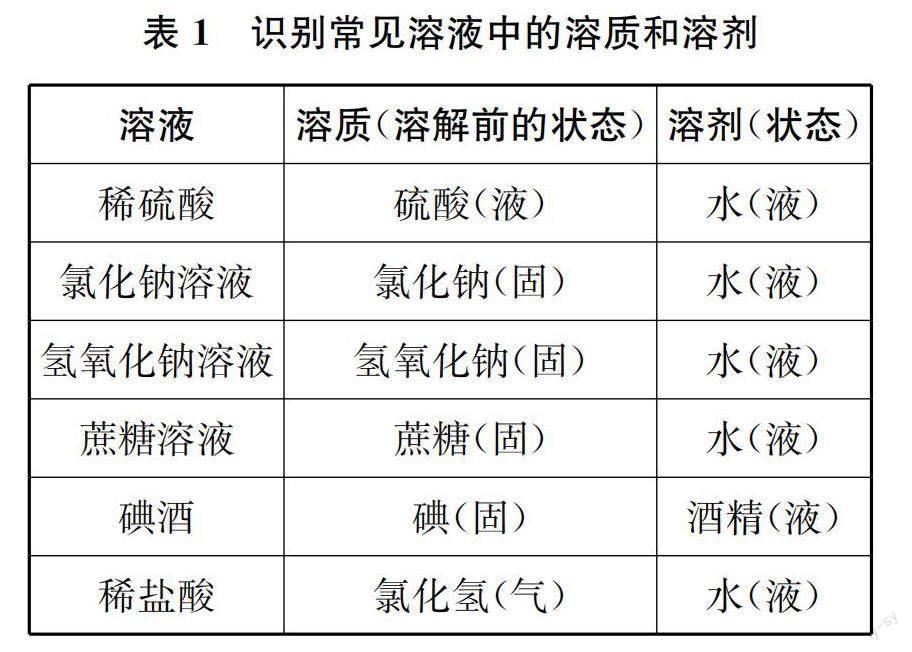
師?帶著對溶質、溶劑概念的初步認識,我們來填寫表格。(學生填寫表格,教師巡視指導,最終得到表1。)
師?從表格中,同學們能總結出溶質、溶劑識別的一般規律嗎?
生?固液相溶,固體為溶質,液體為溶劑;氣液相溶,氣體為溶質,液體為溶劑;液液相溶,非水液體為溶質,水為溶劑;如果兩種液體都不是水,則量少的液體為溶質,量多的液體為溶劑。
師?硫酸銅溶液中的溶質是硫酸銅,如果硫酸銅溶液與氫氧化鈉溶液恰好完全反應,所得溶液中的溶質是什么?
生?硫酸鈉。
師?如果硫酸銅溶液和鐵粉恰好完全反應,所得溶液中的溶質又是什么?
生?硫酸亞鐵。
師?從宏觀、定性的角度看,溶液由溶質和溶劑組成,在判斷溶質、溶劑的過程中,要注意規律的運用,還要注意溶質的變化。
[設計意圖:借助硫酸銅溶液的配制,引出“被溶解和能溶解”的話題,幫助學生建立溶質、溶劑的初步概念。通過常見溶液中溶質、溶劑的識別,總結識別規律,拓展學生認知寬度。通過硫酸銅溶液與氫氧化鈉溶液、鐵粉兩個化學反應的再現,重回教學情境,提高學生認知深度。]
(二) 從微觀、定性的視角認識溶液組成
師?前面的學習中曾分析過稀硫酸、氯化鈉溶液、氫氧化鈉溶液等導電的原因,請同學們回憶、交流。
生?稀硫酸能夠導電,是因為其中含有自由移動的氫離子和硫酸根離子;氯化鈉溶液能夠導電,是因為其中含有自由移動的鈉離子和氯離子;氫氧化鈉溶液能夠導電,是因為其中含有自由移動的鈉離子和氫氧根離子。
師?硫酸銅溶液也能導電,原因是什么?
生?因為硫酸銅溶液中含有自由移動的銅離子和硫酸根離子。
師?從微觀、定性的角度看,溶液的組成該如何描述?
生?溶液由溶質離子(分子)和溶劑分子等微粒構成。
[設計意圖:通過稀硫酸、氯化鈉溶液、氫氧化鈉溶液等導電原因的回憶,將溶液組成的認識思路由宏觀轉向微觀,然后回到硫酸銅溶液導電原因的分析上。這樣,既豐富了學生從微觀角度認識溶液組成的素材,又保持了以硫酸銅溶液為主角所創設的教學情境的一致性。]
(三) 從宏觀、定量的視角認識溶液組成
師?在溶液的實際應用中,有時僅僅知道溶液的定性組成還不夠,還需要了解溶液的定量構成。讓我們沿著硫酸銅溶液這條主線繼續開展探究活動。(課件呈現泳池的畫面)
為了消毒殺菌,通常會向泳池的水中加入一定量的硫酸銅。有關資料表明,為了減少硫酸銅這種有毒物質對人體的傷害,泳池水中硫酸銅的含量一般要控制在0.000025%-0.00005%之間。你知道這里的百分數的含義嗎?
生?溶液中溶質的質量占比,也叫溶質質量分數。
師?在化學實驗室里,某同學將1g硫酸銅完全溶解于19g水中,所得溶液中硫酸銅的質量分數為多少?
生??1g/1g+19g×100%=5%。
師?溶質質量分數是一個比值,它和我們先前學過的眾多比值中的哪些比值在內涵上最為接近。可以從比的方向(橫向還是豎向)、比的方式(局部與局部還是局部與整體)、比的結果(整數比還是小于100%的比)等幾個方面去思考。
生?和赤鐵礦中氧化鐵的質量分數最接近——都是豎向的比,都是局部與整體的比,都是結果小于100%的比……
師?請同學們結合剛才的學習內容,對溶液的組成做一個簡要的小結。
生?從宏觀、定量的角度看,溶液的組成可以用溶質的質量分數來表示。
[設計意圖:借助泳池中硫酸銅含量的限定范圍,將溶液組成的認識視角從定性轉向定量,幫助學生建立溶質質量分數的概念。通過實驗室配制硫酸銅溶液的計算,讓學生進一步理解概念。通過已學的各種“比”的多角度對比,促進學生加深概念理解,完善知識結構,培養高階思維。]
(四) 從微觀、定量的視角認識溶液組成
師 (指板書,見下頁圖2)黑板上的板書還缺一部分,同學們預測一下,此處應該寫什么?沒錯,從微觀、定量的視角去認識溶液的組成。已知硫酸銅溶液中銅離子和水分子的個數比為1∶170,求該溶液中硫酸銅的質量分數。
生?約為5%。
師?能把你解決問題的思路和大家分享一下嗎?
生?由硫酸銅溶液中銅離子和水分子的個數比,求算銅離子和水分子的質量比,再算硫酸銅和水的質量比,最終得出硫酸銅溶液中溶質的質量分數。
師?顯然,溶液的組成也可以用溶液中溶質微粒與溶劑微粒(通常為水分子)的個數比來表示。這種微觀、定量的數值可以轉化為宏觀、定量的表示結果。
師 (小結)九年級開始學化學至今,我們和硫酸銅溶液打過三次交道——初遇硫酸銅,認識了質量守恒定律;二遇硫酸銅,了解了鐵與其發生置換反應的性質;三遇硫酸銅,從不同的視角認識了溶液的組成。可以說,遇見一次硫酸銅,我們的眼界就開闊一次。這就是成長,這就是飛躍!
[設計意圖:借助板書缺角的觀察、思考,引出最后一個認識問題的角度——從微觀、定量的視角認識溶液的組成。通過學生思維路線的呈現,培養學生的有序思維習慣和語言表達能力;同時,也讓學生意識到認識溶液的組成有多個視角(宏觀、微觀;定性、定量),這些認識視角可以彼此切換,認識結果也可以相互轉化。最后的結語將學習和成長相連,意在激勵學生努力學習、享受學習,尋求生命飛躍。]
三、 教學反思
(一) 教學情境具有貫穿性
新課標指出,“真實、生動、直觀且富有啟迪性的情境,能夠激發化學學習興趣,引發學生的思考,幫助學生建構大概念和核心概念,促進學生核心素養的發展”[1]。
硫酸銅溶液先后在教材第4章、第5章的學習中出現過,是學生較為熟悉的一種溶液。用硫酸銅溶液創設的情境主線,環環相扣,一“境”到底。這種貫穿式的教學情境避免了目前大多數中學化學教學中的“脫境”(創設的情境只能用于新課導入,后面的教學脫離該情境)和“多境”(一節課創設多個教學情境)現象,提高了教學的流暢性,為本節課的教學推進提供了邏輯基礎。
(二) 教學流程以活動線統攝
對于“物質的組成”這一大概念,新課標是這樣解讀的:初步形成基于元素和分子、原子認識物質及其變化的視角,建立認識物質的宏觀和微觀視角之間的關聯,知道物質的性質與組成、結構有關。[2]“多維度認識溶液的組成”是“物質的組成”大概念和本課教學內容結合的產物,即“課時大概念”。
在“多維度認識溶液的組成”這一課時大概念的統攝下,“溶液的組成”的學習有四條路徑:宏觀、定性;微觀、定性;宏觀、定量;微觀、定量。核心概念的學習不再是碎片化的,而是一種整體建構式的探索,這樣的教學也有了單元教學的意蘊。溶質、溶劑、溶質質量分數就不再是沒有邏輯的“知識拼盤”,而是組成了一個彼此關聯的“學習小主題”。這個學習小主題與基于物質的視角認識氣態混合物的組成、基于物質的視角認識固態混合物的組成以及基于元素的視角認識純凈物的組成等主題,共同豐富了“物質的組成”大概念的內涵。
因為有“多維度認識溶液組成”這一課時大概念的統攝,“從宏觀的視角定性認識溶液組成”“從微觀的視角定性認識溶液組成”“從宏觀的視角定量認識溶液組成”“從微觀的視角定量認識溶液組成”等4個活動,形成了一個角度有異、指向一致的活動鏈。這樣的活動鏈,消除了學生碎片化的學習,催生了他們結構化的認知。
(三) 教學活動聚焦學生思維的流動
思維是課堂教學的核心,是學生發展的關鍵。不管課堂教學采用什么樣的方式,如果抓不住學生的思維,沒有學生思維的積極流動,特別是高水平的思維流動,就不可能將知識轉化為能力,也不可能將知識上升為觀念,更不可能促進學生核心素養的發展。[3]
在多途徑認識溶液的組成的學習過程中,學生經歷了多次高水平的思維流動。比如,在溶質、溶劑的概念建立后,返回硫酸銅溶液情境的過程中,教師要求學生思考氫氧化鈉溶液、鐵粉分別與硫酸銅溶液恰好反應后所得溶液中的溶質。這不僅打通了“物質的組成與結構”“物質的性質與應用”“物質的化學變化”等學習主題之間的知識壁壘,而且讓學生學會從變化的視角辨識溶質,加深了學生對溶質內涵的理解。又如,在溶質質量分數的概念建立后,教師沒有立刻讓學生做題鞏固,而是用一個思考題將學生的思維引向深處:溶質質量分數是一個比值,它和我們先前學過的眾多比值中的哪些比值在內涵上最為接近?通過回憶和比對,建立“溶質質量分數”模型(豎比,局部對整體,小于100%的比),為下一個高水平的思維流動——用模型從微觀的視角定量認識硫酸銅溶液的組成,奠定了堅實的基礎。
參考文獻:
[1][2] 中華人民共和國教育部.義務教育化學課程標準(2022年版)[S].北京:北京師范大學出版社,2022:44,23.
[3] 畢華林.促進核心素養發展的化學課程改革——《義務教育化學課程標準(2022年版)》的研制及其變化[J].中學化學教學參考,2022(11):9.

